Ammonium nitrat
| |
| |

| |
| Nama | |
|---|---|
| Nama IUPAC
Ammonium nitrat
| |
| Pengecam | |
Imej model 3D Jmol
|
|
| ChemSpider | |
| ECHA InfoCard | 100.026.680 |
| Nombor EC |
|
PubChem CID
|
|
| Nombor RTECS |
|
| UNII | |
| Nombor PBB | 0222 – dengan > 0.2% bahan mudah terbakar 1942 – dengan <= 0.2% bahan mudah terbakar 2067 – baja 2426 – cecair |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| NH4NO3 | |
| Jisim molar | 80.043 g/mol |
| Rupa bentuk | Pepejal putih atau kelabu |
| Ketumpatan | 1.725 g/cm3 (20 °C) |
| Takat lebur | 169.6 °C (337.3 °F; 442.8 K) |
| Takat didih | anggaran 210 °C (410 °F; 483 K) Terurai |
| Endotermik 118 g/100 ml (0 °C) 150 g/100 ml (20 °C) 297 g/100 ml (40 °C) 410 g/100 ml (60 °C) 576 g/100 ml (80 °C) 1024 g/100 ml (100 °C)[1] | |
| -33.6·10−6 cm3/mol | |
| Struktur | |
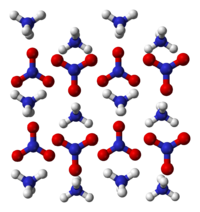
| Struktur kristal | Trigonal |
| Data bahan letupan | |
| Kepekaan kejutan | Amat rendah |
| Kepekaan geseran | Amat rendah |
| Detonation velocity | 2500 m/s |
| Bahaya | |
| Bahaya-bahaya utama | Bahan letupan, pengoksidaan |
| Piktogram GHS |   
|
| Perkataan isyarat GHS | Danger |
| H201, H271, H319 | |
| P220, P221, P271, P280, P264, P372 | |
| NFPA 704 (berlian api) | |
| Dos maut (LD) atau kepekatan dos maut (LC) | |
LD50 (median dos)
|
2085–5300 mg/kg (tikus, oral)[2] |
| Sebatian berkaitan | |
Anion lain
|
Ammonium nitrit |
Kation lain
|
Natrium nitrat Kalium nitrat Hidroksilammonium nitrat |
Sebatian berkaitan
|
Ammonium perklorat |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| | |
| Rujukan kotak info | |
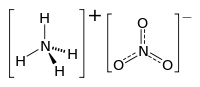
Ammonium nitrat ialah sebatian kimia dengan formula kimia NH4NO3 yang berwarna putih serta sangat larut dalam air. Sebatian ini terdiri daripada kation ammonium dan anion nitrat.
Sebatian ini biasanya digunakan dalam bidang pertanian sebagai baja nitrogen.[4] Tambahan pula, sebatian ini juga digunakan sebagai bahan letupan dalam bidang pelombongan dan pembinaan awam.
Penghasilan[sunting | sunting sumber]
Ammonium nitrat dihasilkan dalam industri melalui tindak balas asid dan bes, yakni antara ammonia dan asid nitrik.[5]
Tindak balas[sunting | sunting sumber]
Ammonium nitrat bertindak balas dengan hidroksida logam untuk menghasilkan ammonia dan nitrat logam alkali. Dalam persamaan di bawah, M mewakili logam alkali seperti natrium dan kalium.
Ammonium nitrat akan terurai menjadi nitrus oksida dan air apabila dipanaskan.
Walau bagaimanapun, dalam letupan atau pembakaran pantas, ammonium nitrat akan terurai menjadi gas nitrogen, gas oksigen dan air.
Keselamatan[sunting | sunting sumber]
Bencana[sunting | sunting sumber]
Ammonium nitrat terurai menjadi nitrus oksida dan wap air apabila dipanaskan, tetapi boleh terurai secara letupan. Sifat ammonium oksida sebagai pengoksida boleh memarakkan letupan dengan mudah, menjadikan ammonium nitrat memiliki risiko kebakaran yang besar.
Letupan kecil yang melibatkan ammonium hidroksida adalah agak lazim, tetapi beberapa bencana besar pernah direkodkan seperti:
- bencana Texas City pada 16 April 1947 yang berlaku akibat letupan lebih kurang 2,086 tan metrik sebatian ini;[6]
- letupan di Tianjin, China pada 12 Ogos 2015 yang melibatkan kira-kira 800 tan sebatian ammonium nitrat; jumlah kematian rasmi ialah 173 orang dengan kira-kira 800 orang kematian;[7][8]
- letupan di Pelabuhan Beirut, Lubnan pada 4 Ogos 2020 yang berpunca daripada kira-kira 2,750 tan ammonium nitrat yang disimpan di gudang pelabuhan itu.[9]
Sesetengah daripada letupan ini direkodkan sebagai salah satu letupan bukan nuklear terbesar yang pernah dicatat.
Bahaya kesihatan[sunting | sunting sumber]
Ammonium nitrat tidak berbahaya kepada kesihatan dan biasanya digunakan dalam produk baja. [10] [11] [12]
Ammonium nitrat mempunyai LD 50 bagi setiap 2217 mg/kg, [13] yang mana sebagai perbandingan adalah kira-kira dua pertiga daripada garam meja sahaja.
Rujukan[sunting | sunting sumber]
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ^ Martel, B.; Cassidy, K. (2004). Chemical Risk Analysis: A Practical Handbook. Butterworth–Heinemann. m/s. 362. ISBN 1-903996-65-1.
- ^ "Archived copy". Diarkibkan daripada yang asal pada 2015-02-17. Dicapai pada 2015-03-13.CS1 maint: archived copy as title (link)
- ^ Karl-Heinz Zapp "Ammonium Compounds" in Ullmann's Encyclopedia of Industrial Chemistry 2012, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a02_243
- ^ "Archived copy" (PDF). Diarkibkan daripada yang asal (PDF) pada 2012-01-23. Dicapai pada 2008-11-11.CS1 maint: archived copy as title (link)
- ^ "Texas City, Texas Disaster" (dalam bahasa Inggeris). Fire Prevention and Engineering Bureau of Texas. 29 April 1947. Dicapai pada 8 Ogos 2020.
- ^ "Tianjin explosion: China sets final death toll at 173, ending search for survivors". The Guardian (dalam bahasa Inggeris). Associated Press. 12 September 2015. Dicapai pada 8 Ogos 2020.
- ^ "155位"8–12"事故遇难者身份公开". Sohu. 2 September 2015. Diarkibkan daripada yang asal pada 2015-09-14. Dicapai pada 2 September 2015.
- ^ Gadzo, Mersiha (4 Ogos 2020). "Dozens killed, thousands wounded in Beirut blast: Live updates" [Berdozen-dozen terbunuh, beribu-ribu tercedera dalam letupan Beirut: Kemas kini langsung]. Al Jazeera (dalam bahasa Inggeris). Diarkibkan daripada yang asal pada 4 Ogos 2020. Dicapai pada 4 Ogos 2020.
- ^ CF Industries. "Ammonium nitrate MSDS" (PDF). Diarkibkan daripada yang asal (PDF) pada 27 March 2014.
- ^ "Chemicalland21 – Ammonium Nitrate". Diarkibkan daripada yang asal pada 10 January 2012.
- ^ "Ammonium Nitrate". Paton Fertilizers Pty Ltd. 2005.
- ^ "Material Safety Data Sheet, Ammonium nitrate MSDS".
Pautan luar[sunting | sunting sumber]
 Media berkenaan Ammonium nitrat di Wikimedia Commons
Media berkenaan Ammonium nitrat di Wikimedia Commons





