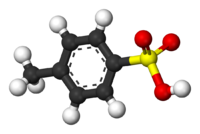
Asid p-toluenasulfonik

| |
| |
| Nama | |
|---|---|
| Nama IUPAC pilihan
Asid 4-metilbenzena-1-sulfonik 4-Methylbenzene-1-sulfonic acid | |
| Nama lain
Asid tosilik
| |
| Pengecam | |
Imej model 3D Jmol
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.002.891 |
| KEGG | |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C7H8O3S | |
| Jisim molar | 172.20 g/mol (kontang) 190.22 g/mol (monohidrat) |
| Rupa bentuk | Pepejal putih |
| Ketumpatan | 1.24 g/cm3 |
| Takat lebur | 38 °C (100 °F; 311 K) (kontang)[2] 103 hingga 106 °C (217 hingga 223 °F; 376 hingga 379 K) (monohidrat) |
| Takat didih | 140 °C (284 °F; 413 K) at 20 mmHg |
| 67 g/100 mL | |
| Keasidan (pKa) | −2.8 (Air)[3] 8.5 (Asetonitril)[4] |
| Struktur | |
| Bentuk molekul | Tetrahedron di S |
| Bahaya | |
| Bahaya-bahaya utama | Merengsa kulit |
| MSDS | External MSDS |
| Frasa R | R36/37/38 |
| Frasa S | S26 |
| Sebatian berkaitan | |
Asid sulfonik berkaitan
|
Asid benzenasulfonik Asid sulfanilik |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| | |
| Rujukan kotak info | |
Asid p-toluenasulfonik atau asid tosilik ialah sejenis asid dan sebatian organik dengan formula kimia CH3C6H4SO3H atau TsOH secara ringkas. Sebatian ini terdiri daripada kumpulan tosil, CH3C6H4SO2– yang boleh diringkaskan dengan simbol Ts. Asid ini memiliki dua jenis, yakni jenis kontang dan jenis monohidrat, TsOH.H2O. Sebatian ini umumnya digunakan sebagai mangkin dalam tindak balas organik.
Ester-ester terbitan asid ini dipanggil sebagai tosilat.
Sifat[sunting | sunting sumber]
Asid p-toluenasulfonik terurai dalam pemanasan dan menghasilkan sulfur dioksida. Garam barium dan sulfurnya, tidak seperti dalam asid sulfurik, larut dalam air.[5]
Penghasilan[sunting | sunting sumber]
Asid ini dihasilkan melalui pensulfonaan toluena dalam industri. Penulenan dapat dibuat melalui penghabluran semula dalam larutan akueus pekat dan seterusnya, pengeringan azeotrop dengan toluena.[6]
Kegunaan[sunting | sunting sumber]
Sebatian ini digunakan sebagai mangkin dalam tindak balas organik seperti pengasetalan, pengesteran dan pendehidratan.[7]
Rujukan[sunting | sunting sumber]
- ^ Merck Index, Edisi ke-11, 9459.
- ^ Armarego, Wilfred (2003). Purification of Laboratory Chemicals. Elsevier Science. m/s. 370. ISBN 0-7506-7571-3.
- ^ Guthrie, J. P. Hydrolysis of esters of oxy acids: pKa values for strong acids. Can. J. Chem. 1978, 56, 2342-2354.
- ^ Eckert, F.; Leito, I.; Kaljurand, I.; Kütt, A.; Klamt, A.; Diedenhofen, M. Prediction of Acidity in Acetonitrile Solution with COSMO-RS. J. Comput. Chem. 2009, 30, 799-810. doi:10.1002/jcc.21103
- ^ Beyer-Walter, Lehrbuch der Organischen Chemie, 23. Auflage, S. Hirzel Verlag 1998 ISBN 3-7776-0808-4
- ^ Perrin, D. D.; Armarego, W. L. F. (1988). Purification of Laboratory Chemicals. Oxford: Pergamon Press. Unknown parameter
|lastauthoramp=ignored (bantuan) - ^ "Methylbenzolsulfonsäuren". Römpp Online (dalam bahasa Jerman). Dicapai pada 1 September 2019.
