Miastenia gravis
| Miastenia gravis | |
|---|---|
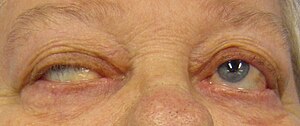 | |
| Penyimpangan mata dan kelopak mata yang terkulai pada orang yang menghidap miastenia gravis yang cuba membuka matanya | |
| Pengkhususan | Neurologi |
| Gejala | Tahap kelemahan otot bervariasi, penglihatan berganda, kelopak mata terkulai, masalah bercakap, masalah berjalan[1] |
Permulaan biasa | Wanita di bawah 40, lelaki berusia lebih dari 60 [1] |
| Tempoh | Jangka panjang[1] |
| Punca | Penyakit autoimun[1] |
| Ujian darah untuk antibodi spesifik , ujian edrofonium, kajian konduksi saraf[1] | |
| sindrom Guillain–Barré, botulisme, keracunan organofosfat, strok batang otak[2] | |
| Rawatan | Ubatan, pembedahan membuang timus, plasmaferesis[1] |
Rawatan perubatan | Perencat asetilkolinesterase (neostigmina, pyridostigmine), imunosupresan[1] |
| Kekerapan | 50 hingga 200 setiap juta[3][4] |
| sunting | |
Miastenia gravis (MG) adalah penyakit neuromuskular jangka panjang yang membawa kepada pelbagai tahap kelemahan otot rangka.[1] Otot yang paling kerap terkena adalah otot mata, muka, dan menelan.[5] Ini akan mengakibatkan penglihatan berganda, kelopak mata yang terkulai, masalah berbicara, dan masalah berjalan. Permulaan boleh berlaku secara tiba-tiba. Mereka yang terkena selalunya mempunyai timus yang besar atau mengalami timoma.[1]
Miastenia gravis adalah penyakit autoimun yang berpunca daripada antibodi yang menyekat atau memusnahkan reseptor asetilkolin nikotinik (AChR) di persimpangan antara saraf dan otot.[6][7][1] Ini menghalang impuls saraf untuk mencetuskan pengecutan otot. Sebilangan besar kes disebabkan oleh antibodi imunoglobulin G1 (IgG1) dan IgG3 yang menyerang AChR pada membran pascasinaptik, menyebabkan kerosakan pada perantara pelengkap dan kelemahan otot.[8] Kecacatan genetik pada simpang neuromuskular yang diwarisi dan mengakibatkan keadaan serupa yang dikenali sebagai miastenia kongenital adalah jarang berlaku.[9][10] Bayi yang ibunya mempunyai miastenia mungkin mengalami simptom selama beberapa bulan pertama kehidupan mereka, yang dikenali sebagai miastenia neonatal. Diagnosis dapat disokong dengan ujian darah untuk antibodi tertentu, ujian edrofonium, atau kajian konduksi saraf.
MG umumnya dirawat dengan ubat-ubatan yang dikenali sebagai perencat asetilkolinesterase, seperti neostigmina dan pyridostigmine.[1] Imunosupresan, seperti prednison atau azatioprina, juga boleh digunakan. Pembuangan timus secara pembedahan dapat memperbaiki gejala dalam kes tertentu. Plasmaferesis dan imunoglobulin intravena berdos tinggi boleh digunakan semasa keadaan mendadak. Sekiranya otot pernafasan menjadi lemah, pengudaraan mekanikal mungkin diperlukan. Perencat asetilkolinesterase yang diintubasi dapat menahan sementara untuk mengurangkan rembesan saluran udara. [11]
MG mempengaruhi 50 hingga 200 setiap juta orang.[3][4] Ia baru didiagnosis pada tiga hingga 30 per juta orang setiap tahun.[12] Diagnosis menjadi lebih biasa kerana peningkatan kesedaran.[12] MG paling kerap berlaku pada wanita di bawah usia 40 tahun dan pada lelaki berusia lebih dari 60 tahun.[1][13][14] Ia tidak biasa pada kanak-kanak. Dengan rawatan, kebanyakan mereka yang terkena menjalani kehidupan yang agak normal dan mempunyai jangka hayat yang normal. Perkataan itu adalah dari Greek mys, "otot" dan astheneia "kelemahan", dan Latin gravis, "serius".[15]
Tanda dan gejala[sunting | sunting sumber]
Gejala awal, utama dalam MG adalah kelemahan otot tertentu yang tidak menyakitkan, bukan keletihan.[16] Kelemahan otot menjadi semakin teruk dalam tempoh aktiviti fizikal dan bertambah baik setelah berehat. Biasanya, kelemahan dan keletihan semakin teruk menjelang akhir hari.[17] MG biasanya bermula dengan kelemahan okular (mata); ia mungkin akan berkembang menjadi bentuk umum yang lebih teruk, yang dicirikan oleh kelemahan pada bahagian kaki atau otot yang mengatur fungsi kehidupan asas.[18]
Mata[sunting | sunting sumber]
Pada kira-kira dua pertiga individu, gejala awal MG berkaitan dengan otot di sekitar mata.[16] Kelopak mata terkulai (ptosis mungkin berlaku kerana kelemahan m. levator palpebrae superioris)[19] dan penglihatan berganda (diplopia, kerana kelemahan otot luar okulus).[17] Gejala mata cenderung bertambah buruk ketika menonton televisyen, membaca, atau memandu, terutama dalam keadaan terang. Akibatnya, sebilangan individu yang terkena memilih untuk memakai cermin mata hitam. Istilah "miastenia gravis okular" menerangkan subjenis MG apabila kelemahan otot terbatas pada mata, iaitu otot ekstraokular, m. levator palpebrae superioris, dan m. orbicularis oculi. Biasanya, subjenis ini berkembang menjadi MG umum, biasanya selepas beberapa tahun.
Makan[sunting | sunting sumber]
Kelemahan otot yang terlibat dalam menelan boleh menyebabkan kesukaran menelan (disfagia). Biasanya, ini bermaksud bahawa beberapa makanan mungkin tertinggal di mulut setelah percubaan untuk menelan,[20] atau makanan dan cecair boleh masuk semula ke dalam hidung daripada turun ke kerongkong (kekurangan velofarinks).[17] Kelemahan otot yang menggerakkan rahang (otot pengunyahan) boleh menyebabkan kesukaran untuk mengunyah. Pada individu dengan MG, mengunyah cenderung menjadi lebih melelahkan ketika mengunyah makanan yang berserat dan liat.[16] Kesukaran menelan, mengunyah, dan bercakap adalah gejala pertama pada sekitar seperenam individu.
Bercakap[sunting | sunting sumber]
Kelemahan otot yang terlibat dalam pengucapan boleh membawa kepada disartria dan hipofonia.[16] Pertuturan mungkin lambat dan tidak jelas,[21] atau mempunyai hipernasal.[17] Dalam beberapa kes, hobi atau pekerjaan menyanyi mesti ditinggalkan. [20]
Kepala dan leher[sunting | sunting sumber]
Oleh kerana kelemahan otot-otot muka dan otot-otot penguyahan, kelemahan wajah mungkin muncul sebagai ketidakmampuan menutup mulut[16] ("tanda rahang tergantung") dan sebagai ekspresi geram (snarling) ketika cuba tersenyum.[17] Dengan kelopak mata yang terkulai, kelemahan wajah dapat menyebabkan individu itu kelihatan mengantuk atau sedih. Kesukaran memastikan kepala dalam keadaan tegak mungkin berlaku.[21]
Lain-lain[sunting | sunting sumber]
Otot yang mengawal pernafasan dan pergerakan anggota badan juga boleh terjejas; jarang berlaku sebagai gejala pertama MG, tetapi berkembang dari bulan ke tahun.[22] Dalam krisis miastenik, kelumpuhan otot pernafasan berlaku, memerlukan pengudaraan berbantu untuk mengekalkan kehidupan.[23] Krisis mungkin dipicu oleh pelbagai tekanan biologi seperti jangkitan, demam, reaksi teruk terhadap ubat-ubatan, atau tekanan emosi.
Patofisiologi[sunting | sunting sumber]
MG adalah sinaptopati autoimun. Gangguan ini berlaku apabila sistem imun tubuh malfungsi dan menghasilkan antibodi yang menyerang tisu badan. Antibodi dalam MG menyerang protein manusia normal, reseptor asetilkolin nikotinik, atau protein yang berkaitan yang disebut MuSK, sejenis kinase khusus untuk otot.[24][25] Selain itu, kurang antibodi yang menyerang protein LRP4, agrin, dan titin.[26][27]
Haplotip antigen leukosit manusia dikaitkan dengan peningkatan kerentanan terhadap miastenia gravis dan gangguan autoimun yang lain. Mereka yang mempunyai pertalian dengan orang yang menghidap MG mempunyai peratusan gangguan imun yang lain yang lebih tinggi.[28][29]
Sel kelenjar timus membentuk sebahagian daripada sistem imun badan. Pada mereka yang mempunyai miastenia gravis, saiz kelenjar timus besar dari kebiasaan dan tidak normal. Kadang kala mengandungi sekumpulan sel imun yang menunjukkan hiperplasia limfoid, dan kelenjar timus mungkin memberikan arahan yang salah kepada sel imun.[30]
-
Persimpangan neuromuskular: 1. Axon 2. Membran sel otot 3. Vesikel sinaptik 4. Reseptor asetilkolin Nikotinik 5. Mitokondria
-
Timus remaja menyusut seiring bertambahnya usia.
Semasa mengandung[sunting | sunting sumber]
Bagi wanita yang hamil dan sudah mempunyai MG, pada sepertiga kes, mereka diketahui mengalami peningkatan gejala mereka, dan dalam kes tersebut, biasanya terjadi pada trimester pertama kehamilan.[31] Tanda dan gejala pada ibu mengandung cenderung bertambah baik pada trimester kedua dan ketiga. Pengurangan sepenuhnya boleh berlaku pada sebilangan ibu.[32] Terapi imunosupresif harus dijaga sepanjang kehamilan, kerana ini mengurangkan kemungkinan kelemahan otot neonatal, dan mengawal miastenia ibu.[33]
Kira-kira 10-20% bayi dengan ibu yang terjejas oleh keadaan dilahirkan dengan miastenia neonatal sementara (TNM), yang secara amnya menghasilkan kesukaran makan dan pernafasan yang berkembang sekitar 12 jam hingga beberapa hari selepas kelahiran.[31][33] Seorang kanak-kanak dengan TNM biasanya bertindak balas dengan baik terhadap perencat asetilkolinesterase, dan keadaannya biasanya sembuh dalam jangka masa tiga minggu, kerana antibodi berkurang, dan umumnya tidak mengakibatkan komplikasi. Jarang sekali, bayi boleh dilahirkan dengan artrogriposis multipleks kongenita, yang disebabkan oleh kelemahan intrauterin yang parah. Ini disebabkan oleh antibodi ibu yang mensasarkan reseptor asetilkolin bayi. Dalam beberapa kes, ibu tetap tidak asimptomatik.
Diagnosis[sunting | sunting sumber]
MG sukar didiagnosis, kerana gejalanya sukar dibezakan dari kedua-dua varian normal dan gangguan neurologi lain.[20]
Tiga jenis gejala miastenia pada kanak-kanak: [34]
- Miastenia neonatal zat alihan (transient) berlaku pada 10 hingga 15% bayi yang dilahirkan oleh ibu yang menderita gangguan tersebut, dan hilang setelah beberapa minggu.
- Miastenia kongenital, bentuk yang paling jarang berlaku, berlaku apabila gen wujud dari kedua ibu bapa.
- Miastenia gravis juvenil paling kerap berlaku pada wanita.
Miastenia kongenital menyebabkan kelemahan otot dan keletihan yang serupa dengan MG.[35] Tanda-tanda miastenia kongenital biasanya muncul pada tahun-tahun pertama masa kanak-kanak, walaupun mungkin tidak dikesan sehingga dewasa.[36]
Pengelasan[sunting | sunting sumber]
| Kelas | Penerangan |
|---|---|
| I | Mana-mana kelemahan otot mata, kemungkinan ptosis, tidak ada bukti kelemahan otot lain di tempat lain |
| II | Kelemahan otot mata dari mana-mana keparahan, kelemahan ringan otot lain |
| IIa | Sebilangan besar otot anggota badan atau aksial |
| IIb | Sebilangan besar otot bulbar dan/atau pernafasan |
| III | Kelemahan otot mata apa-apa keparahan, kelemahan otot lain yang sederhana |
| IIIa | Sebilangan besar otot anggota badan atau aksial |
| IIIb | Sebilangan besar otot bulbar dan/atau pernafasan |
| IV | Kelemahan otot mata dari mana-mana keparahan, kelemahan otot lain yang teruk |
| IVa | Sebilangan besar otot anggota badan atau aksial |
| IVb | Sebilangan besar otot bulbar dan/atau pernafasan |
| V | Intubasi diperlukan untuk mengekalkan saluran udara |
Apabila didiagnosis menghidap MG, seseorang dinilai status neurologinya dan tahap penyakitnya ditetapkan. Ini biasanya dilakukan dengan menggunakan skala Pengelasan Klinikal MIastenia Gravis Yayasan Amerika yang diterima.[perlu rujukan]
Pemeriksaan fizikal[sunting | sunting sumber]
Semasa pemeriksaan fizikal untuk memeriksa MG, doktor mungkin meminta individu itu melakukan pergerakan berulang. Sebagai contoh, doktor boleh meminta seseorang untuk melihat titik tetap selama 30 saat dan merehatkan otot-otot dahi, kerana seseorang dengan MG dan ptosis mata mungkin secara tidak sengaja menggunakan otot dahi untuk mengimbangi kelemahan pada kelopak mata.[20] Pemeriksa klinikal juga mungkin berusaha untuk mendapatkan "tanda tirai" pada seseorang dengan menahan salah satu mata orang itu terbuka, yang dalam hal MG akan menyebabkan mata yang lain ditutup.
Ujian darah[sunting | sunting sumber]
Sekiranya diagnosis disyaki, serologi dapat dilakukan:
- Satu ujian adalah untuk antibodi terhadap reseptor asetilkolin;[20] ujian mempunyai kepekaan yang wajar 80-96%, tetapi pada myasthenia okular, sensitiviti jatuh ke 50%.
- Sebilangan orang yang tidak mempunyai antibodi terhadap reseptor asetilkolin mempunyai antibodi terhadap protein MuSK.[38]
- Dalam situasi tertentu, ujian dilakukan untuk sindrom Lambert-Eaton.
Elektrodiagnostik[sunting | sunting sumber]


Gentian otot pada individu dengan MG adalah mudah letih, yang dapat didiagnos melalui ujian rangsangan saraf berulang. Dalam elektromiografi gentian tunggal, yang dianggap sebagai ujian yang paling sensitif (walaupun bukan yang paling spesifik) untuk MG,[20] elektrod jarum nipis dimasukkan ke kawasan yang berlainan otot tertentu untuk merakam potensi tindakan dari beberapa persampelan gentian otot individu yang berbeza. Dua gentian otot yang tergolong dalam unit motor yang sama dikenal pasti, dan kebolehubahan temporal dalam corak cetusan diukur. Kekerapan dan perkadaran corak potensi tindakan tidak normal tertentu, yang disebut "jitter" dan "blocking", adalah diagnostik. Jitter merujuk kepada variasi yang tidak normal dalam selang waktu antara potensi tindakan gentian otot bersebelahan dalam unit motor yang sama. "Blocking" merujuk kepada kegagalan impuls saraf untuk mendapatkan potensi tindakan pada gentian otot bersebelahan dari unit motor yang sama.[39]
Ujian ais[sunting | sunting sumber]
Meletakkan ais selama 2–5 minit ke otot dilaporkan mempunyai kepekaan dan kekhususan masing-masing 76.9% dan 98.3%, untuk mengenal pasti MG. Asetilkolinesterase dianggap dapat direncat pada suhu yang lebih rendah, yang menjadi asas untuk ujian diagnostik ini. Ini secara amnya dilakukan pada kelopak mata ketika terdapat ptosis dan dianggap positif jika kenaikan kelopak mata ≥2 mm berlaku setelah ais dikeluarkan.[40]
Ujian Edrofonium[sunting | sunting sumber]
Ujian ini memerlukan pemberian edrofonium klorida atau neostigmine secara intravena, ubat-ubatan yang menyekat pemecahan asetilkolin oleh kolinesterase (perencat asetilkolinesterase).[41] Ujian ini tidak lagi biasanya dilakukan, kerana penggunaannya dapat menyebabkan bradikardia (degupan jantung perlahan) yang mengancam nyawa yang memerlukan perhatian kecemasan segera.[42] Pengeluaran edrofonium dihentikan pada tahun 2008.[23]
Pengimejan[sunting | sunting sumber]
X-ray dada boleh mengenal pasti pelebaran mediastinum yang menunjukkan timoma, tetapi tomografi berkomputer atau pencitraan resonans magnetik (MRI) adalah cara yang lebih sensitif untuk mengenal pasti timoma dan secara amnya dilakukan untuk alasan ini.[43] MRI tengkorak dan orbit juga dapat dilakukan untuk mengecualikan luka mampatan dan keradangan pada saraf kranial dan otot mata.[44]
Ujian fungsi peparu[sunting | sunting sumber]
Kapasiti vital paksa dapat dipantau pada selang waktu untuk mengesan peningkatan kelemahan otot. Secara amnya, daya inspirasi negatif dapat digunakan untuk menentukan kecukupan pengudaraan; ia dilakukan pada individu yang mempunyai MG.
Pengurusan[sunting | sunting sumber]
Rawatan adalah dengan ubat dan/atau pembedahan. Ubat terutamanya terdiri daripada perencat asetilkolinesterase untuk secara langsung meningkatkan fungsi otot dan ubat imunosupresan untuk mengurangkan proses autoimun.[45][46] Timektomi adalah kaedah pembedahan untuk merawat MG.[47]
Ubat[sunting | sunting sumber]
Kemerosotan boleh berlaku dengan ubat seperti fluorokuinolon, aminoglikosida, dan magnesium.[48] Kira-kira 10% orang dengan MG umum dianggap sebagai rawatan-refraktori.[49] Transplantasi sel tunjang hematopoietik autologus (HSCT) kadang-kadang digunakan dalam MG yang teruk dan sukar ditangani. Data yang ada memberikan bukti awal bahawa HSCT dapat menjadi pilihan terapi yang berkesan dalam kes yang dipilih dengan teliti.[50]
Perencat asetilkolinesterase[sunting | sunting sumber]
Perencat asetilkolinesterase dapat memberikan faedah simptomatik dan mungkin tidak dapat sepenuhnya menghilangkan kelemahan seseorang dari MG.[51] Walaupun mereka mungkin tidak sepenuhnya menghapus semua gejala MG, mereka masih boleh membiarkan seseorang melakukan aktiviti harian yang normal. Biasanya, perencat asetilkolinesterase dimulakan pada dos yang rendah dan meningkat sehingga hasil yang diinginkan dicapai. Sekiranya diambil 30 minit sebelum makan, gejala akan menjadi ringan semasa makan, yang sangat membantu bagi mereka yang mengalami kesukaran menelan kerana sakit. Ubat lain yang digunakan untuk MG, atropin, dapat mengurangkan kesan sampingan muskarinik perencat asetilkolinesterase.[52] Pyridostigmine adalah ubat yang bertindak lama (jika dibandingkan dengan agonis kolinergik lain), dengan jangka hayat sekitar empat jam dengan sedikit kesan sampingan.[53] Umumnya, ia dihentikan pada mereka yang berventilasi secara mekanikal, kerana diketahui dapat meningkatkan jumlah rembesan air liur. Beberapa kajian berkualiti tinggi secara langsung membandingkan perencat kolinesterase dengan rawatan lain (atau plasebo); faedah praktikal mereka adalah sedemikian rupa sehingga membuat kajian di mana mereka akan ditahan dari beberapa orang menjadi sukar.[54]
Supresan imun[sunting | sunting sumber]
Predison steroid juga boleh digunakan untuk mencapai hasil yang lebih baik, tetapi boleh menyebabkan gejala memburuk dan memerlukan masa beberapa minggu untuk mencapai keberkesanan maksimumnya.[53] Research suggests that up to 15% of patients do not positively respond to immune suppressants.[55][56][57] Oleh kerana pelbagai gejala yang boleh menyebabkan rawatan steroid, ini bukan kaedah rawatan yang disukai. Ubat supresan imun lain juga boleh digunakan termasuk rituximab[58] atau azatioprina.[1]
Plasmaferesis dan IVIG[sunting | sunting sumber]
Sekiranya miastenia serius (krisis miastenik), plasmaferesis boleh digunakan untuk menghilangkan kemungkinan antibodi dari peredaran darah. Juga, imunoglobulin intravena (IVIG) boleh digunakan untuk mengikat antibodi yang beredar. Kedua-dua rawatan ini mempunyai manfaat jangka pendek, biasanya diukur dalam beberapa minggu, dan sering dikaitkan dengan kos yang tinggi, yang menjadikannya larangan; ia biasanya disediakan untuk individu dengan MG yang memerlukan kemasukan ke hospital.[53][59]
Pembedahan[sunting | sunting sumber]
Oleh kerana timoma dilihat pada 10% daripada semua orang dengan MG, mereka sering diberikan sinar-X dada dan imbasan CT untuk menilai keperluan mereka untuk pembedahan membuang kelenjar timus mereka dan sebarang tisu barah yang mungkin ada.[23][42] Walaupun pembedahan dilakukan untuk membuang timoma, secara amnya tidak membawa kepada pengurangan MG.[53] Pembedahan dalam kes MG melibatkan penyingkiran timus, walaupun pada tahun 2013, tidak ada manfaat yang jelas ditunjukkan kecuali jika terdapat timoma.[60] Walau bagaimanapun, percubaan terkawal dan rawak 2016 menemui beberapa faedah.[61]
Langkah-langkah fizikal[sunting | sunting sumber]
Orang dengan MG harus dididik mengenai sifat gejala mereka yang berubah-ubah, termasuk kelemahan dan keletihan yang disebabkan oleh senaman. Penyertaan dalam senaman harus digalakkan dengan rehat yang kerap[18] Pada individu dengan MG umum, beberapa bukti menunjukkan program rumah separa termasuk latihan dalam pernafasan diafragmatik, pernafasan penjerutan bibir, dan terapi otot berdasarkan selang dapat meningkatkan kekuatan otot pernafasan, mobiliti dinding dada, corak pernafasan, dan daya tahan pernafasan. [62]
Pengimejan perubatan[sunting | sunting sumber]
Pada orang dengan miastenia gravis, bentuk kontras beriodin lebih tua yang digunakan untuk pencitraan perubatan telah menyebabkan peningkatan risiko penyakit ini, tetapi bentuk moden tidak mempunyai risiko peningkatan yang segera.[63]
Prognosis[sunting | sunting sumber]
Prognosis individu dengan MG pada umumnya baik, begitu juga dengan kualiti hidup, apabila diberi rawatan yang sangat baik.[64] Pemantauan seseorang dengan MG sangat penting, kerana sekurang-kurangnya 20% orang yang didiagnosis dengannya akan mengalami krisis miastenik dalam masa dua tahun dari diagnosis mereka, memerlukan intervensi perubatan yang cepat.[53] Secara amnya, tempoh MG yang paling melumpuhkan mungkin bertahun-tahun setelah diagnosis awal.[51] Pada awal tahun 1900-an, 70% kes yang dikesan mati akibat masalah paru-paru; sekarang, jumlah itu diperkirakan sekitar 3–5%, yang disebabkan oleh peningkatan kesedaran dan ubat-ubatan untuk mengatasi gejala.
Epidemiologi[sunting | sunting sumber]
MG berlaku pada semua kumpulan etnik dan kedua-dua jantina. Ia paling sering menyerang wanita berusia di bawah 40 tahun dan individu dari 50 hingga 70 tahun dari kedua-dua jantina, tetapi ia diketahui berlaku pada usia apa pun. Orang muda jarang menghidap timoma. Prevalens di Amerika Syarikat dianggarkan antara 0.5 dan 20.4 kes per 100,000, dengan anggaran 60.000 orang Amerika terjejas.[23][65] Di United Kingdom, kira-kira 15 kes MG berlaku bagi setiap 100,000 orang.[42]
Sejarah[sunting | sunting sumber]
Yang pertama menulis mengenai MG adalah Thomas Willis, Samuel Wilks, Erb, dan Goldflam.[19] Istilah "myasthenia gravis pseudo-paralytica" dicadangkan pada tahun 1895 oleh Jolly, seorang doktor Jerman. Mary Walker merawat seseorang dengan MG dengan physostigmine pada tahun 1934. Simpson dan Nastuck memperincikan sifat autoimun dari keadaan ini. Pada tahun 1973, Patrick dan Lindstrom menggunakan arnab untuk menunjukkan bahawa imunisasi dengan reseptor asetilkolin seperti otot yang tertulen menyebabkan perkembangan gejala seperti MG.
Penyelidikan[sunting | sunting sumber]
Bahan imunomodulasi, seperti ubat-ubatan yang mencegah modulasi reseptor asetilkolin oleh sistem imun, sedang diteliti.[66] Beberapa kajian baru-baru ini mengenai perencat anti-c5 untuk penyelidikan rawatan kerana ia selamat dan digunakan dalam rawatan penyakit lain.[67] Efedrina nampaknya memberi manfaat kepada beberapa orang berbanding ubat-ubatan lain, tetapi belum dipelajari dengan betul pada tahun 2014.[10][68] Di makmal, MG kebanyakannya dikaji dalam model organisma, seperti tikus. Di samping itu, pada tahun 2015, saintis mengembangkan ujian simpang neuromuskular in-vitro yang berfungsi untuk semua manusia dari sel tunjang embrio manusia dan sel tunjang otot somatik. Selepas penambahan antibodi patogen terhadap reseptor asetilkolin dan pengaktifan sistem pelengkap, kultur neuromuskular menunjukkan gejala seperti kontraksi otot yang lebih lemah.[69]
Rujukan[sunting | sunting sumber]
- ^ a b c d e f g h i j k l m "Myasthenia Gravis Fact Sheet". NINDS. 10 May 2016. Diarkibkan daripada yang asal pada 27 July 2016. Dicapai pada 8 August 2016.
- ^ Kahan, Scott (2005). In a Page: Neurology (dalam bahasa Inggeris). Lippincott Williams & Wilkins. m/s. 118. ISBN 978-1-4051-0432-6. Diarkibkan daripada yang asal pada 8 September 2017.
- ^ a b Kaminski, Henry J. (2009). Myasthenia Gravis and Related Disorders (dalam bahasa Inggeris) (ed. 2). Springer Science & Business Media. m/s. 72. ISBN 978-1-59745-156-7. Diarkibkan daripada yang asal pada 8 September 2017.
- ^ a b Adams, James G. (2012). Emergency Medicine: Clinical Essentials (dalam bahasa Inggeris) (ed. 2). Elsevier Health Sciences. m/s. 844. ISBN 978-1-4557-3394-1. Diarkibkan daripada yang asal pada 8 September 2017.
- ^ Salari N, Fatahi B, Bartina Y, Kazeminia M, Fatahian R, Mohammadi P, dll. (December 2021). "Global prevalence of myasthenia gravis and the effectiveness of common drugs in its treatment: a systematic review and meta-analysis". Journal of Translational Medicine. 19 (1): 516. doi:10.1186/s12967-021-03185-7. PMC 8686543 Check
|pmc=value (bantuan). PMID 34930325 Check|pmid=value (bantuan). - ^ Young C, McGill SC (April 2021). Rituximab for the Treatment of Myasthenia Gravis: A 2021 Update [Internet] (Laporan). Ottawa (ON): Canadian Agency for Drugs and Technologies in Health. PMID 34255447.
- ^ Dabi A, Solieman N, Kurukumbi M, Kalyanam J (2012). "Myasthenia Gravis: A Review". Autoimmune Diseases. 2012: 1–10. doi:10.1155/2012/874680. PMC 3501798. PMID 23193443.
- ^ "Pathogenesis of myasthenia gravis: update on disease types, models, and mechanisms". F1000Research. 5: 1513. 2016-01-01. doi:10.12688/f1000research.8206.1. PMC 4926737. PMID 27408701.
- ^ Kandel E, Schwartz J, Jessel T, Siegelbaum S, Hudspeth A (2012). Principles of Neural Science (ed. 5). m/s. 318–319.CS1 maint: uses authors parameter (link)
- ^ a b "Ephedrine for myasthenia gravis, neonatal myasthenia and the congenital myasthenic syndromes". The Cochrane Database of Systematic Reviews. 12 (12): CD010028. December 2014. doi:10.1002/14651858.CD010028.pub2. PMC 7387729. PMID 25515947.
- ^ Godoy, DA; Mello, LJ; Masotti, L; Di Napoli, M (September 2013). "The myasthenic patient in crisis: an update of the management in Neurointensive Care Unit". Arquivos de Neuro-psiquiatria. 71 (9A): 627–39. doi:10.1590/0004-282X20130108. PMID 24141444.
- ^ a b McGrogan A, Sneddon S, de Vries CS (2010). "The incidence of myasthenia gravis: a systematic literature review". Neuroepidemiology. 34 (3): 171–183. doi:10.1159/000279334. PMID 20130418. S2CID 34447321.
- ^ Salari N, Fatahi B, Bartina Y, Kazeminia M, Fatahian R, Mohammadi P, dll. (December 2021). "Global prevalence of myasthenia gravis and the effectiveness of common drugs in its treatment: a systematic review and meta-analysis". Journal of Translational Medicine. 19 (1): 516. doi:10.1186/s12967-021-03185-7. PMC 8686543 Check
|pmc=value (bantuan). PMID 34930325 Check|pmid=value (bantuan). - ^ Conti-Fine BM, Milani M, Kaminski HJ (November 2006). "Myasthenia gravis: past, present, and future". The Journal of Clinical Investigation. 116 (11): 2843–2854. doi:10.1172/JCI29894. PMC 1626141. PMID 17080188.
- ^ Ehrlich, Ann; Schroeder, Carol L. (2014). Introduction to Medical Terminology (dalam bahasa Inggeris). Cengage Learning. m/s. 87. ISBN 978-1-133-95174-2. Diarkibkan daripada yang asal pada 8 September 2017.
- ^ a b c d e Engel AG (2012). Myasthenia Gravis and Myasthenic Disorders (ed. 2nd). Oxford University Press, US. m/s. 109–110. ISBN 978-0-19-973867-0. Diarkibkan daripada yang asal pada 8 September 2017.
- ^ a b c d e Scully C (2014). Scully's Medical Problems in Dentistry. Elsevier Health Sciences UK. ISBN 978-0-7020-5963-6. Diarkibkan daripada yang asal pada 8 September 2017.
- ^ a b "Myasthenia Gravis: Practice Essentials, Background, Anatomy". 2015-06-06. Diarkibkan daripada yang asal pada 23 June 2015. Cite journal requires
|journal=(bantuan) - ^ a b "Ocular myasthenia gravis: a review". Indian Journal of Ophthalmology. 62 (10): 985–991. October 2014. doi:10.4103/0301-4738.145987. PMC 4278125. PMID 25449931.
- ^ a b c d e f "Does this patient have myasthenia gravis?". JAMA. 293 (15): 1906–1914. April 2005. doi:10.1001/jama.293.15.1906. PMID 15840866.
- ^ a b Rajendran A; Sundaram S (2014). Shafer's Textbook of Oral Pathology (ed. 7th). Elsevier Health Sciences APAC. m/s. 867. ISBN 978-81-312-3800-4. Diarkibkan daripada yang asal pada 2 April 2017.
- ^ MedlinePlus Encyclopedia Myasthenia gravis
- ^ a b c d Marx, John A. Marx (2014). Rosen's emergency medicine : concepts and clinical practice (ed. 8th). Philadelphia: Elsevier/Saunders. m/s. 1441–1444. ISBN 978-1-4557-0605-1.
- ^ Valenzuela DM, Stitt TN, DiStefano PS, Rojas E, Mattsson K, Compton DL, Nunez L, Park JS, Stark JL, Gies DR, Thomas S, LeBeau MM, Fernald AA, Copeland NG, Jenkins NA, Burden SJ, Glass DJ, Yancopoulos GD (Sep 1995). "Receptor tyrosine kinase specific for the skeletal muscle lineage: expression in embryonic muscle, at the neuromuscular junction, and after injury". Neuron. 15 (3): 573–584. doi:10.1016/0896-6273(95)90146-9. PMID 7546737. S2CID 17575761.
- ^ "Myasthenia gravis". Genetics Home Reference. Diarkibkan daripada yang asal pada 11 July 2015. Dicapai pada 2015-07-10.
- ^ "Pathogenesis of myasthenia gravis: update on disease types, models, and mechanisms". F1000Research. 5: 1513. 2016-01-01. doi:10.12688/f1000research.8206.1. PMC 4926737. PMID 27408701.
- ^ "Mapping autoantigen epitopes: molecular insights into autoantibody-associated disorders of the nervous system". Journal of Neuroinflammation. 13 (1): 219. August 2016. doi:10.1186/s12974-016-0678-4. PMC 5006540. PMID 27577085.
- ^ Sathasivam, Sivakumar (January 2014). "Diagnosis and management of myasthenia gravis". Progress in Neurology and Psychiatry. 18 (1): 6–14. doi:10.1002/pnp.315.
- ^ "Myasthenia Gravis". PubMed Health. Bethesda, MD: U.S. National Library of Medicine. Diarkibkan daripada yang asal pada 18 October 2016. Dicapai pada 2015-07-09.
- ^ "Myasthenia Gravis Fact Sheet". www.ninds.nih.gov. National Institute of Neurological Disorders and Stroke (NINDS). Diarkibkan daripada yang asal pada 11 July 2015. Dicapai pada 2015-07-10.
- ^ a b "Myasthenia gravis and pregnancy". Clinical Obstetrics and Gynecology. 56 (2): 372–381. June 2013. doi:10.1097/GRF.0b013e31828e92c0. PMID 23563874.
- ^ Téllez-Zenteno, José F; Hernández-Ronquillo, Lizbeth; Salinas, Vicente; Estanol, Bruno; da Silva, Orlando (16 November 2004). "Myasthenia gravis and pregnancy: clinical implications and neonatal outcome". BMC Musculoskeletal Disorders. 5 (1): 42. doi:10.1186/1471-2474-5-42. PMC 534111. PMID 15546494.
- ^ a b Warrell, David A; Cox, Timothy M; dll. (2003). Oxford Textbook of Medicine. Volume 3 (ed. Fourth). Oxford. m/s. 1170. ISBN 978-0-19-852787-9.
|volume=has extra text (bantuan) - ^ Rudd, Kathryn; Kocisko, Diane (2013). Pediatric Nursing: The Critical Components of Nursing Care. F.A. Davis. ISBN 978-0-8036-4053-5. Diarkibkan daripada yang asal pada 3 June 2016.
- ^ "Congenital myasthenic syndromes: pathogenesis, diagnosis, and treatment". The Lancet. Neurology. 14 (4): 420–434. April 2015. doi:10.1016/S1474-4422(14)70201-7. PMC 4520251. PMID 25792100.
- ^ "Congenital Myasthenia Information Page: National Institute of Neurological Disorders and Stroke (NINDS)". www.ninds.nih.gov. Diarkibkan daripada yang asal pada 12 July 2015. Dicapai pada 2015-07-11.
- ^ Wolfe, Gil I.; Barohn, Richard J. (2009). "Myasthenia Gravis: Classification and Outcome Measurements". Myasthenia Gravis and Related Disorders. m/s. 293–302. doi:10.1007/978-1-59745-156-7_18. ISBN 978-1-58829-852-2.
- ^ Leite, Maria Isabel; Jacob, Saiju; Viegas, Stuart; Cossins, Judy; Clover, Linda; Morgan, B. Paul; Beeson, David; Willcox, Nick; Vincent, Angela (July 2008). "IgG1 antibodies to acetylcholine receptors in 'seronegative' myasthenia gravis". Brain. 131 (7): 1940–1952. doi:10.1093/brain/awn092. PMC 2442426. PMID 18515870.
- ^ "Single-fiber EMG: A review". Annals of Indian Academy of Neurology. 14 (1): 64–67. January 2011. doi:10.4103/0972-2327.78058. PMC 3108086. PMID 21654930.
- ^ Kearsey, Christopher; Fernando, Prabhath; D'costa, Domnick; Ferdinand, Phillip (30 June 2010). "The Use of the Ice Pack Test in Myasthenia Gravis". JRSM Short Reports. 1 (1): 14. doi:10.1258/shorts.2009.090037. PMC 2984327. PMID 21103106.
- ^ MedlinePlus Encyclopedia Tensilon test
- ^ a b c Spillane, J.; Higham, E.; Kullmann, D. M. (21 December 2012). "Myasthenia gravis". BMJ. 345 (dec21 3): e8497. doi:10.1136/bmj.e8497. PMID 23261848.
- ^ "CT and myasthenia gravis: correlation between mediastinal imaging and histopathological findings". Interactive Cardiovascular and Thoracic Surgery. 4 (3): 267–271. June 2005. doi:10.1510/icvts.2004.097246. PMID 17670406.
- ^ Allan H. Ropper, Robert H. Brown Adams and Victor's Principles of Neurology McGraw-Hill Professional; 8 edition (2005)
- ^ Salari N, Fatahi B, Bartina Y, Kazeminia M, Fatahian R, Mohammadi P, dll. (December 2021). "Global prevalence of myasthenia gravis and the effectiveness of common drugs in its treatment: a systematic review and meta-analysis". Journal of Translational Medicine. 19 (1): 516. doi:10.1186/s12967-021-03185-7. PMC 8686543 Check
|pmc=value (bantuan). PMID 34930325 Check|pmid=value (bantuan). - ^ Mehndiratta MM, Pandey S, Kuntzer T (October 2014). "Acetylcholinesterase inhibitor treatment for myasthenia gravis". The Cochrane Database of Systematic Reviews. 2014 (10): CD006986. doi:10.1002/14651858.CD006986.pub3. PMC 7390275. PMID 25310725.
- ^ Gronseth, Gary S.; Barohn, Richard J. (12 July 2000). "Practice parameter: Thymectomy for autoimmune myasthenia gravis (an evidence-based review): Report of the Quality Standards Subcommittee of the American Academy of Neurology". Neurology. 55 (1): 7–15. doi:10.1212/wnl.55.1.7. PMID 10891896.
- ^ Mehrizi, Mehyar (August 2012). "Medications and Myasthenia Gravis (A Reference for Health Care Professionals)" (PDF). Myasthenia Gravis Foundation of America. Department of Neurology, Indiana University School of Medicine. Diarkibkan daripada yang asal (PDF) pada 2019-08-29. Dicapai pada 2021-02-05.
- ^ "[Clinical and neuropsychological symptoms of normal pressure hydrocephalus]". Nederlands Tijdschrift voor Geneeskunde. 131 (36): 1584–1585. September 1987. PMC 3670444. PMID 23766745.
- ^ Burman, Joachim; Tolf, Andreas; Hägglund, Hans; Askmark, Håkan (February 2018). "Autologous haematopoietic stem cell transplantation for neurological diseases". Journal of Neurology, Neurosurgery & Psychiatry. 89 (2): 147–155. doi:10.1136/jnnp-2017-316271. PMC 5800332. PMID 28866625.
- ^ a b "Acetylcholinesterase inhibitor treatment for myasthenia gravis". The Cochrane Database of Systematic Reviews (10): CD006986. October 2014. doi:10.1002/14651858.CD006986.pub3. PMC 7390275. PMID 25310725.
- ^ "Atropine – Myasthenia-gravis medicines and drugs". NHS Choices. 2014. Diarkibkan daripada yang asal pada 12 July 2015. Dicapai pada 2015-07-11.
- ^ a b c d e "Treatment of myasthenia gravis". Current Neurology and Neuroscience Reports. 11 (1): 89–96. February 2011. doi:10.1007/s11910-010-0151-1. PMID 20927659.
- ^ Mehndiratta, Man Mohan; Pandey, Sanjay; Kuntzer, Thierry (13 October 2014). "Acetylcholinesterase inhibitor treatment for myasthenia gravis". Cochrane Database of Systematic Reviews (10): CD006986. doi:10.1002/14651858.CD006986.pub3. PMC 7390275. PMID 25310725.
- ^ Drachman DB, Adams RN, Hu R, Jones RJ, Brodsky RA (2008-06-01). "Rebooting the immune system with high-dose cyclophosphamide for treatment of refractory myasthenia gravis". Annals of the New York Academy of Sciences. 1132 (1): 305–314. Bibcode:2008NYASA1132..305D. doi:10.1196/annals.1405.033. PMC 3390145. PMID 18567882.
- ^ Suh J, Goldstein JM, Nowak RJ (June 2013). "Clinical characteristics of refractory myasthenia gravis patients". The Yale Journal of Biology and Medicine. 86 (2): 255–260. PMC 3670444. PMID 23766745.
- ^ Salari N, Fatahi B, Bartina Y, Kazeminia M, Fatahian R, Mohammadi P, dll. (December 2021). "Global prevalence of myasthenia gravis and the effectiveness of common drugs in its treatment: a systematic review and meta-analysis". Journal of Translational Medicine. 19 (1): 516. doi:10.1186/s12967-021-03185-7. PMC 8686543 Check
|pmc=value (bantuan). PMID 34930325 Check|pmid=value (bantuan). - ^ "Rituximab treatment of myasthenia gravis: A systematic review". Muscle & Nerve. 56 (2): 185–196. August 2017. doi:10.1002/mus.25597. PMID 28164324.
- ^ "Myasthenia gravis: management of myasthenic crisis and perioperative care". Seminars in Neurology. 24 (1): 75–81. March 2004. doi:10.1055/s-2004-829595. PMID 15229794. S2CID 260320936 Check
|s2cid=value (bantuan). - ^ "Thymectomy for non-thymomatous myasthenia gravis". The Cochrane Database of Systematic Reviews (10): CD008111. October 2013. doi:10.1002/14651858.CD008111.pub2. PMID 24122674.
- ^ "Randomized Trial of Thymectomy in Myasthenia Gravis". The New England Journal of Medicine. 375 (6): 511–522. August 2016. doi:10.1056/NEJMoa1602489. PMC 5189669. PMID 27509100. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Exercise therapy and other types of physical therapy for patients with neuromuscular diseases: a systematic review". Archives of Physical Medicine and Rehabilitation. 88 (11): 1452–1464. November 2007. doi:10.1016/j.apmr.2007.07.024. PMID 17964887.
- ^ Mehrizi, Mehyar; Pascuzzi, Robert M. (September 2014). "Complications of radiologic contrast in patients with myasthenia gravis". Muscle & Nerve. 50 (3): 443–444. doi:10.1002/mus.24254. PMID 24677227.
- ^ "Myasthenia gravis: an update for the clinician". Clinical and Experimental Immunology. 175 (3): 408–418. March 2014. doi:10.1111/cei.12217. PMC 3927901. PMID 24117026.
- ^ "Thymectomy for non-thymomatous myasthenia gravis". The Cochrane Database of Systematic Reviews (10): CD008111. October 2013. doi:10.1002/14651858.CD008111.pub2. PMID 24122674.
- ^ "Treatment of myasthenia gravis by preventing acetylcholine receptor modulation". Annals of the New York Academy of Sciences. 1132 (1): 174–179. 2008. Bibcode:2008NYASA1132..174L. doi:10.1196/annals.1405.034. PMID 18567867.
- ^ "Myasthenia gravis: past, present, and future". The Journal of Clinical Investigation. 116 (11): 2843–2854. November 2006. doi:10.1172/JCI29894. PMC 1626141. PMID 17080188.
- ^ "Ephedrine for myasthenia gravis, neonatal myasthenia and the congenital myasthenic syndromes". The Cochrane Database of Systematic Reviews. 12 (12): CD010028. December 2014. doi:10.1002/14651858.CD010028.pub2. PMC 7387729. PMID 25515947.
- ^ "Functional Connectivity under Optogenetic Control Allows Modeling of Human Neuromuscular Disease". Cell Stem Cell. 18 (1): 134–143. January 2016. doi:10.1016/j.stem.2015.10.002. PMC 4707991. PMID 26549107.
Bacaan lanjut[sunting | sunting sumber]
- "Evaluation of the quality of guidelines for myasthenia gravis with the AGREE II instrument". PLOS ONE. 9 (11): e111796. 17 November 2014. Bibcode:2014PLoSO...9k1796Z. doi:10.1371/journal.pone.0111796. PMC 4234220. PMID 25402504.
- "Diagnostic: Myasthenia gravis". National Center for Biotechnology Information (NCBI). U.S. National Library of Medicine. Dicapai pada 2015-07-11.
Pautan luar[sunting | sunting sumber]
Templat:Penyakit simpang mioneural dan neurootot Templat:Penyakit autoimun