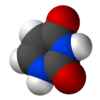
Urasil

| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
Pirimidina-2,4(1H,3H)-diona
| |||
| Pengecam | |||
Imej model 3D Jmol
|
|||
| 3DMet | |||
| 606623 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.565 | ||
| Nombor EC |
| ||
| 2896 | |||
| KEGG | |||
PubChem CID
|
|||
| Nombor RTECS |
| ||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| C4H4N2O2 | |||
| Jisim molar | 112.08676 g/mol | ||
| Rupa bentuk | Pepejal | ||
| Ketumpatan | 1.32 g/cm3 | ||
| Takat lebur | 335 °C (635 °F; 608 K)[1] | ||
| Takat didih | N/A – Terurai | ||
| Larut | |||
| Bahaya | |||
| Bahaya-bahaya utama | Karsinogen dan teratogen dalam pendedahan melampau | ||
| Piktogram GHS |  
| ||
| Perkataan isyarat GHS | Warning | ||
| H315, H319, H335, H361 | |||
| P201, P202, P261, P264, P271, P280, P281, P302+352, P304+340, P305+351+338, P308+313, P312, P321, P332+313, P337+313, P362, P403+233, P405, P501 | |||
| NFPA 704 (berlian api) | |||
| Takat kilat | Tidak mudah terbakar | ||
| Sebatian berkaitan | |||
Sebatian berkaitan
|
Timina Sitosina | ||
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |||
| | |||
| Rujukan kotak info | |||
Urasil (U) merupakan salah satu daripada bes nitrogen dalam asid nukleik RNA bersama adenina (A), guanina (G) dan sitosina (C). Dalam DNA, urasil digantikan dengan timina (T) yang merupakan sebatian dengan struktur sama tanpa metil. Urasil merupakan sebatian pirimidina yang biasa dan mudah dijumpai dalam alam sekitar.[2]
Sintesis[sunting | sunting sumber]
Pelbagai tindak balas boleh dilakukan di makmal untuk menghasilkan urasil. Salah satu daripadanya ialah tindak balas antara sitosina dan air untuk menghasilkan urasil dan ammonia sebagai bahan sampingan.[2]
Rujukan[sunting | sunting sumber]
- ^ Myers, Richard L.; Myers, Rusty L. (2007). The 100 Most Important Chemical Compounds. m/s. 92–93. ISBN 9780313337581.[petikan lengkap diperlukan]
- ^ a b Garrett, Reginald H.; Grisham, Charles M. (1997). Principals of Biochemistry with a Human Focus. United States: Brooks/Cole Thomson Learning.
Kategori:
- Rencana yang memerlukan rujukan lebih terperinci dari December 2018
- Rencana dengan pengecam EBI berubah
- Rencana dengan pengecam ChemSpider berubah
- ECHA InfoCard ID from Wikidata
- Articles with changed FDA identifier
- Rencana dengan pengecam InChI berubah
- Articles containing unverified chemical infoboxes
- Chembox image size set
- Pirimidina