Keton
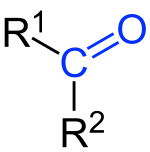
Keton merujuk kepada sama ada kelompok berfungsi yang dicirikan oleh kumpulan karbonil (O=C) yang terikat kepada dua atom karbon, atau sebatian kimia yang mengandungi kelompok berfungsi ini. Ia umumnya dapat dilambangkan melalui formula yang berikut:
Satu karbon karbonil yang terikat kepada dua atom karbon membezakan keton daripada asid karboksilik, aldehid, ester, amida, dan sebatian-sebatian lain yang mengandungi oksigen. Sebaliknya, ikatan ganda dua kumpulan karbonil membezakan keton daripada alkohol dan eter. Keton yang paling mudah ialah aseton yang juga dikenali sebagai propanon.
Atom karbon yang terletak di sebelah kumpulan karbonil dipanggil α-karbon, manakala atom-atom hidrogen yang terikat pada karbon ini dipanggil α-hidrogen. Dengan adanya mangkin asid, keton akan mengalami apa yang dipanggil ketautomeran keto-enol, manakala tindak balas dengan bes yang kuat menghasilkan enolat yang sepadan. Diketon ialah sebatian yang mengandungi dua kumpulan keton.
Tatanama
[sunting | sunting sumber]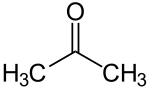
Keton umumnya dinamai dengan menggunakan tatanama IUPAC yang menukarkan akhiran -n menjadi -non untuk keluarga alkana. Bagi keton biasa, sesetengah nama tradisi seperti aseton dan benzofenon digunakan secara meluas, dan nama ini telahpun dikekalkan sebagai nama IUPAC, sungguhpun sesetengah buku teks kimia yang asas menggunakan nama-nama seperti 2-propanon atau propanon.
Ciri-ciri fizikal
[sunting | sunting sumber]Kumpulan karbonil adalah berkutub dan oleh itu, menyebabkan keton merupakan suatu sebatian berkutub. Kumpulan karbonil bertindak balas dengan air melalui pengikatan hidrogen, tetapi tidak berupaya mengikat kepada hidrogen pada dirinya. Ia adalah penerima ikatan hidrogen, bukannya penderma ikatan hidrogen. Ini menyebabkan keton lebih meruap, berbanding dengan alkohol dan asid karboksilik yang mempunyai berat molekul yang sama.
Ciri-ciri spektroskopi
[sunting | sunting sumber]Spektroskopi adalah penting untuk mengenalpasti keton. Keton dan aldehaid akan menunjukkan puncak dalam spekroskopi inframerah pada sekitar 1700 cm−1 (lebih kurang, bergantung kepada persekitaran kimia).
Sintesis
[sunting | sunting sumber]- Keton boleh dibentuk dengan pengoksidaan alkohol tahap kedua. Proses ini memerlukan agen pengoksida yang kuat seperti kalium dikromat atau agen lain yang mengandungi Cr(VI). Alkohol dioksidakan dengan pemanasan beserta refluks dalam larutan berasid. Sebagai contoh, propan-2-ol dioksidakan menjadi propanon (aseton):
- H3C-CH(OH)-CH3 → H3C-CO-CH3
- Dua atom hidrogen disingkirkan, meninggakam satu atom oksigen berikatan ganda dua dengan atom karbon.
- Keton juga boleh disediakan oleh hidrolisis batuan halida.
- Keton beraroma boleh disediakan dalam tindak balas Friedel-Crafts dan penyusunan semula Fries.
Penggunaan
[sunting | sunting sumber]Keton sering dugunakan dalam minyak wangi dan cat untuk menstabilkan bahan lain agar tidak terurai dengan cepat. Kegunaan lain adalah sebagai pelarut dan bahan perantaraan dalam industri kimia. Contoh keton adalah Asetofenon, Butanon (metil etil keton) dan Propanon (aseton).
Rujukan
[sunting | sunting sumber]Pautan luar
[sunting | sunting sumber] Kategori berkenaan Keton di Wikimedia Commons
Kategori berkenaan Keton di Wikimedia Commons
{{#switch:||Kategori=
