Alkana
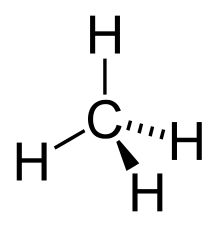
Alkana merupakan hidrokarbon alifatik dan hidrokarbon tepu. Formula am alkana ialah CnH2n+2 di mana n bersamaan 1,2,3, dan seterusnya; dan merupakan siri homolog hidrokarbon yang penting. Susunan elektron karbon ialah 2.4 atau 1s2 2s2 2p2 dan boleh menerima sehingga empat ikatan. Dalam alkana, setiap atom karbon terikat kepada empat atom lain dan ia tidak boleh menerima lagi atom hidrogen. Semua atom dalam satu-satu alkana membentuk ikatan tunggal sahaja iaitu ikatan σ (sigma). Ikatan ini terletak di antara satu atom karbon dengan atom karbon lain ataupun dengan atom hidrogen. Sudutnya pula ialah 109.5o.
Alkana adalah agak stabil terhadap tindak balas kimia, dan ia bersifat kurang reaktif kerana atom-atomnya terikat antara satu sama lain dengan kuat. Ia tidak bertindak balas dengan air bromin atau larutan kalium manganat (VII) berasid tetapi bertindakbalas dengan halogen dalam sinar ultraungu.
Ia menghasilkan sedikit jelaga apabila terbakar berbanding dengan alkena disebabkan oleh peratusan karbon dalam molekulnya yang lebih rendah.
Klasifikasi struktur[sunting | sunting sumber]
Hidrokarbon tepu dapat dikelaskan secara berikut:
- linear (formula umum CnH2n + 2) setiap atom karbon bergabung untuk dalam struktur seakan-akan bentuk ular
- bercabang (formula umum CnH2n + 2, n > 3) struktur utama karbon berpecah ke satu atau lebih arah
- sebatian kitaran (formula umum CnH2n, n > 2) struktur utama karbon bergabung untuk menghasilkan satu kitaran
Berdasarkan definisi IUPAC, hidrokarbon linear dan bercabang dikategorikan sebagai alkana, manakala sebatian kitaran diklasifikasikan sebagai sikloalkana.[1] Hidrokarbon tepu yang bergabung dengan struktur linear, kitaran dan bercabang tetap diklasifikasikan sebagai alkana asalkan strutur tersebut merupakan sebatian terbuka (asiklik), iaitu tanpa sebarang gelung. Setiap atom karbon mempunyai ikatan kovalen tunggal sesama diri.
Sistem penamaan alkana[sunting | sunting sumber]
Berikut adalah nama sepuluh ahli pertama alkana rantai lurus.
| Bilangan atom karbon per molekul | Nama IUPAC | Formula molekul |
|---|---|---|
| 1 | Metana | CH4 |
| 2 | Etana | C2H6 |
| 3 | Propana | C3H8 |
| 4 | Butana | C4H10 |
| 5 | Pentana | C5H12 |
| 6 | Heksana | C6H14 |
| 7 | Heptana | C7H16 |
| 8 | Oktana | C8H18 |
| 9 | Nonana | C9H20 |
| 10 | Dekana | C10H22 |
Sifat fizik[sunting | sunting sumber]
Sifat fizik alkana adalah seperti :
| Nama alkana | Takat lebur (°C) | Takat didih (°C) | Keadaan fizik pada suhu bilik | Ketumpatan pada suhu bilik (g cm-3) |
|---|---|---|---|---|
| Metana | -182 | -162 | Gas | 0.0007 |
| Etana | -183 | -89 | Gas | 0.0013 |
| Propana | -188 | -42 | Gas | 0.0018 |
| Butana | -138 | -0.5 | Gas | 0.0024 |
| Pentana | -130 | 36 | Cecair | 0.56 |
| Heksana | -95 | 69 | Cecair | 0.66 |
| Heptana | -90 | 98 | Cecair | 0.68 |
| Oktana | -57 | 126 | Cecair | 0.70 |
| Nonana | -54 | 153 | Cecair | 0.72 |
| Dekana | -30 | 174 | Cecair | 0.74 |
Keadaan fizik[sunting | sunting sumber]
Apabila menuruni siri alkana, sifat fiziknya berubah secara beransur-ansur. Pada suhu bilik, metana sehingga butana wujud sebagai gas manakala pentana sehingga heksadekana, C16H34 wujud sebagai cecair. Heptadekana, C17H36 dan seterusnya wujud sebagai pepejal berminyak.
Takat lebur dan takat didih[sunting | sunting sumber]
Alkana wujud sebagai molekul kovalen ringkas. Oleh itu, alkana mempunyai takat lebur dan takat didih yang rendah kerana molekul-molekulnya ditarik oleh daya van der Waals yang lemah jadi hanya sedikit haba yang diperlukan untuk memecahkan daya tarikan antara molekul ini supaya peleburan dan pendidihan dapat berlaku. Semasa perubahan keadaan fizik berlaku, tenaga yang sedikit sudah mencukupi untuk memutuskan daya ini.
Ketumpatan[sunting | sunting sumber]
Semua alkana mempunyai ketumpatan yang rendah disebabkan daya van der Waals antara molekul adalah lemah. Oleh sebab itu susunan molekul-molekulnya kurang padat. Ketumpatan alkana kurang berbanding ketumpatan air (997 kg m-3)
Apabila bilangan atom karbon per molekul bertambah , molekul alkana dengan saiz yang yang semakin bertambah dapat menarik antara satu sama lain dengan daya van der Waals antara molekul dengan lebih kuat. Oleh itu, molekul-molekulnya lebih besar dan tersusun dengan lebih padat lalu meningkatkan ketumpatannya.
Keterlarutan dalam air[sunting | sunting sumber]
Semua alkana tidak larut dalam air kerana alkana merupakan sebatian kovalen yang hanya larut dalam pelarut organik seperti eter dan benzena.
Kekonduksian elektrik[sunting | sunting sumber]
Semua alkana adalah sebatian kovalen yang terdiri daripada molekul ringkas yang tiada ion-ion bebas bergerak. Oleh itu, alkana tidak mengkonduksikan elektrik.
Sifat kimia[sunting | sunting sumber]
- Diikat dengan ikatan kovalen.
- Bertindak balas dengan halogen seperti gas klorin dan membentuk monokloroetana, dikloroetana, trikloroetana dan tetrakloroetana dalam kehadiran sinar ultraungu. Penukargantian telah berlaku.
- Menghasilkan karbon dioksida dan air apabila dibakar secara lengkap. Pembakaran yang tidak lengkap akan menghasilkan karbon dan karbon monoksida (melalui tindak balas pembakaran).
- Tindak balas yang dijalani oleh alkana biasanya melalui mekanisme radikal bebas.
- Boleh diprotonkan dengan asid super (super acids).
Tindak balas pembakaran[sunting | sunting sumber]
- Semua alkana terbakar dalam oksigen, O2 dan membebaskan haba.
Pembakaran lengkap[sunting | sunting sumber]
Dengan bekalan gas oksigen yang berlebihan, alkana terbakar dengan lengkap untuk menghasilkan gas karbon dioksida, CO2 dan wap air sahaja. Contohnya pembakaran metana,CH4 lengkap :
CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O (ce)
Pembakaran tidak lengkap[sunting | sunting sumber]
Dengan bekalan oksigen yang terhad, pembakaran alkana adalah tidak lengkap. Nyalaan adalah lebih berjelaga. Campuran karbon,C, gas karbon monoksida , CO, dan air, H2O, terhasil. Contoh pembakaran etana yang tidak lengkap:
C2H6 (g) + 2O2 (g) → C (p) + CO (g) + 3H2O (ce)
Semakin menuruni siri homolog alkana, nyalaan alkana semakin berjelaga dan pembakaran menjadi semakin sukar. Ini adalah kerana peratus kandungan karbon mengikut jisim dalam molekul semakin meningkat.
Tindak balas penukargantian[sunting | sunting sumber]
Tindak balas ini berlaku dalam kehadiran cahaya matahari atau sinaran ultraungu. Dalam tindak balas ini, atom-atom hidrogen dalam molekul alkana diganti dengan atom yang lain, seperti atom klorin atau bromin. Tindak balas penukargantian metana dengan klorin dapat ditulis seperti di bawah:
CH4 + Cl2 → CH3Cl(monoklorometana) + HCl
atau
CH4 + 2Cl2 → CH2Cl2(diklorometana) + 2HCl
atau
CH4 + 3Cl2 → CHCl3(triklorometana) + 3HCl
atau
CH4 + 4Cl2 → CCl4(tetraklorometana) + 4HCl
Rujukan[sunting | sunting sumber]
- ^ Kesatuan Kimia Tulen dan Gunaan Antarabangsa. "alkanes". Ringkasan Terminologi Kimia Edisi Internet.
