Atom hidrogen
 | |
| Maklumat umum | |
|---|---|
| Simbol | 1H |
| Nama | atom hidrogen, 1H, H-1, protium, ¹H |
| Proton (Z) | 1 |
| Neutron (N) | 0 |
| Data nuklid | |
| Kelimpahan semula jadi | 99.985% |
| Jisim isotop | 1.007825 Da |
| Spin | 12 |
| Tenaga lebihan | 7288.969 keV |
| Tenaga pengikatan | 0.000 keV |
| Isotop hidrogen Jadual nuklid lengkap | |
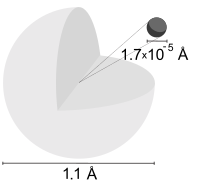
Atom hidrogen ialah atom unsur kimia hidrogen. Atom dengan cas elektrik neutral ini mempunyai satu proton bercas positif dan satu elektron bercas negatif yang diikat pada nukleus oleh daya Coulomb. Hidrogen atom membentuk kira-kira 75% jisim unsur alam semesta. (Kebanyakan jisim alam semesta bukannya dalam bentuk unsur kimia, iaitu jirim "barion", tetapi dalam bentuk jirim gelap dan tenaga gelap.)
Dalam kehidupan seharian di Bumi, atom hidrogen yang terasing (biasanya dinamakan "hidrogen atom", atau lebih tepat lagi "hidrogen monoatom") adalah sangat jarang. Sebaliknya, hidrogen cenderung untuk bergabung dengan atom-atom lain dalam bentuk sebatian, atau dengan dirinya sendiri untuk menghasilkan gas hidrogen dwiatom yang biasa, H2. Istilah "hidrogen atom" dan "atom hidrogen" memberi makna yang berbeza. Misalnya, satu molekul air mengandungi dua atom hidrogen, tetapi tidak mengandungi hidrogen atom (yang merujuk kepada atom hidrogen yang terasing).
Penghasilan dan kereaktifan
[sunting | sunting sumber]Ikatan H-H ialah salah satu ikatan yang paling kuat dalam kimia, dengan entalpi peleraian ikatan sebanyak 435.88 kJ/mol pada 298 K (25 °C; 77 °F). Kesan ikatan yang kuat ini, hanya sebahagian kecil H2 terlerai sehingga ia mencapai suhu yang lebih tinggi. Pada 3,000 K (2,730 °C; 4,940 °F), darjah peleraian hanyalah setakat 7.85%:
- H2 ⇌ 2 H
Atom hidrogen sangatlah reaktif sehinggakan ia bergabung dengan hampir setiap unsur.
Isotop
[sunting | sunting sumber]Isotop yang terbanyak, hidrogen-1, protium atau hidrogen ringan, tidak mempunyai neutron; isotop hidrogen yang lain seperti deuterium dan tritium, mempunyai satu atau lebih neutron. Formula-formula yang diberikan di bawah boleh digunakan bagi ketiga-tiga isotop hidrogen, tetapi nilai pemalar Rydberg yang sedikit berbeza perlu digunakan bagi setiap isotop hidrogen (formula pembetulan diberikan di bawah).
Analisis teori kuantum
[sunting | sunting sumber]Atom hidrogen mempunyai kepentingan istimewa dalam mekanik kuantum dan teori medan kuantum sebagai sistem fizikal masalah dua jasad ringkas yang menghasilkan pelbagai penyelesaian analitik yang ringkas dalam bentuk tertutup.
Pada tahun 1913, Neils Bohr telah memperoleh frekuensi spektrum atom hidrogen selepas membuat beberapa andaian meringkaskan. Andaian-andaian ini; asas kepada model Bohr, tidak tepat sepenuhnya tetapi boleh memperoleh jawapan tenaga yang agak tepat (dengan ralat relatif dalam tenaga pengionan keadaan asas kira-kira α2/4 atau kira-kira 10-5). Hasil-hasil Bohr bagi frekuensi dan nilai-nilai tenaga dasar telah diulang oleh penyelesaian persamaan Schrödinger pada tahun 1925-1926. Penyelesaian kepada persamaan Schrödinger bagi hidrogen adalah analitik yang memberikan ungkapan mudah bagi paras-paras tenaga hidrogen dan kemudiannya frekuensi garis spektrum hidrogen. Penyelesaian persamaan Schrödinger telah pergi lebih jauh berbanding model Bohr, kerana ia juga memperoleh bentuk fungsi gelombang elektron ("orbital") bagi pelbagai keadaan mekanik kuantum yang boleh terjadi, lalu menjelaskan sifat anisotropi ikatan atom.
Persamaan Schrödinger juga boleh digunapakai bagi atom dan molekul yang lebih rumit. Apabila terdapat lebih daripada satu elektron atau nukleus penyelesaiannya bukan analitik dan sama ada pengiraan komputer diperlukan atau andaian mempermudahkan perlu dilakukan.
Persamaan Schrödinger tidak tepat sepenuhnya. Penambahbaikan seterusnya adalah persamaan Dirac (lihat di bawah).
Penyelesaian persamaan Schrödinger: Gambaran keseluruhan hasil-hasil
[sunting | sunting sumber]Penyelesaian persamaan Schrödinger (persamaan-persamaan gelombang) bagi atom hidrogen menggunakan kenyataan bahawa potensi Coulomb yang dihasilkan oleh nukleus bersifat isotropik (ia simetri secara jejari dalam ruang dan hanya bergantung kepada jarak ke nukleus). Meskipun fungsi eigen tenaga yang terhasil (orbital) itu sendiri tidak isotropik, kebergantungannya pada koordinat sudutan mengikut penuh secara amnya daripada isotropi potensi asas ini: keadaan-keadaan eigen Hamiltonian (iaitu keadaan eigen tenaga) boleh dipilih sebagai keadaan eigen serentak pengendali momentum sudutan. Ini bersamaan dengan kenyataan bahawa momentum sudutan dikekalkan di dalam pergerakan orbital elektron di sekeliling nukleus. Oleh itu, keadaan eigen tenaga boleh dikelaskan melalui dua nombor kuantum momentum sudutan, ℓ and m (kedua-duanya integer). Nombor kuantum momentum sudutan ℓ = 0, 1, 2, ... menentukan magnitud momentum sudutan. Nombor kuantum magnetik m = -ℓ, ..., +ℓ menentukan unjuran momentum sudutan pada paksi- z (yang dipilih secara rawak).
Selain daripada ungkapan matematik bagi jumlah momentum sudutan dan unjuran momentum sudutan bagi fungsi gelombang, satu ungkapan bagi kebergantungan jejari bagi fungsi-fungsi gelombang perlu dicari. Hanya di sini butiran 1/r potensi Coulumb memainkan peranan (membawa kepada polinomial Laguerre dalam r). Ini membawa kepada nombor kuantum ketiga iaitu nombor kuantum utama n = 1, 2, 3, .... Nombor kuantum utama dalam hidrogen berkait dengan jumlah tenaga atom itu.
Perhatikan bahawa nilai tertinggi nombor kuantum momentum sudutan dihadkan oleh nombor kuantum utama: ia hanya boleh mencapai n - 1, dengan kata lain ℓ = 0, 1, ..., n − 1.
Oleh kerana pengabadian momentum sudutan, keadaan dengan ℓ yang sama tetapi m yang berbeza mempunyai tenaga yang sama (ini serupa juga bagi semua masalah dengan simetri putaran). Tambahan lagi, bagi atom hidrogen, keadaan dengan n yang sama tetapi ℓ yang berbeza juga merosot (dengan kata lain, mereka memiliki tenaga yang sama). Namun, ini adalah ciri yang khas bagi hidrogen dan tidak benar bagi atom-atom yang lebih rumit yang mempunyai potensi (berkesan) yang berbeza daripada bentuk 1/r (disebabkan kewujuda elektron dalaman yang melindungi potensi nukleus).
Dengan mengambil kira spin elektron, satu lagi nombor kuantum ditambah iaitu unjuran momentum sudutan spin elektron di sepanjang paksi z, yang boleh mempunyai dua nilai. Oleh itu, sebarang keadaan eigen elektron dalam atom hidrogen diterangkan sepenuhnya oleh empat nombor kuantum. Menurut hukum biasa mekanik kuantum, keadaan sebenar elektron boleh jadi sebarang superkedudukan keadaan-keadaan ini. Ini juga menjelaskan mengapa pemilihan paksi z bagi pengkuantaan berarah vektor momentum sudutan adalah tidak hakiki: satu orbital dengan ℓ dan m′ diberikan yang diperoleh bagi satu lagi paksi pilihan z′ boleh dinyatakan sebagai superkedudukan sesuai pelbagai keadaan dengan m yang berbeza (tetapi ℓ) yang sama yang telah diperolehi bagi z.
