Ikatan kimia
Sebuah ikatan kimia adalah tarikan tahan antara atom yang membolehkan pembentukan sebatian kimia. Bon mungkin hasil dari elektrostatik daya tarikan antara atom bertentangan dengan tuduhan, atau melalui perkongsian elektron seperti dalam atom. Kekuatan kimia bon berubah-ubah, ada "ikatan yang kuat" seperti kovalen atau ionik bon dan "lemah bon" seperti yang dibuat manusia-dibuat manusia interaksi, London sebaran daya dan hidrogen ikatan.
Sejak bertentangan dengan tuduhan menarik melalui mudah elektromagnetik, negatif dikenakan elektron yang mengorbit nukleus dan bercas proton di nukleus menarik satu sama lain. Elektron diletakkan di antara dua nukleus akan tertarik untuk mereka berdua, dan nukleus akan menarik ke arah elektron dalam kedudukan ini. Tarikan ini merupakan ikatan kimia. Kerana perkara gelombang sifat elektron dan mereka lebih kecil massa, mereka mesti menduduki jumlah yang lebih besar jumlah dibandingkan dengan inti, dan ini jumlah yang diduduki oleh elektron menyimpan inti atom agak jauh, berbanding dengan saiz nukleus diri mereka sendiri. Ini fenomena batas jarak antara nukleus dan atom dalam ikatan.
Secara umum, kuat kimia ikatan dikaitkan dengan perkongsian atau pemindahan elektron antara menyertai atom. Atom dalam molekul, kristal, logam dan dwiatom gas—memang paling fizikal di sekitar kita—diadakan bersama-sama dengan kimia bon, yang menentukan struktur dan sebahagian besar sifat perkara.

Semua bon dapat dijelaskan oleh kuantum teori, tetapi, dalam praktek, memudahkan peraturan membenarkan ahli kimia untuk meramalkan kekuatan, arah, dan kutub bon. Itu oktet peraturan dan VSEPR teori adalah dua contoh. Lebih canggih teori valens bon teori yang termasuk orbit hibridisasi dan resonans, dan molekul orbit teori yang termasuk linear kombinasi atom orbital dan ligan bidang teori. Elektrostatik digunakan untuk menggambarkan bon kutub dan kesan mereka telah mengenai bahan-bahan kimia.
Gambaran utama jenis ikatan kimia[sunting | sunting sumber]
ikatan kimia adalah satu tarikan antara atom. Tarikan ini mungkin dilihat sebagai hasil dari tingkah laku yang berbeza dari yang paling luar atau valens elektron atom. Ini laku bergabung ke satu sama lain dengan lancar dalam pelbagai keadaan, supaya tidak ada garis yang jelas yang disediakan di antara mereka. Namun ia masih berguna dan adat untuk membezakan antara jenis bon, yang menyebabkan berbeza sifat perkara pekat.
Yang paling mudah melihat seorang kovalen bond, satu atau lebih elektron (sering sepasang elektron) ditarik ke dalam ruang di antara dua inti atom. Energi dilepaskan oleh ikatan pembentukan. Ini bukan kerana pengurangan potensi tenaga, karena tarikan dua elektron untuk dua proton [penjelasan yang diperlukan] diimbangi oleh elektron-elektron dan proton-proton repulsions. Sebaliknya, pengeluaran tenaga (dan itu kestabilan ikatan) timbul dari pengurangan kinetik tenaga disebabkan oleh elektron yang lebih ruang diedarkan (iaitu lagi de Broglie panjang gelombang) orbit dibandingkan dengan setiap elektron yang terkurung lebih dekat untuk masing-masing nukleus.[1] bon Ini wujud antara dua tertentu dikenal pasti atom dan mempunyai satu arah di ruang, memungkinkan mereka untuk ditunjukkan sebagai satu garis-garis yang menghubungkan antara atom dalam lukisan, atau dimodelkan sebagai kayu antara bidang dalam model.
Di kutub kovalen bond, satu atau lebih elektron tidak sama bersama antara dua nukleus. Atom sering hasil dalam pembentukan kecil koleksi baik-disambungkan atom dipanggil molekul, yang pada padatan dan cecair terikat dengan yang lain molekul oleh kuasa yang sering lebih lemah daripada atom yang memegang molekul dalaman bersama-sama. Seperti yang lemah ikatan antara molekul memberikan bahan molekul organik, seperti lilin dan minyak, mereka lembut besar karakter, dan mereka lebur rendah mata (dalam cecair, molekul mesti dihentikan paling tersusun atau berorientasi kontak dengan satu sama lain). Ketika atom link panjang rantai atom dalam molekul besar, bagaimanapun (seperti dalam polimer seperti nilon), atau ketika atom melanjutkan rangkaian melalui padatan yang tidak terdiri dari diskrit molekul (seperti berlian atau kuarsa atau silikat mineral dalam banyak jenis rock) kemudian struktur yang hasilnya mungkin kedua-dua kuat dan tangguh, sekurang-kurangnya di arah berorientasi betul dengan rangkaian atom. Juga, lebur mata seperti kovalen polimer dan rangkaian peningkatan yang besar.
Dalam mudah melihat sebuah ionik bond, ikatan elektron tidak bersama sama sekali, tetapi dipindahkan. Dalam jenis ini bond, luar atom orbit satu atom telah kekosongan yang membolehkan samping itu satu atau lebih elektron. Ini baru ditambah elektron berpotensi menduduki tenaga yang lebih rendah-negeri (berkesan lebih dekat untuk lebih nuklear mengenakan) daripada mereka pengalaman yang berbeda atom. Oleh itu, satu nukleus menawarkan yang lebih ketat terikat posisi untuk elektron daripada tidak nukleus lain, dengan keputusan yang salah atom boleh memindahkan elektron untuk yang lain. Pemindahan ini menyebabkan satu atom untuk menganggap yang bersih positif jawab, dan yang lain untuk menganggap yang bersih negatif bertanggungjawab. Itu bon kemudian keputusan dari elektrostatik ketertarikan antara atom, atom menjadi positif atau negatif dikenakan ion. Ionik bon boleh dilihat sebagai contoh melampau polarisasi dalam atom. Sering, bon itu tidak tertentu dalam ruang, sejak mereka hasil dari yang sama elektrostatik tarikan setiap ion untuk semua ion di sekitar mereka. Ionik bon kuat (dan itu ionik bahan memerlukan suhu yang tinggi untuk mencairkan) tapi juga rapuh, sejak kuasa antara ion jarak pendek dan tidak mudah jambatan retak dan patah. Ini jenis bon memberikan naik ke ciri-ciri fizikal kristal klasik garam mineral, seperti meja garam.
Yang kurang sering disebut jenis ikatan adalah logam ikatan. Dalam jenis ini ikatan, setiap atom dalam logam menyumbang satu atau lebih elektron untuk "laut" elektron yang tinggal di antara banyak atom logam. Dalam hal ini laut, setiap elektron adalah percuma (menurut sifat gelombang) dikaitkan dengan banyak atom sekaligus. Bon keputusan kerana logam atom menjadi agak bercas kerana kehilangan mereka elektron sementara elektron tetap tertarik untuk banyak atom, tanpa menjadi bagian dari apa-apa yang diberikan atom. Logam ikatan yang boleh dilihat sebagai sebuah contoh yang ekstrim dari delocalization elektron lebih besar sistem atom, di mana setiap atom terlibat. Ini jenis ikatan sering sangat kuat (menyebabkan kekuatan tegangan logam). Bagaimanapun, logam ikatan yang lebih kolektif dalam alam daripada jenis lain, dan begitu ia membenarkan logam kristal untuk lebih mudah berubah bentuk, karena mereka terdiri dari atom tertarik untuk satu sama lain, tetapi tidak di mana-mana khususnya berorientasi cara. Ini keputusan dalam sifat lunak logam. Laut elektron dalam logam ikatan menyebabkan bersifat baik elektrik dan terma logam, dan juga mereka "shiny" refleksi yang paling frekuensi cahaya putih.
Sejarah[sunting | sunting sumber]
Awal spekulasi tentang sifat kimia bond, dari pada awal abad ke-12, seharusnya bahwa beberapa jenis kimia spesies yang telah disertai oleh jenis kimia pertalian. Dalam 1704, Sir Isaac Newton terkenal digariskan atom ikatan teori, "Pertanyaan 31" Opticks, di mana atom lampirkan untuk satu sama lain dengan beberapa "force". Secara khusus, selepas mengakui pelbagai popular teori menjadi tren di masa, bagaimana atom telah alasan untuk melampirkan ke satu sama lain, yaitu "ketagih atom", "terpaku bersama-sama dengan sisanya", atau "terjebak bersama-sama dengan bersekongkol usul", Newton menyatakan bahwa dia akan agak membuat kesimpulan dari mereka perpaduan, yang "partikel menarik satu sama lain oleh beberapa kekerasan, yang segera hubungi adalah sangat kuat, pada jarak yang kecil melakukan operasi kimia, dan sampai tidak jauh dari partikel dengan apa-apa masuk akal kesan."
Pada tahun 1819, pada tumit ciptaan longgokan voltan, Jöns Jakob Berzelius membangunkan teori kimia kombinasi menekankan elektronegatif dan ion larut watak-watak menggabungkan atom. Pada pertengahan abad ke-19, Edward Frankland, F. A. Kekulé, A. S. Couper, Alexander Butlerov, dan Hermann Kolbe, bangunan di teori radikal, maju teori valensi, asalnya disebut "menggabungkan kekuatan", di mana sebatian telah disertai oleh kerana satu tarikan kutub positif dan negatif. Pada tahun 1916, ahli kimia Gilbert N. Lewis mengembangkan konsep elektron-sepasang bond, di mana dua atom boleh berkongsi satu untuk enam elektron, itu membentuk tunggal elektron bon, yang tunggal bond, dua bond, atau tiga kali lipat bon; dalam Lewis kata-kata sendiri, "elektron boleh membentuk bagian dari shell yang berbeza dua atom dan tidak dapat dikatakan untuk milik salah satu secara eksklusif."[2]
Pada tahun 1927, yang pertama secara matematis lengkap kuantum keterangan yang mudah kimia bond, iaitu bahawa dihasilkan oleh satu elektron di hidrogen molekul ion, H2+, telah diperolehi oleh denmark fisikawan Oyvind Burrau.[3] kerja-kerja Ini menunjukkan bahawa kuantum pendekatan untuk ikatan kimia dapat menghasilkan dan kuantitatif betul, tapi kaedah matematik digunakan tidak dapat dilanjutkan untuk molekul yang mengandungi lebih daripada satu elektron. Yang lebih praktis, walaupun kurang kuantitatif, pendekatan yang telah dimasukkan ke depan di tahun yang sama dengan Walter Heitler dan Fritz London. Itu Heitler-London kaedah bentuk dasar apa yang sekarang disebut valens bon teori. Pada tahun 1929, linear kombinasi atom orbital molekul orbit kaedah (LCAO) anggaran itu diperkenalkan oleh Sir John Lennard-Jones, yang juga mencadangkan kaedah untuk mendapatkan elektronik struktur molekul F2 (florin) dan O2 (oksigen) molekul, asas dari kuantum prinsip-prinsip. Ini molekul orbit teori mewakili kovalen bon sebagai orbit dibentuk dengan menggabungkan mekanik kuantum Schrödinger atom orbital yang telah hipotesis untuk elektron dalam atom tunggal. Persamaan untuk ikatan elektron di multi-elektron atom tidak dapat diselesaikan untuk kesempurnaan matematik (iaitu, analitik), tapi anggaran untuk mereka yang masih memberikan banyak yang baik kualitatif ramalan dan keputusan. Paling kuantitatif pengiraan dalam moden kimia kuantum menggunakan sama ada ikatan valens atau molekul orbit teori sebagai titik permulaan, walaupun pendekatan ketiga, kepadatan berfungsi teori, telah menjadi semakin populer dalam beberapa tahun kebelakangan ini.
Pada tahun 1933, H. H. James dan A. S. Coolidge dijalankan pengiraan di dihydrogen molekul itu, tidak seperti sebelumnya pengiraan yang digunakan fungsi hanya jarak elektron dari inti atom, digunakan fungsi yang juga dengan jelas berkata jarak antara dua elektron.[4] Dengan 13 laras parameter mereka memperoleh hasil sangat dekat dengan hasil eksperimen untuk penceraian tenaga. Kemudian sambungan telah digunakan sehingga 54 parameter dan memberikan yang sangat baik perjanjian dengan eksperimen. Pengiraan ini meyakinkan komunitas ilmiah yang kuantum teori bisa memberikan perjanjian dengan eksperimen. Namun pendekatan ini telah tiada fizikal gambar-gambar valens ikatan molekul dan orbit teori-teori dan sukar untuk melanjutkan untuk molekul yang lebih besar.
Bon di formula kimia[sunting | sunting sumber]
Karena atom dan molekul tiga-dimensi, ia sukar untuk menggunakan satu kaedah untuk menunjukkan orbital dan bon. Dalam molekul rumus kimia bon (mengikat orbital) antara atom ditunjukkan dalam cara yang berbeza bergantung pada jenis perbincangan. Kadang-kadang, beberapa butiran yang diabaikan. Sebagai contoh, di kimia organik satu kadang-kadang hanya peduli dengan kumpulan berfungsi molekul. Oleh itu, molekul formula etanol mungkin ditulis dalam conformational bentuk, bentuk tiga dimensi, penuh dua dimensi bentuk (menunjukkan setiap bond dengan tidak tiga-dimensi arah), mampat dua dimensi bentuk (BAB3–CH2–OH), dengan memisahkan berfungsi kumpulan dari bahagian lain molekul (C2H5OH), atau oleh atom konstituen (C2H6O), menurut apa yang dibincangkan. Kadang-kadang, bahkan bukan ikatan valens shell elektron (dengan dua dimensi anggaran arah) ditandai, contohnya untuk unsur karbon .'C'. Beberapa ahli kimia mungkin juga mark masing-masing orbital, seperti yang dibayangkan ethene-4 anion (\/C=C/\ -4) menunjukkan kemungkinan bon pembentukan.
ikatan kimia[sunting | sunting sumber]
| Typical bond lengths in pm and bond energies in kJ/mol. | ||
| Bond | Length (pm) |
Energy (kJ/mol) |
|---|---|---|
| H — Hydrogen | ||
| H–H | 74 | 436 |
| H–O | 96 | 366 |
| H–F | 92 | 568 |
| H–Cl | 127 | 432 |
| C — Carbon | ||
| C–H | 109 | 413 |
| C–C | 154 | 348 |
| C–C= | 151 | |
| =C–C≡ | 147 | |
| =C–C= | 148 | |
| C=C | 134 | 614 |
| C≡C | 120 | 839 |
| C–N | 147 | 308 |
| C–O | 143 | 360 |
| C–F | 134 | 488 |
| C–Cl | 177 | 330 |
| N — Nitrogen | ||
| N–H | 101 | 391 |
| N–N | 145 | 170 |
| N≡N | 110 | 945 |
| O — Oxygen | ||
| O–O | 148 | 145 |
| O=O | 121 | 498 |
| F, Cl, Br, I — Halogens | ||
| F–F | 142 | 158 |
| Cl–Cl | 199 | 243 |
| Br–H | 141 | 366 |
| Br–Br | 228 | 193 |
| I–H | 161 | 298 |
| I–I | 267 | 151 |
Ikatan ionik[sunting | sunting sumber]
Ionik ikatan adalah jenis elektrostatik interaksi antara atom yang besar keelektronegatifan perbezaan. Tidak ada yang tepat nilai yang membezakan ionik dari kovalen, tetapi perbezaan keelektronegatifan lebih 1.7 mungkin ionik, dan perbezaan kurang dari 1.7 mungkin kovalen.[6] Ionik ikatan petunjuk untuk memisahkan positif dan negatif ion. Ionik tuduhan yang biasa di antara -3e untuk +3e. Ionik ikatan yang biasa berlaku dalam garam logam seperti natrium klorida (meja garam). Ciri khas dari ionik bon adalah spesies bentuk ke ionik kristal, di mana tidak ada ion adalah khusus berpasangan dengan apa-apa pun yang lain ion, dalam satu arah tertentu. bond. Sebaliknya, setiap spesies ion dikelilingi oleh ion yang bertentangan yang bertanggungjawab, dan jarak antara itu dan setiap berlawanan ion dekat itu, adalah hal yang sama untuk semua sekitar atom jenis yang sama. Ia adalah itu tidak lebih mungkin untuk mengaitkan ion dengan apa-apa khusus lain tunggal terionisasi atom dekat. Ini adalah situasi yang tidak seperti yang dalam kovalen kristal, di mana atom antara khusus atom masih dilihat dari jarak yang lebih pendek antara mereka, yang diukur melalui teknik seperti X-ray difraksi.
Ionik kristal mungkin mengandungi campuran kovalen dan ionik spesies yang, sebagai contohnya garam kompleks asid, seperti natrium sianida, NaCN. X-ray difraksi menunjukkan bahwa dalam NaCN, untuk contoh, ikatan antara natrium nya (Na+) dan sianida batuan (CN−) ionik, dengan tidak natrium ion yang berkaitan dengan apa-apa tertentu sianida. Bagaimanapun, ikatan antara C dan N atom dalam sianida yang kovalen jenis, membuat setiap karbon dan nitrogen yang berkaitan dengan hanya satu yang bertentangan dengan jenis, ke mana ia secara fisik lebih dekat daripada yang lain karbon atau nitrogens dalam natrium sianida kristal.
Ketika itu kristal cair ke cecair, ionik bon patah pertama karena mereka bukan arah dan membenarkan spesies dikenakan untuk bergerak bebas. Begitu juga, ketika seperti garam larut dalam air, ionik bon biasanya dipecahkan oleh interaksi dengan air, tetapi atom terus memegang. Sebagai contoh, dalam penyelesaian, sianida ion, masih terikat bersama-sama sebagai satu CN− ion, bergerak bebas melalui penyelesaian, seperti yang dilakukan ion natrium, dan Na+. Di dalam air, ion bergerak selain kerana setiap daripada mereka yang lebih kuat tertarik untuk beberapa molekul air, daripada untuk satu sama lain. Tarikan antara ion dan molekul air dalam penyelesaian itu adalah disebabkan oleh jenis lemah dibuat manusia-dibuat manusia jenis kimia. bond. Dalam cair ionik sebatian, ion terus menjadi tertarik kepada satu sama lain, tetapi tidak di mana-mana diperintahkan atau kristal.
Kovalen bon[sunting | sunting sumber]
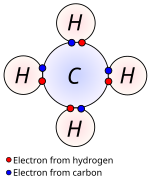
Kovalen adalah jenis biasa ikatan, di mana dua atom berkongsi dua valens elektron, satu dari setiap atom. Dalam nonpolar atom, keelektronegatifan perbezaan antara terikat atom kecil, biasanya 0 untuk 0.3. Bon dalam paling organik senyawa yang digambarkan sebagai kovalen. Angka menunjukkan metana (BAB4), di mana setiap hidrogen membentuk ikatan kovalen dengan karbon. Lihat sigma bon dan pi bon untuk LCAO-keterangan apa-apa ikatan.
Molekul yang terbentuk terutamanya dari bukan kutub atom sering tak boleh campur dalam air atau yang lain pelarut kutub, tapi lebih larut dalam bukan kutub pelarut seperti menerusi.
Satu kutub kovalen bond adalah kovalen ikatan dengan penting ionik watak. Ini bermakna kedua-dua bersama elektron lebih dekat ke salah satu atom daripada yang lain, mewujudkan ketidakseimbangan yang bertanggungjawab. Bon itu berlaku antara dua atom dengan sederhana berbeza electronegativities dan menimbulkan yang dibuat manusia-dibuat manusia interaksi. Itu keelektronegatifan perbezaan antara dua atom dalam ikatan ini adalah 0.3 untuk 1.7.
Tunggal dan beberapa bon[sunting | sunting sumber]
Yang satu ikatan antara dua atom sepadan untuk berbagi satu pasangan elektron. Elektron kepadatan ini dua ikatan elektron tertumpu di kawasan antara dua atom, yang menentukan kualitas yang sigma bond.

Yang dua ikatan antara dua atom dibentuk oleh perkongsian dua pasang elektron, satu dalam sigma bon dan satu dalam pi bond, dengan elektron kepadatan tertumpu pada dua sisi berlawanan internuclear axis. A triple bon terdiri dari tiga bersama pasangan elektron, membentuk satu sigma dan dua pi bon.
Quadruple dan lebih tinggi bon yang sangat jarang dan hanya berlaku antara tertentu peralihan logam atom.
Koordinat kovalen bond (Dipolar ikatan)[sunting | sunting sumber]

Sebuah koordinat kovalen bond adalah kovalen bon di mana kedua-dua bersama ikatan elektron dari satu sama atom terlibat dalam ikatan. Sebagai contoh, boron trifluoride (BF3) dan ammonia (NH3) dari adduct atau koordinasi kompleks F3B KESAN NH3 dengan B–N bon di mana pasangan lone elektron pada N dibagi dengan kosong atom orbit di B. BF3 dengan kosong orbit digambarkan sebagai pasangan elektron penerima atau Lewis asid, ketika NH3 dengan lone pasangan yang boleh berkongsi digambarkan sebagai elektron-sepasang donor atau Lewis pangkalan. Elektron bersama kira-kira sama rata di antara atom dalam kontras untuk ikatan ionik. Itu ikatan ditunjukkan oleh anak panah menunjuk ke Lewis asid.
Peralihan logam kompleks biasanya terikat oleh koordinat atom. Sebagai contoh, ion Ag+ bertindak sebagai Lewis asid dengan dua molekul Lewis pangkalan NH3 untuk membentuk kompleks ion Ag(NH3)2+, yang memiliki dua Ag Kesan N koordinat atom.
Logam ikatan[sunting | sunting sumber]
Dalam logam ikatan, ikatan elektron delocalized lebih kisi atom. Sebaliknya, di ionik sebatian, lokasi mengikat elektron dan mereka bayaran statik. Bebas bergerak atau delocalization ikatan elektron membawa klasik logam ciri-ciri seperti kilau (cahaya permukaan pembalik), listrik dan terma, kemuluran, dan tinggi kekuatan tegangan.
Ikatan molekul[sunting | sunting sumber]
Terdapat empat jenis asas ikatan yang dibentuk antara dua atau lebih (jika tidak, bukan dikaitkan) molekul, ion atau atom. Molekul angkatan menyebabkan molekul menjadi tertarik atau ditangkis oleh satu sama lain. Sering, ini menentukan beberapa ciri-ciri fizikal (seperti titik lebur) bahan.
- Perbezaan yang besar di keelektronegatifan antara dua terikat atom akan menyebabkan tetap mengenakan pemisahan, atau dibuat manusia, di dalam molekul atau ion. Dua atau lebih molekul atau ion dengan tetap dipoles bisa berinteraksi dalam dibuat manusia-dibuat manusia interaksi. Ikatan elektron dalam molekul atau ion akan, rata-rata, lebih dekat lebih elektronegatif atom lebih sering daripada yang kurang elektronegatif satu, memberikan naik ke separa tuduhan pada setiap atom, dan menyebabkan elektrostatik angkatan antara molekul atau ion.
- Sebuah ikatan hidrogen berkesan contoh yang kuat interaksi antara dua tetap dipoles. Perbezaan yang besar di electronegativities antara hidrogen dan mana-mana florin, nitrogen dan oksigen, ditambah pula dengan mereka lone pasangan elektron menyebabkan kuat elektrostatik angkatan antara molekul. Hidrogen bon bertanggungjawab untuk tinggi mendidih mata air dan ammonia dengan hormat untuk mereka yang lebih berat analog.
- Ini London penyebaran memaksa timbul akibat serta-merta dipoles di tetangga atom. Seperti yang negatif menjaga elektron tidak seragam sekitar seluruh atom, ada selalu mengenakan ketidakseimbangan. Ini kecil mengenakan akan mendorong satu sama dibuat manusia di dekatnya molekul; menyebabkan satu tarikan antara kedua-dua. Elektron kemudian bergerak ke bahagian lain awan elektron dan tarikan rusak.
- Yang kasi–pi interaksi berlaku antara pi bon dan yang kasi.
Teori ikatan kimia[sunting | sunting sumber]
Dalam (tidak realistik) had "yang murni" ionik ikatan, elektron yang sempurna setempat pada salah satu dari dua atom dalam ikatan. Bon itu bisa dipahami oleh fizik klasik. Angkatan antara atom ditandai oleh isotropic kontinum elektrostatik potensi. Mereka sebesar ini di bahagian yang mudah untuk yang mengenakan perbezaan.
Atom yang lebih baik dipahami oleh ikatan valens teori atau molekul orbit teori. Sifat-sifat yang atom terlibat dapat difahami menggunakan konsep-konsep seperti oksidasi nombor. Elektron kepadatan dalam ikatan yang tidak diberikan kepada individu atom, tetapi sebaliknya delocalized antara atom. Dalam ikatan valens teori, dua elektron pada dua atom ditambah bersama-sama dengan bond kekuatan bergantung pada pertindihan di antara mereka. Dalam molekul orbit teori, linear kombinasi atom orbital (LCAO) membantu menggambarkan delocalized molekul orbit struktur dan tenaga berdasarkan atom orbital atom mereka datang dari. Tidak seperti yang murni ionik bon, atom mungkin telah diarahkan anisotropic sifat. Ini mungkin mempunyai nama-nama mereka sendiri, seperti sigma bon dan pi bond.
Rujukan[sunting | sunting sumber]
- ^ {Rioux, F. The Covalent Bond in H 2.
- ^ Lewis, Gilbert N. (1916).
- ^ Laidler, K. J. (1993).
- ^ James, H. H.; Coolidge, A. S. (1933).
- ^ "Bond Lengths and Energies" Diarkibkan 2007-12-14 di Wayback Machine.
- ^ Atkins, Peter; Loretta Jones (1997).
