Pewarnaan H&E

Pewarnaan hematoksilin dan eosin (selalunya disingkatkan jadi pewarnaan H&E atau pewarnaan HE) merupakan salah satu daripada kaedah pewarnaan tisu utama yang digunakan dalam bidang histologi.[1][2][3] Ia merupakan kaedah pewarnaan yang paling banyak digunakan dalam diagnosis perubatan dan selalunya merupakan piawaian emas.[4] Contohnya, apabila seorang ahli patologi melihat biopsi kanser yang disyaki, keratan histologi mungkin diwarnai dengan H&E.
Kaedah H&E menggunakan gabungan dua pewarna histologi: hematoksilin dan eosin. Hematoksilin mewarnakan nukleus sel dengan warna biru keunguan, dan eosin mewarnakan matriks ekstrasel dan sitoplasma dengan warna merah jambu, manakala struktur lain pula diwarnakan dengan bayangan, rona dan warna hasil gabungan hematoksilin dan eosin pada tahap yang berbeza-beza.[5][6] Disebabkan itulah ahli patologi dapat dengan mudah membezakan antara bahagian nukleus dengan sitoplasma dalam sebuah sel, tambahan pula corak keseluruhan pewarnaan tersebut menunjukkan susun atur sel dan taburan sel secara umum, sehingga dapat memberikan gambaran umum struktur sampel tisu.[7] Oleh itu, pengecaman corak, baik melalui kepakaran manusia sendiri mahupun melalui perisian yang membantu pakar tersebut (dalam bidang patologi digital) dapat menyediakan maklumat histologi.
Kombinasi dua pewarna ini diperkenalkan pada tahun 1877 oleh ahli kimia Nicolaus Wissozky di Universiti Diraja Kasan di Rusia.[8][7]
Kegunaan[sunting | sunting sumber]
Prosedur pewarnaan H&E merupakan pewarnaan tunjang dalam bidang histologi[3][7][2][5] kerana ia boleh dilakukan dengan cepat,[7] tidak mahal, dan mewarnakan tisu dalam cara yang boleh mendedahkan[7][5][4] sejumlah besar anatomi mikroskopik,[9][10] dan boleh digunakan untuk mendiagnosis pelbagai keadaan histopatologi.[8] Hasil daripada pewarnaan H&E tidak terlalu bergantung pada bahan kimia yang digunakan untuk menetap tisu mahupun sedikit ketidakkonsistenan dalam protokol makmal,[11] dan faktor-faktor ini menyumbang kepada penggunaan rutinnya dalam histologi.[7]
Pewarnaan H&E tidak selalunya memberikan kontras yang mencukupi untuk membezakan semua tisu, struktur sel, mahupun corak taburan bahan kimia.[9] Jika butiran yang lebih lanjut diperlukan, maka pewarnaan dan kaedah yang lebih khusus perlu digunakan.[10][7]
Kaedah penerapan[sunting | sunting sumber]

Terdapat banyak cara untuk menyediakan larutan hematoksilin (formulasi) yang digunakan dalam prosedur H&E,[11][12][6] tambahan pula terdapat banyak protokol makmal untuk menghasilkan slaid berwarna H&E,[9] dengan sesetengah daripada cara-cara atau protokol-protokol tersebut mungkin khusus hanya untuk sesebuah makmal tertentu.[7] Walaupun tiada prosedur piawai,[11][9] hasil pewarnaan kebiasaannya bersifat konsisten kerana nukleus sel diwarnakan biru dan sitoplasma dan matriks ekstrasel diwarnakan merah jambu.[7] Makmal histologi juga boleh melaraskan kandungan atau jenis pewarnaan khusus untuk pakar patologi tertentu.[7]
Selepas tisu telah dikumpul (selalunya sebagai biopsi) dan difiksasi, ia lazimnya dinyahairkan dan ditanam dalam lilin parafin cair, selepas itu blok yang terhasil dipasang pada mikrotom dan dihiris menjadi helaian parafin yang nipis.[6] Helaian tersebut dilekatkan pada slaid mikroskop dengan seterusnya lilin dikeluarkan oleh pelarut dan hirisan tisu yang melekat pada slaid dihidrasi semula dan sedia untuk pewarnaan.[6] Alternatifnya, pewarnaan H&E ialah noda yang paling banyak digunakan dalam pembedahan Mohs melalui penggunaan tisu yang biasanya dibekukan, dipotong pada kriostat (mikrotom yang memotong tisu beku), difiksasi dalam alkohol dan kemudian diwarnakan.[9]
Kaedah pewarnaan H&E melibatkan penggunaan pewarna hematoksilin yang bercampur dengan garam logam (atau mordan) selalunya diikuti dengan bilasan dalam larutan asid lemah untuk menghilangkan pewarnaan berlebihan (pembezaan), diikuti dengan pembiruan dalam larutan beralkali sederhana.[13][8][14] Selepas penggunaan hematoksilin, tisu diwarna balas dengan eosin (kebiasaannya eosin Y).[6][8][7]
Hasil[sunting | sunting sumber]
Hematoksilin pada dasarnya mewarnakan nukleus sel dengan warna biru atau ungu tua,[6][15][14] bersama-sama dengan beberapa tisu lain, seperti butiran keratohialin dan bahan terkalsifikasi . Eosin pula mewarnakan sitoplasma dan beberapa struktur lain termasuk matriks ekstrasel seperti kolagen[5][7][14] sehingga lima jenis warna merah jambu.[8] Struktur eosinofil (bahan yang diwarnai oleh eosin) biasanya terdiri daripada protein intrasel atau ekstrasel. Jasad Lewy dan jasad Mallory merupakan contoh struktur eosinofil. Kebanyakan sitoplasma adalah eosinofil dan menjadi merah jambu.[10][15] Sel darah merah pula diwarnakan dengan merah berkepekatan tinggi.
Cara tindakan[sunting | sunting sumber]
Walaupun hematein (yakni bentuk teroksida hematoksilin)[5][16][14] merupakan pewarna aktif (apabila digabungkan dengan mordan), pewarna tersebut masih dirujuk sebagai hematoksilin.[8][13] Hematoksilin apabila digabungkan dengan mordan (kebiasaannya tawas aluminium) sering dianggap sebagai "menyerupai"[10] pewarna bes, bercas positif, atau kation.[5] Eosin merupakan pewarna anion (bercas negatif) dan berasid.[5][10] Pewarnaan nukleus oleh hemalum (gabungan ion aluminium dan hematein)[14] biasanya disebabkan oleh pengikatan kompleks pewarna-logam terhadap DNA, tetapi pewarnaan nukleus boleh diperolehi selepas pengekstrakan DNA daripada bahagian tisu tersebut.[14] Mekanismenya adalah berbeza daripada pewarnaan nukleus oleh pewarna asas (kation) seperti tionin atau biru toluidin.[10] Pewarnaan oleh pewarna bes hanya berlaku pada larutan yang kurang berasid daripada hemalum, dan ia dihalang oleh pengekstrakan asid nukleik secara kimia atau berenzim sebelumnya. Terdapat bukti untuk menunjukkan bahawa ikatan koordinat, sama seperti yang mengikat aluminium dan hematein, mengikat kompleks hemalum kepada DNA dan kepada kumpulan karboksi protein dalam kromatin nukleus.
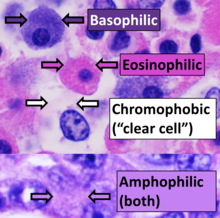
Sesuatu struktur sel tidak perlu bersifat asid atau bes untuk dipanggil basofil dan eosinofil; terminologi tersebut adalah berdasarkan pertalian komponen sel terhadap pewarna. Warna lain, contohnya kuning dan coklat, boleh didapati dalam sampel; ia disebabkan oleh pigmen intrinsik seperti melanin. Lamina dasar perlu diwarnai oleh pewarna PAS atau beberapa pewarna perak, jika ia perlu kelihatan dengan baik. Gentian retikular juga memerlukan pewarnaan perak. Struktur hidrofobik juga cenderung untuk kekal jelas; dan struktur tersebut biasanya kaya dengan lemak, contohnya adiposit, mielin di sekeliling akson neuron, dan membran jasad Golgi.
Contoh tisu yang diwarnakan dengan H&E[sunting | sunting sumber]
-
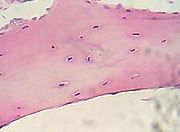
Tulang, nukleus sel (biru-ungu), matriks tulang (merah jambu).
-
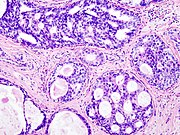
Duktus karsinoma in situ (DCIS) pada tisu payudara, nukleus sel (biru-ungu), bahan ekstrasel (merah jambu).
-
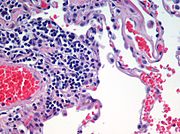
Tisu peparu yang diambil dari pesakit emfisema. Nukleus sel (biru-ungu), sel darah merah (merah terang), beberapa jasad sel dan bahasa ekstrasel lain (merah jambu), dan ruang udara kosong (putih).
-
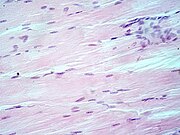
Tisu otot, nukleus sel (biru-ungu), badan sel (merah jambu).
-
Karsinoma sel dasar kulit, nukleus sel (biru-ungu), bahan ekstrasel (merah jambu).
Rujukan[sunting | sunting sumber]
- ^ Titford, M. (2005). "The long history of hematoxylin". Biotechnic & Histochemistry. 80 (2): 73–80. doi:10.1080/10520290500138372. PMID 16195172. S2CID 20338201.
- ^ a b Smith C (2006). "Our debt to the logwood tree: the history of hematoxylin". MLO Med Lab Obs. 38 (5): 18, 20–2. PMID 16761865.
- ^ a b Dapson RW, Horobin RW (2009). "Dyes from a twenty-first century perspective". Biotech Histochem. 84 (4): 135–7. doi:10.1080/10520290902908802. PMID 19384743. S2CID 28563610.
- ^ a b Rosai J (2007). "Why microscopy will remain a cornerstone of surgical pathology". Lab Invest. 87 (5): 403–8. doi:10.1038/labinvest.3700551. PMID 17401434.
- ^ a b c d e f g Chan JK (2014). "The wonderful colors of the hematoxylin-eosin stain in diagnostic surgical pathology". Int J Surg Pathol. 22 (1): 12–32. doi:10.1177/1066896913517939. PMID 24406626. S2CID 26847314.
- ^ a b c d e f Stevens, Alan (1982). "The Haematoxylins". Dalam Bancroft, John; Stevens, Alan (penyunting). The Theory and Practice of Histological Techniques (ed. 2nd). Longman Group Limited. m/s. 109.
- ^ a b c d e f g h i j k l Wittekind D (2003). "Traditional staining for routine diagnostic pathology including the role of tannic acid. 1. Value and limitations of the hematoxylin-eosin stain". Biotech Histochem. 78 (5): 261–70. doi:10.1080/10520290310001633725. PMID 14989644. S2CID 10563849.
- ^ a b c d e f Titford, Michael (2009). "Progress in the Development of Microscopical Techniques for Diagnostic Pathology". Journal of Histotechnology. 32 (1): 9–19. doi:10.1179/his.2009.32.1.9. ISSN 0147-8885. S2CID 26801839.
- ^ a b c d e Larson K, Ho HH, Anumolu PL, Chen TM (2011). "Hematoxylin and eosin tissue stain in Mohs micrographic surgery: a review". Dermatol Surg. 37 (8): 1089–99. doi:10.1111/j.1524-4725.2011.02051.x. PMID 21635628. S2CID 2538853.CS1 maint: multiple names: authors list (link)
- ^ a b c d e f Ross, Michael H.; Pawlina, Wojciech (2016). Histology : a text and atlas : with correlated cell and molecular biology (ed. 7th). Wolters Kluwer. m/s. 984p. ISBN 978-1451187427.
- ^ a b c Schulte EK (1991). "Standardization of biological dyes and stains: pitfalls and possibilities". Histochemistry. 95 (4): 319–28. doi:10.1007/BF00266958. PMID 1708749. S2CID 29628388.
- ^ Llewellyn BD (2009). "Nuclear staining with alum hematoxylin". Biotech Histochem. 84 (4): 159–77. doi:10.1080/10520290903052899. PMID 19579146. S2CID 205713596.
- ^ a b Ortiz-Hidalgo C, Pina-Oviedo S (2019). "Hematoxylin: Mesoamerica's Gift to Histopathology. Palo de Campeche (Logwood Tree), Pirates' Most Desired Treasure, and Irreplaceable Tissue Stain". Int J Surg Pathol. 27 (1): 4–14. doi:10.1177/1066896918787652. PMID 30001639.
- ^ a b c d e f Kiernan JA (2018). "Does progressive nuclear staining with hemalum (alum hematoxylin) involve DNA, and what is the nature of the dye-chromatin complex?". Biotech Histochem. 93 (2): 133–148. doi:10.1080/10520295.2017.1399466. PMID 29320873. S2CID 13481905.
- ^ a b Leeson, Thomas S.; Leeson, C. Roland (1981). Histology (ed. Fourth). W. B. Saunders Company. m/s. 600. ISBN 978-0721657042.
- ^ Kahr, Bart; Lovell, Scott; Subramony, Anand (1998). "The progress of logwood extract". Chirality. 10 (1–2): 66–77. doi:10.1002/chir.12.
Bacaan lanjut[sunting | sunting sumber]
- Kiernan JA (2008) Histological and Histochemical Methods: Theory and Practice. 4th ed. Bloxham, UK: Scion.
- Lillie RD, Pizzolato P, Donaldson PT (1976) Nuclear stains with soluble metachrome mordant lake dyes. The effect of chemical endgroup blocking reactions and the artificial introduction of acid groups into tissues. Histochemistry 49: 23–35.
- Llewellyn BD (2009) Nuclear staining with alum-hematoxylin. Biotech. Histochem. 84: 159–177.
- Puchtler H, Meloan SN, Waldrop FS (1986) Application of current chemical concepts to metal-haematein and -brazilein stains. Histochemistry 85: 353–364.