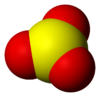
Sulfur trioksida
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC pilihan
Sulfur trioksida | |||
| Nama lain
Sulfuric anhidrida, Sulfur(VI) oksida
| |||
| Sifat | |||
| SO3 | |||
| Jisim molar | 80.066 g/mol | ||
| Rupa bentuk | Pepejal kristal jernih atau putih yang meruwap dalam udara.[1] Gas dan cecair tanpa warna[2] | ||
| Bau | Wap berbau luat seperti sulfur dioksida.[3] Kabus tidak berbau[2] | ||
| Ketumpatan | 1.92 g/cm3, liquid | ||
| Takat lebur | 16.9 °C (62.4 °F; 290.0 K) | ||
| Takat didih | 45 °C (113 °F; 318 K) | ||
| Bertindak balas menjadi asid sulfurik | |||
| Termokimia | |||
| Entropi molar piawai S |
256.77 J K−1 mol−1 | ||
Entalpi pembentukan
piawai (ΔfH⦵298) |
−395.7 kJ/mol | ||
| Bahaya | |||
| Bahaya-bahaya utama | |||
| MSDS | ICSC 1202 | ||
| Piktogram GHS |  
| ||
| Perkataan isyarat GHS | Danger | ||
| H250, H314, H310, H300, H335 | |||
| P261, P270, P280, P305+351+338, P310 | |||
| NFPA 704 (berlian api) | |||
| Takat kilat | Tidak mudah terbakar | ||
| Dos maut (LD) atau kepekatan dos maut (LC) | |||
LC50 (median kepekatan)
|
tikus, 4 hr 375 mg/m3[perlu rujukan] | ||
| Sebatian berkaitan | |||
Kation lain
|
Selenium trioksida Telurium trioksida | ||
Oksida sulfur lain berkaitan
|
Sulfur monoksida Sulfur dioksida | ||
Sebatian berkaitan
|
Asid sulfurik | ||
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |||
| | |||
| Rujukan kotak info | |||
Sulfur trioksida merupakan sebuah sebatian sulfur dengan formula SO3. Dalam bentuk gas, sulfur trioksida merupakan salah satu pencemar udara yang utama kerana sebatian ini merupakan agen utama dalam hujan asid.[4] Sulfur trioksida dihasilkan dalam industri dalam penghasilan asid sulfurik.
Rujukan[sunting | sunting sumber]
- ^ "SULFUR TRIOXIDE CAMEO Chemicals NOAA". Cameochemicals.noaa.gov.
- ^ a b Lerner, L. (2011). "Small-Scale Synthesis of Laboratory Reagents with Reaction Modeling". CRC Press. m/s. 10. ISBN 9781439813133. LCCN 2010038460.
- ^ "Substance:Sulfur trioxide - Learn Chemistry Wiki". Rsc.org.
- ^ Thomas Loerting; Klaus R. Liedl (2000). "Toward elimination of descrepancies between theory and experiment: The rate constant of the atmospheric conversion of SO3 to H2SO4". Proceedings of the National Academy of Sciences of the United States of America. 97 (16): 8874–8878. doi:10.1073/pnas.97.16.8874. PMC 16788.