Asid malonik
| |

| |
| Nama | |
|---|---|
| Nama IUPAC pilihan
Asid propanedioik[1] | |
| Nama lain
Asid metanadikarboksilik
| |
| Pengecam | |
Model 3D (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.005.003 |
PubChem <abbr title="<nowiki>Compound ID</nowiki>">CID
|
|
| UNII | |
CompTox Dashboard (<abbr title="<nowiki>U.S. Environmental Protection Agency</nowiki>">EPA)
|
|
| |
| |
| Sifat | |
| C3H4O4 | |
| Jisim molar | 104.061 g·mol−1 |
| Ketumpatan | 1.619 g/cm3 |
| Takat lebur | 135 to 137 °C (275 to 279 °F; 408 to 410 K) (terurai) |
| Takat didih | terurai |
| 763 g/L | |
| Keasidan (pKa) | pKa1 = 2.83[2] pKa2 = 5.69[2] |
| -46.3·10−6 cm3/mol | |
| Sebatian berkaitan | |
Anion lain
|
Malonat |
Asid karboksilik berkaitan
|
Asid oksalik Asid propionik Asid suksinik Asid fumarik |
Sebatian berkaitan
|
Malondialdehid Dimetil malonat |
| Hazards | |
| Lembaran data keselamatan | Pautan dokumen lembaran |
Kecuali jika dinyatakan sebaliknya, Data diberi berdasarkan bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa).
Infobox references
| |
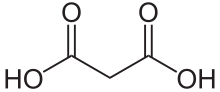
Asid malonik (nama sistematik IUPAC : asid propanedioik) ialah asid dikarboksilik berstruktur CH2(COOH)2. Bentuk terion asid malonik, serta ester dan garamnya, dikenali sebagai malonat. Contohnya, dietil malonat ialah dietil ester kepada asid malonik. Nama asid ini berasal dari perkataan Yunani μᾶλον (malon) yang bermaksud 'epal'.
Sejarah[sunting | sunting sumber]
Asid malonik ialah bahan yang terdapat secara semulajadi dalam banyak buah-buahan dan sayur-sayuran.[3] Terdapat cadangan bahawa buah sitrus yang dihasilkan melalui pertanian organik mengandungi tahap asid malonik yang lebih tinggi berbanding buah-buahan yang dihasilkan dalam pertanian konvensional. [4]
Asid malonik pertama kali disediakan pada tahun 1858 oleh ahli kimia Perancis Victor Dessaignes melalui pengoksidaan asid malik.[5]
Struktur dan penyediaan[sunting | sunting sumber]
Struktur ditentukan melalui kaedah kristalografi sinar-X [6] dan data sifat terperinci yang termasuk data termokimia fasa mampat boleh didapati di Institut Piawaian dan Teknologi Kebangsaan Amerika Syarikat.[7] Penyediaan klasik asid malonik bermula daripada asid kloroasetik:

Natrium karbonat menjana garam natrium, yang kemudiannya bertindak balas dengan natrium sianida untuk menyediakan garam natrium kepada asid sianoasetik melalui penggantian nukleofilik. Kumpulan nitril ini boleh dihidrolisis oleh natrium hidroksida menjadi natrium malonat, dan proses pengasidan seterusnya menghasilkan asid malonik. Walau bagaimanapun di peringkat perkilangan, asid malonik dihasilkan melalui hidrolisis dimetil malonat atau dietil malonat.[8] Asid ini juga boleh dihasilkan melalui penapaian glukosa.[9]
Tindak balas organik[sunting | sunting sumber]
Asid malonik bertindak balas sebagaimana kebiasaan asid karboksilik bertindak balas: membentuk amida, ester, anhidrida, dan bahan terbitan klorida.[10] Malonik anhidrida boleh digunakan sebagai perantaraan kepada bahan-bahan terbitan mono-ester atau amida, di antaranya malonil klorida paling berguna untuk mendapatkan diester atau diamida. Dalam tindak balas yang biasa dikenali, asid malonik berkondensasi dengan urea untuk membentuk asid barbiturik. Asid malonik juga boleh dikondensasi dengan aseton untuk membentuk asid Meldrum, yakni bahan perantaraan serba boleh dalam pelbagai transformasi lanjutan. Ester-ester kepada asid malonik juga digunakan sebagai sinton −CH 2COOH dalam sintesis ester malonik.
Tambahan pula, koenzim A terbitan dari malonat, malonil-KoA (bersama-sama dengan asetil KoA) ialah prekursor penting dalam biosintesis asid lemak. Malonil KoA terbentuk daripada asetil KoA oleh tindakan karboksilase asetil-KoA, dan malonat dipindahkan ke protein pembawa asil untuk ditambah kepada rantai asid lemak.
Reaksi Briggs–Rauscher[sunting | sunting sumber]
Asid malonik ialah komponen utama dalam tindak balas Briggs–Rauscher, yang merupakan contoh klasik bagi tindak balas kimia berayun.[11]
Pemeluwapan Knoevenagel[sunting | sunting sumber]
Dalam pemeluwapan Knoevenagel, asid malonik atau diester-diesternya bertindak balas dengan kumpulan karbonil pada sesuatu aldehid atau keton, diikuti dengan tindak balas penyahhidratan.

Penggunaan asid malonik itu sendiri biasanya kerana produk sasaran mempunyai langkah peringkat kedua melibatkan penghilangan karbon dioksida, yang dikenali sebagai pengubahsuaian Doebner.[12]

Oleh itu, hasil tindak balas seperti tindak balas antara akrolein dan asid malonik dalam piridina ialah asid trans-2,4-pentadienoik dengan hanya satu kumpulan asid karboksilik, bukannya dua.
Penyediaan karbon suboksida[sunting | sunting sumber]
Karbon suboksida disediakan melalui pemanasan campuran kering fosforus pentoksida (P
4O
10) dan asid malonik.[13] Tindak balas ini seakan tindak balas penyediaan malonik anhidrida yang membentuk malonat.[14]
Kegunaan dan fungsi[sunting | sunting sumber]
Asid malonik ialah prekursor kepada poliester-poliester istimewa. Asid ini boleh ditukar kepada 1,3-propanadiol untuk digunakan dalam poliester dan polimer (walaupun tahap kegunaannya kurang jelas). Ia boleh dijadikan sebagai komponen kepada pembentukan resin alkid yang digunapakai dalam penyalutan untuk melindungi daripada kerosakan yang disebabkan oleh cahaya UV, pengoksidaan dan kakisan. Satu lagi kegunaan asid malonik dalam industri salutan ialah menyambung silang salutan serbuk penawar bersuhu rendah, yang semakin berharga untuk substrat sensitif haba dan pemercepatkan proses salutan.[15] Pasaran salutan global dalam sektor automobil dianggarkan berjumlah $18.59 bilion pada 2014 dengan unjuran kadar pertumbuhan tahunan gabungan sebanyak 5.1% hingga 2022.
Asid malonik digunakan dalam pelbagai proses perkilangan sebagai bahan kimia khusus bernilai tinggi termasuk dalam industri elektronik, industri perisa dan pewangi,[3] dan industri pelarut khusus, penghubung silang polimer dan farmaseutikal. Pada tahun 2004, pengeluaran global tahunan asid malonik dan diester-diester berkaitan melebihi 20,000 tan metrik. [16] Potensi pertumbuhan pasaran ini mungkin disebabkan oleh kemajuan dalam bioteknologi industri yang berusaha untuk menggantikan bahan-bahan kimia berasaskan petroleum dalam penggunaan-penggunaan industri.
Pada tahun 2004, asid malonik telah disenaraikan oleh Jabatan Tenaga AS sebagai salah satu daripada 30 bahan kimia teratas yang akan dihasilkan melalui biojisim.
Dalam aplikasi makanan dan ubat, asid malonik boleh digunakan untuk mengawal keasidan, sama ada sebagai eksipien dalam formulasi farmaseutikal atau bahan tambahan pengawet semulajadi untuk makanan. [3]
Asid malonik digunakan sebagai blok binaan bahan kimia untuk menghasilkan pelbagai sebatian berharga,[17] termasuk sebatian-sebatian rasa dan pewangi gamma-nonalaktona, asid sinamik, dan sebatian farmaseutikal valproat.
Asid malonik (sehingga 37.5% berat per berat) telah digunakan untuk memaut silang kanji-kanji jagung dan kentang untuk menghasilkan termoplastik terbiodegradasi. Proses ini dilakukan di dalam air menggunakan pemangkin-pemangkin tidak toksik.[18][19] Polimer-polimer berasaskan kanji merangkumi 38% daripada pasaran polimer terbiodegradasi global pada tahun 2014 dengan segmen penggunaan akhir terbesar dalam bidang-bidang pembungkusan makanan, pembungkusan busa dan beg kompos.
Syarikat Eastman Kodak dan syarikat yang lain menggunakan asid malonik dan derivatif-derivatifnya sebagai bahan pelekat pembedahan.[20]
Patologi[sunting | sunting sumber]
Aras asid malonik tinggi yang disertai dengan aras asid metilmalonik tinggi akan menyebabkan penyakit metabolik gabungan asiduria malonik dan metilmalonik (CMAMMA). Melalui pengiraan nisbah asid malonik kepada asid metilmalonik dalam plasma darah, CMAMMA boleh dibezakan daripada asidemia metilmalonik klasik.[21]
Biokimia[sunting | sunting sumber]
Asid malonik ialah satu contoh klasik perencat kompetitif kepada enzim suksinat dehidrogenase (kompleks II), dalam rantaian pengangkutan elektron pernafasan.[22] Asid ini mengikat tapak aktif enzim tanpa bertindak balas atau bersaing dengan substrat suksinat biasa, namun ketiadaan kumpulan −CH2CH2− diperlukan untuk penyahhidrogenan. Pemerhatian ini digunakan untuk menyimpulkan struktur tapak aktif dalam suksinat dehidrogenase. Perencatan enzim ini mengurangkan respirasi selular.[23][24] Oleh kerana asid malonik ialah komponen semula jadi dalam pelbagai bahan makanan, ia terdapat dalam haiwan mamalia termasuk manusia.[25]
Bahan Kimia Berkaitan[sunting | sunting sumber]
Versi asid malonik terfluorinasi ialah asid difluoromalonik.[1]
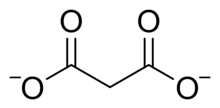
Asid malonik adalah diprotik; bermaksud ia boleh menderma dua proton untuk setiap molekul. <span about="#mwt221" class="mwe-math-element" data-mw="{"name":"math","attrs":{"chem":""},"body":{"extsrc":"pK_a"}}" id="9" typeof="mw:Extension/math"><span class="mwe-math-mathml-inline mwe-math-mathml-a11y" style="display: none;"><math xmlns="http://www.w3.org/1998/Math/MathML">
<semantics>
<mrow class="MJX-TeXAtom-ORD">
<mstyle displaystyle="true" scriptlevel="0">
<mi>p</mi>
<msub>
<mi>K</mi>
<mrow class="MJX-TeXAtom-ORD">
<mi>a</mi>
</mrow>
</msub>
</mstyle>
</mrow>
<annotation encoding="application/x-tex">{\displaystyle pK_{a}}</annotation>
</semantics>
</math></span><img alt="{\displaystyle pK_{a}}" aria-hidden="true" class="mwe-math-fallback-image-inline" data-cx="{"adapted":false}" src="https://wikimedia.org/api/rest_v1/media/math/render/svg/638bae3cdb6c6efb096307cdedc73e5ada96d81e" style="vertical-align: -0.671ex; margin-left: -0.089ex; width:4.334ex; height:2.509ex;"></span> pertamanya ialah 2.8 dan yang keduanya ialah 5.7.[2] Oleh itu ion malonat boleh jadi HOOCCH
2COO− atau CH
2(COO)2−
2. Sebatian malonat atau propanadioat termasuk garam-garam dan ester-ester asid malonik, seperti
- Dietil malonat
- Dimetil malonat
- Dinatrium malonat
- Malonil-KoA
Rujukan[sunting | sunting sumber]
- ^ International Union of Pure and Applied Chemistry (2014). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. The Royal Society of Chemistry. p. 746. doi:10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ^ a b c pKa Data Compiled by R. Williams (pdf; 77 kB) Archived 2010-06-02 at the Wayback Machine
- ^ a b c "Propanedioic acid". The Good Scents Company. Dicapai pada 2020-10-07. Ralat petik: Tag
<ref>tidak sah, nama "gsc" digunakan secara berulang dengan kandungan yang berbeza - ^ "Organic Acids Concentration in Citrus Juice from Conventional Versus Organic Farming". Acta Horticulturae. 933 (933): 601–606. 2012. doi:10.17660/actahortic.2012.933.78. ISSN 0567-7572.
|hdl-access=requires|hdl=(bantuan) - ^ "Note sur un acide obtenu par l'oxydation de l'acide malique"] (Note on an acid obtained by oxidation of malic acid)". Comptes rendus. 47: 76–79. 1858.
- ^ "An experimental charge density study of aliphatic dicarboxylic acids". Journal of Molecular Structure. 521 (1–3): 97–106. 2000. Bibcode:2000JMoSt.521...97S. doi:10.1016/S0022-2860(99)00293-8.
- ^ NIST Chemistry WebBook. "Propanedioic acid".
- ^ US patent 2373011, Britton EC, Ezra M, "Production of malonic acid", issued 1945-04-03, assigned to Dow Chemical Co
- ^ US 20200172941, Dietrich JA, "Recombinant host cells for the production of malonate.", assigned to Lygos Inc
- ^ Pollak P, Romeder G, penyunting (2005). "Malonic Acid and Derivatives". Van Nostrand's Encyclopedia of Chemistry. doi:10.1002/0471740039.vec1571. ISBN 0471740039.
- ^ "The Effect of Salicylic Acid on the Briggs-Rauscher Oscillating Reaction" (PDF). Studia UBB Chemia. 1: 285–300.
- ^ "Ueber die der Sorbinsäure homologen, ungesättigten Säuren mit zwei Doppelbindungen". Berichte der Deutschen Chemischen Gesellschaft. 35: 1136–36. 1902. doi:10.1002/cber.190203501187.
- ^ "Ueber das Kohlensuboxyd. I". Chem. Ber. 39: 689–697. 1906. doi:10.1002/cber.190603901103.
- ^ "Paradigms and Paradoxes: Aspects of the Energetics of Carboxylic Acids and Their Anhydrides". Structural Chemistry. 11 (4): 265–269. 2000. doi:10.1023/A:1009270411806.
- ^ Facke T, Subramanian R, Dvorchak M, Feng S (February 2004). "Diethylmalonate blocked isocyanate as crosslinkers for low temperature cure powder coatings.". Proceedings of 31st International Waterborene, High-Solids and Powder Coating Symposium.
- ^ "Malonic acid diesters" (PDF). Inchem. UNEP Publications. Diarkibkan daripada yang asal (PDF) pada 2017-11-18. Dicapai pada 2015-12-11.
- ^ Hildbrand, S.; Pollak, P. Malonic Acid & Derivatives.
- ^ US
- ^ "'Green' crosslinking of native starches with malonic acid and their properties". Carbohydrate Polymers. 90 (4): 1620–8. November 2012. doi:10.1016/j.carbpol.2012.07.041. PMID 22944425.
- ^ US, "Surgical Adhesive Compositions"
- ^ "A New Approach for Fast Metabolic Diagnostics in CMAMMA". JIMD Reports. Springer. 30: 15–22. 2016. doi:10.1007/8904_2016_531. ISBN 978-3-662-53681-0. PMC 5110436. PMID 26915364. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Malonate inhibition of oxidations in the Krebs tricarboxylic acid cycle". The Journal of Biological Chemistry. 178 (1): 241–250. March 1949. doi:10.1016/S0021-9258(18)56954-4. PMID 18112108.
- ^ "Studies on the Mechanism of Hydrogen Transport in Animal Tissues : VI. Inhibitor Studies with Succinic Dehydrogenase". The Journal of General Physiology. 26 (4): 391–404. March 1943. doi:10.1085/jgp.26.4.391. PMC 2142566. PMID 19873352.
- ^ "Studies on succinate dehydrogenase". Biochimica et Biophysica Acta (BBA) - Specialized Section on Enzymological Subjects. 92 (2): 233–247. 1964. doi:10.1016/0926-6569(64)90182-8.
- ^ "Metabocard for Malonic acid". Human Metabolome Database. 2020-03-13. Dicapai pada 2020-10-06.
