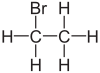
Bromoetana
| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC pilihan
Bromoetana[2] | |||
| Nama lain | |||
| Pengecam | |||
Imej model 3D Jmol
|
|||
| 1209224 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.751 | ||
| Nombor EC |
| ||
| KEGG | |||
| MeSH | bromoethane | ||
PubChem CID
|
|||
| Nombor RTECS |
| ||
| UNII | |||
| Nombor PBB | 1891 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| C2H5Br | |||
| Jisim molar | 108.97 g·mol−1 | ||
| Rupa bentuk | Cecair tak berwarna | ||
| Bau | Seperti etana | ||
| Ketumpatan | 1.46 g mL−1 | ||
| Takat lebur | −120 hingga −116 °C; −184 hingga −177 °F; 153 hingga 157 K | ||
| Takat didih | 38.0 hingga 38.8 °C; 100.3 hingga 101.8 °F; 311.1 hingga 311.9 K | ||
| 1.067 g/100 mL (0 °C) 0.914 g/100 mL (20 °C) 0.896 g/100 mL (30 °C) | |||
| Keterlarutan | Larut campur dengan etanol, eter, kloroform, pelarut organik | ||
| log P | 1.809 | ||
| Tekanan wap | 51.97 kPa (20 °C) | ||
Pemalar hukum Henry (kH)
|
1.3 μmol Pa−1 kg−1 | ||
| -54.70·10−6 cm3/mol | |||
Indeks biasan (nD)
|
1.4225 | ||
| Kelikatan | 402 Pa.s (20 °C) | ||
| Termokimia | |||
| Muatan haba tentu, C | 105.8 J K−1 mol−1 | ||
Entalpi pembentukan
piawai (ΔfH⦵298) |
−97.6–93.4 kJ mol−1 | ||
| Bahaya | |||
| Piktogram GHS |   
| ||
| Perkataan isyarat GHS | Danger | ||
| H225, H302, H332, H351 | |||
| P210, P281 | |||
| NFPA 704 (berlian api) | |||
| Takat kilat | −23 °C (−9 °F; 250 K) | ||
| 511 °C (952 °F; 784 K) | |||
| Had letupan | 6.75–11.25% | ||
| Dos maut (LD) atau kepekatan dos maut (LC) | |||
LD50 (median dos)
|
1.35 g kg−1 (oral, tikus) | ||
LC50 (median kepekatan)
|
26,980 ppm (tikus, 1 jam) 16,230 ppm (tikus, 1 jam) 4681 ppm (tikus) 2723 ppm (tikus)[3] | ||
LCLo (paling rendah diketahui)
|
3500 ppm (tikus) 24,000 ppm (tikus belanda, 30 min) 7000 ppm (tikus belanda, >4.5 jam)[3] | ||
| NIOSH (Had pendedahan kesihatan AS): | |||
PEL (Dibenarkan)
|
TWA 200 ppm (890 mg/m3)[1] | ||
REL (Disyorkan)
|
Tiada yang ditubuhkan[1] | ||
IDLH (Bahaya serta-merta)
|
2000 ppm[1] | ||
| Sebatian berkaitan | |||
alkana berkaitan
|
|||
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |||
| | |||
| Rujukan kotak info | |||
Bromoetana atau etil bromida ialah sebatian kimia dalam kumpulan haloalkana. Ia disingkatkan sebagai EtBr (juga merupakan singkatan bagi etidium bromida). Sebatian meruwap ini memiliki bau seperti eter.
Penyediaan[sunting | sunting sumber]
Penyediaan EtBr ialah model bagi penghasilan bromoalkana secara am. Ia biasanya dihasilkan melalui penambahan hidrogen bromida terhadap etena:
- H2C=CH2 + HBr → H3C-CH2Br
Bromoetana adalah murah dan jarang disediakan di makmal. Sintesis makmal termasuk bertindak balas etanol dengan campuran hidrobromik dan asid sulfurik. Laluan alternatif melibatkan refluks etanol dengan fosforus dan bromin; fosforus tribromida dihasilkan in situ.[4]
Kegunaan[sunting | sunting sumber]
Dalam sintesis organik, EtBr ialah molekul setara jenis buatan bagi karbokation etil (Et+), sinton.[5] Dalam alam nyata, kation sebegitu tidak terhasil. Sebagai contoh, garam karboksilat ditukar kepada etil ester,[6] karbanion terbitan beretil, tiourea menjadi garam etilisotiouronium,[7] dan amina menjadi etilamina.[8]
Rujukan[sunting | sunting sumber]
- ^ a b c d e NIOSH Pocket Guide to Chemical Hazards. "#0265" (dalam bahasa Inggeris). National Institute for Occupational Safety and Health (NIOSH).
- ^ "bromoethane - Compound Summary". PubChem Compound. USA: National Center for Biotechnology Information. 26 March 2005. Identification. Dicapai pada 15 June 2012.
- ^ a b "Ethyl bromide". Immediately Dangerous to Life or Health Concentrations (IDLH). Institut Kebangsaan untuk Keselamatan dan Kesihatan Pekerjaan (NIOSH).
- ^ Oliver Kamm & C. S. Marvel (1941). "Alkyl and alkylene bromides". Organic Syntheses.; Collective Volume (dalam bahasa Inggeris), 1, m/s. 25
- ^ Makosza, M.; Jonczyk, A. "Phase-Transfer Alkylation of Nitriles: 2-Phenylbutyronitrile". Organic Syntheses. 55: 91.; Collective Volume (dalam bahasa Inggeris), 6, m/s. 897
- ^ Petit, Y.; Larchevêque, M. "Ethyl Glycidate from (S)-Serine: Ethyl (R)-(+)-2,3-Epoxypropanoate". Organic Syntheses. 75: 37.; Collective Volume (dalam bahasa Inggeris), 10, m/s. 401
- ^ E. Brand; Brand, F. C. "Guanidodacetic Acid". Organic Syntheses. 22: 440.; Collective Volume (dalam bahasa Inggeris), 3
- ^ Brasen, W. R; Hauser, C. R. "o-Methylethylbenzyl Alcohol". Organic Syntheses. 34: 58.; Collective Volume (dalam bahasa Inggeris), 4, m/s. 582