Penghalang saluran kalsium
| Penghalang saluran kalsium | |
|---|---|
| Kelas ubat | |
| Pengenal kelas | |
| Kegunaan | Hipertensi, aritmia, sakit kepala kluster[1] |
| Kod ATC | C08 |
| Pautan luar | |
| MeSH | D002121 |
| Di Wikidata | |
Penghalang/Penyekat saluran kalsium (CCB), antagonis saluran kalsium atau antagonis kalsium[2] ialah sekumpulan ubat yang mengganggu pergerakan kalsium (Ca2+) melalui saluran kalsium.[3] Penyekat saluran kalsium digunakan sebagai ubat antihipertensi, yakni ubat untuk menurunkan tekanan darah pada pesakit hipertensi (tekanan darah tinggi). CCB amat berkesan terhadap kekakuan salur besar, salah satu punca biasa peningkatan tekanan darah sistolik pada pesakit warga emas.[4] Penyekat saluran kalsium juga kerap digunakan untuk mengubah kadar denyutan jantung (terutamanya daripada fibrilasi atrium), untuk mengelakkan kekejangan vasokular periferi dan serebrum, dan untuk mengurangkan sakit dada disebabkan angina pektoris.
Saluran kalsium bergantung voltan jenis N, L dan T terdapat dalam zona glomerulosa di kelenjar adrenal manusia, dan CCB boleh secara langsung mempengaruhi biosintesis aldosteron dalam sel adrenokortikal, dengan kesan susulan terhadap rawatan klinikal hipertensi dengan agen ini.[5]
CCB telah terbukti lebih berkesan sedikit daripada penyekat beta dalam menurunkan kematian kardiovaskular yang berkaitan dengan strok, tetapi ia dikaitkan dengan lebih banyak kesan sampingan.[6][7] Namun begitu, potensi risiko utama begini didapati secara lebih ketara dikaitkan dengan CCB tindakan singkat.[8]
Kelas[sunting | sunting sumber]
Dihidropiridina[sunting | sunting sumber]

Penyekat saluran kalsium dihidropiridina (DHP) berasal daripada molekul dihidropiridina, dan sering digunakan untuk mengurangkan rintangan vaskular sistemik dan tekanan arteri. Kadangkala, apabila ia digunakan untuk merawat angina, vasodilatasi dan hipotensi boleh membawa kepada takikardia refleks yang boleh memudaratkan pesakit yang mengalami gejala iskemia disebabkan oleh peningkatan permintaan oksigen miokardium. Penyekat saluran kalsium dihidropiridina boleh memburukkan lagi proteinuria pada pesakit dengan nefropati.[9]
Kelas CCB ini mudah dikenal pasti dengan akhiran "-dipina".
- Amlodipina (Norvasc)
- Aranidipina (Sapresta)
- Azelnidipina (Calblock)
- Barnidipina (HypoCa)
- Benidipina (Coniel)
- Efonidipina (Landel)
- Felodipina (Plendil)
- Isradipina (DynaCirc, Prescal)
- Klevidipina (Cleviprex)
- Lasidipina (Motens, Lacipil)
- Lerkanidipina (Zanidip)
- Manidipina (Calslot, Madipine)
- Nikardipina (Cardene, Carden SR)
- Nifedipina (Procardia, Adalat)
- Nilvadipina (Nivadil)
- Nimodipina (Nimotop) Bahan ini boleh melalui sempadan darah otak, dan digunakan untuk menghalang vasospasma serebrum.
- Nisoldipina (Baymycard, Sular, Syscor)
- Nitrendipina (Cardif, Nitrepin, Baylotensin)
- Pranidipina (Acalas)
- Silnidipina (Atelec, Cinalong, Siscard)
Bukan dihidropiridina[sunting | sunting sumber]
Fenilalkilamina[sunting | sunting sumber]

Penyekat saluran kalsium fenilalkilamina agak selektif terhadap miokardium, mengurangkan permintaan oksigen miokardium dan membalikkan vasospasma koronari, dan sering digunakan untuk merawat angina. Ia mempunyai kesan vasodilator yang minimum berbanding dengan dihidropiridina, dan oleh itu, kurang menyebabkan takikardia refleks, lalu menjadikannya pilihan untuk rawatan angina, di mana takikardia boleh menjadi penyumbang paling ketara kepada keperluan oksigen terhadap jantung. Oleh itu, kerana vasodilasi adalah minimum dengan fenilalkilamina, mekanisme utama tindakan menyebabkan inotropi negatif. Fenilalkilamina dianggap mengakses saluran kalsium dari sisi intrasel, walaupun buktinya agak bercampur.[10]
- Fendilina
- Gallopamil
- Verapamil (Calan, Isoptin)
Benzotiazepina[sunting | sunting sumber]

Penyekat saluran kalsium benzotiazepina tergolong dalam kelas sebatian benzotiazepina, dan merupakan kelas perantara antara fenilalkilamina dan dihidropiridina dalam selektiviti mereka terhadap saluran kalsium vaskular. Dengan kedua-dua kesan penenangan jantung dan tindakan vasodilator, benzotiazepina dapat mengurangkan tekanan arteri tanpa menghasilkan tahap rangsangan jantung refleks yang sama yang disebabkan oleh dihidropiridina.
- Diltiazem (Cardizem)
Tidak berpilih[sunting | sunting sumber]
Walaupun kebanyakan ejen yang disenaraikan di atas agak berpilih, terdapat ejen tambahan yang dianggap tidak selektif. Ini termasuk mibefradil, bepridil, flunarizina (merentas darah-otak), fluspirilena (merentas darah-otak)[11] dan fendilina.[12]
Lain-lain[sunting | sunting sumber]
Gabapentinoid seperti gabapentin dan pregabalin ialah penyekat terpilih saluran kalsium berpagar voltan dengan subunit α2δ. Ia digunakan terutamanya untuk merawat epilepsi dan sakit neuropatik. [perlu rujukan]
Zikonotida, sebatian peptida yang berasal daripada omega-konotoksin, ialah penyekat saluran kalsium jenis N terpilih yang mempunyai sifat analgesik dengan kekuatan bersamaan anggaran 1,000 kali ganda morfina. Ia mesti dihantar melalui laluan intratekal (terus ke dalam cecair serebrospinal) melalui pam infusi intratekal.[perlu rujukan]
Sebatian dan unsur semula jadi seperti magnesium juga telah terbukti bertindak sebagai penyekat saluran kalsium apabila diberikan melalui mulut.[13]
Kesan sampingan[sunting | sunting sumber]
Kesan sampingan ubat ini mungkin termasuk tetapi tidak terhad kepada:
- Sembelit
- Edema periferi yang boleh berlaku pada sebanyak 70% orang yang menerima penyekat saluran kalsium, disebabkan oleh penyekat saluran kalsium keutamaan arteriolar atau pelebaran prakapilari tanpa pelebaran yang setimpal dalam peredaran vena atau pascakapilari.[14][15][16][17][18] Memandangkan saliran limfa bergantung pada pengecutan otot licin di dalam salur limfa[19] yang disokong oleh saluran kalsium berpagaran voltan, perencatan saluran kalsium berpagar voltan menimbulkan ancaman ke arah penyingkiran cecair interstisial limfa yang penting untuk fungsi sistem limfa yang normal.[18]
- Pembesaran gingiva
Keracunan[sunting | sunting sumber]
Ketoksikan CCB ringan dirawat dengan penjagaan sokongan. CCB bukan dihidropiridina boleh menghasilkan keracunan yang mendalam, dan dekontaminasi awal, terutamanya untuk agen pelepasan perlahan, adalah penting. Dalam kes dos berlebihan teruk, rawatan biasanya termasuk pemantauan rapi tanda-tanda utama, dan penambahan agen vasopresif serta cecair intravena bagi sokongan tekanan darah. Kalsium glukonat intravena (atau kalsium klorida jika talian tengah tersedia) dan atropin ialah terapi baris pertama. Jika masa kes dos berlebihan diketahui dan ketampakan adalah dalam masa dua jam selepas pengambilan, bahan seperti arang aktif, pengurasan gastrik dan polietilena glikol boleh digunakan untuk menyahcemar usus. Usaha dekontaminasi usus boleh dilanjutkan kepada dalam masa 8 jam selepas pengambilan dengan persediaan pelepasan lanjutan.
Terapi hiperinsulinemia-euglisemia telah muncul sebagai satu bentuk rawatan yang berdaya maju.[20] Walaupun mekanismenya tidak jelas, peningkatan insulin boleh menggerakkan glukosa daripada tisu periferi untuk berfungsi sebagai sumber bahan api alternatif jantung (jantung bergantung terutamanya kepada pengoksidaan asid lemak). Rawatan teori dengan terapi emulsi lipid telah dipertimbangkan dalam kes yang teruk, tetapi belum lagi menjadi standard penjagaan.
Berhati-hati harus diambil apabila menggunakan verapamil dengan penyekat beta kerana risiko bradikardia yang teruk. Jika tidak berjaya, perentak ventrikel harus digunakan.[21]
Penghalang bukan perubatan[sunting | sunting sumber]
Etanol[sunting | sunting sumber]

Penyelidikan menunjukkan etanol terlibat dalam perencatan saluran kalsium jenis L. Satu kajian menunjukkan sifat pengikatan etanol kepada saluran kalsium jenis L adalah mengikut kinetik tertib pertama dengan pekali Hill sekitar 1. Ini menunjukkan etanol mengikat secara bebas ke saluran, menunjukkan pengikatan bukan kooperatif.[22] Kajian awal menunjukkan hubungan antara kalsium dan pembebasan vasopressin oleh sistem utusan sekunder.[23] Tahap vasopresin berkurang selepas pengambilan alkohol.[24] Tahap vasopressin yang lebih rendah daripada penggunaan alkohol telah dikaitkan dengan etanol yang bertindak sebagai antagonis kepada saluran kalsium berpagar voltan (VGCC). Kajian yang dijalankan oleh Treistman et al. dalam aplisia mengesahkan perencatan VGCC oleh etanol. Rakaman pengapit voltan telah dilakukan pada neuron aplisia. VGCC telah diasingkan dan arus kalsium direkodkan menggunakan teknik pengapit tampalan yang mempunyai etanol sebagai rawatan. Rakaman telah direplikasi pada kepekatan yang berbeza-beza (0, 10, 25, 50, dan 100 mM) pada pengapit voltan +30 mV. Keputusan menunjukkan arus kalsium menurun apabila kepekatan etanol meningkat.[25] Keputusan yang sama telah terbukti benar dalam rakaman saluran tunggal dari terminal saraf tikus terpencil yang sebenarnya dilakukan oleh etanol untuk menyekat VGCC.[26]
Kajian yang dilakukan oleh Katsura et al. pada tahun 2006 pada neuron korteks serebrum tikus menunjukkan kesan pendedahan etanol yang berpanjangan. Neuron didedahkan kepada kepekatan etanol berterusan sebanyak 50 mM selama 3 hari secara in vitro. Analisis blot Western dan analisis protein telah dijalankan untuk menentukan jumlah relatif ekspresi subunit VGCC. Subunit α1C, α1D, dan α2/δ1 menunjukkan peningkatan ekspresi selepas pendedahan etanol yang berterusan. Walau bagaimanapun, subunit β4 menunjukkan penurunan. Tambahan pula, subunit α1A, α1B, dan α1F tidak berubah dalam ungkapan relatifnya. Oleh itu, pendedahan etanol yang berterusan boleh mengambil bahagian dalam pembangunan kebergantungan etanol dalam neuron.[27]
Eksperimen lain yang dilakukan oleh Malysz et al. telah mengkaji kesan etanol pada saluran kalsium berpagar voltan pada sel otot licin detrusor dalam tikus belanda. Teknik pengapit tampalan berlubang digunakan dengan cecair intraselular di dalam pipet dan cecair ekstraselular di dalam tab mandi dengan tambahan 0.3% vol/vol (kira-kira 50-mM) etanol. Etanol menurunkan Ca2+ semasa dalam sel DSM dan kelonggaran otot yang disebabkan. Etanol menghalang VGCC dan terlibat dalam kelonggaran yang disebabkan oleh alkohol pada pundi kencing.[28]
Agatoksin bisa labah-labah[sunting | sunting sumber]
Penyelidikan mengenai labah-labah rumput padang pasir, Agelenopsis aperta , telah menunjukkan bahawa agatoksin IVA dan IVB yang terdapat dalam bisanya secara selektif menyekat saluran kalsium. Agatoksin ini juga terdapat dalam spesies labah-labah lain. Gigitan labah-labah rumput padang pasir terhadap serangga mengakibatkan lumpuh yang cepat, tetapi gigitan kepada manusia tidak dianggap kritikal dari segi perubatan.[29]
Mekanisme tindakan[sunting | sunting sumber]

Dalam tisu badan, kepekatan ion kalsium (Ca2+) sel luar biasanya kira-kira 10,000 kali ganda lebih tinggi daripada kepekatan di dalam sel. Membran dalam sesetengah sel ditanam dengan saluran kalsium. Apabila sel-sel ini menerima isyarat tertentu, saluran terbuka lalu membiarkan kalsium memasuki sel. Peningkatan yang terhasil dalam kalsium intraselular mempunyai kesan yang berbeza dalam pelbagai jenis sel. Penyekat saluran kalsium menghalang atau mengurangkan pembukaan saluran ini lalu mengurangkan kesan ini.[perlu rujukan]
Beberapa jenis saluran kalsium berlaku, dengan beberapa kelas penyekat, tetapi hampir kesemuanya secara berkeutamaan atau eksklusif menyekat saluran kalsium berpagaran voltan jenis L.[30]
Saluran kalsium yang bergantung kepada voltan bertanggungjawab untuk gandingan pengujaan-penguncupan otot rangka, licin dan jantung, dan untuk mengawal rembesan aldosteron dan kortisol dalam sel endokrin korteks adrenal.[5] Di jantung, ia juga terlibat dalam pengaliran isyarat perentak jantung. CCB yang digunakan sebagai ubat terutamanya mempunyai empat kesan:
- Dengan bertindak pada otot licin vaskular, ia mengurangkan pengecutan arteri dan menyebabkan peningkatan diameter arteri, fenomena yang dipanggil vasodilasi (CCB tidak berfungsi pada otot licin vena).
- Dengan bertindak pada otot jantung (miokardium), ia mengurangkan daya penguncupan jantung.
- Dengan memperlahankan pengaliran aktiviti elektrik di dalam jantung, ia memperlahankan degupan jantung.
- Dengan menyekat isyarat kalsium pada sel korteks adrenal, ia secara langsung mengurangkan pengeluaran aldosteron yang membawa kepada penurunan tekanan darah.
Oleh kerana tekanan darah berada dalam maklum balas intim dengan keluaran jantung dan rintangan periferi, dengan tekanan darah yang agak rendah, beban selepas pada jantung berkurangan; ini mengurangkan betapa kerasnya jantung mesti bekerja untuk mengeluarkan darah ke dalam aorta, menjadikan jumlah oksigen yang diperlukan oleh jantung berkurangan dengan sewajarnya. Ini boleh membantu mengurangkan gejala penyakit jantung iskemik seperti angina pektoris.
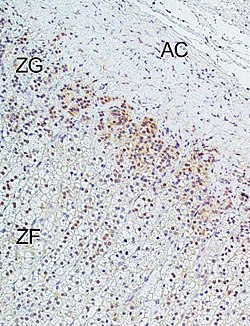
Mengurangkan daya penguncupan miokardium dikenali sebagai kesan inotropik negatif penyekat saluran kalsium.
Tindakan memperlahankan pengaliran aktiviti elektrik dalam jantung dengan menyekat saluran kalsium semasa fasa dataran tinggi potensi tindakan jantung mengakibatkan kesan kronotropik negatif atau menurunkan kadar denyutan jantung. Ini boleh meningkatkan potensi untuk blok jantung. Kesan kronotropik negatif CCB menjadikannya kelas ejen yang biasa digunakan dalam individu yang mengalami fibrilasi atrium atau getaran, di mana kawalan kadar denyutan jantung secara amnya ialah matlamat rawatan. Kronotropi negatif boleh memberi manfaat dalam rawatan pelbagai proses penyakit kerana kadar denyutan jantung yang lebih rendah mewakili keperluan oksigen jantung yang lebih rendah. Kadar denyutan jantung yang tinggi boleh mengakibatkan "kerja jantung" yang lebih tinggi dengan ketara, dan boleh mengakibatkan gejala angina.
Kelas dihidropiridina secara utamanya mempengaruhi otot licin vaskular arteri dan menurunkan tekanan darah dengan menyebabkan vasodilatasi. Kelas fenilalkilamina pula memberi kesan kepada sel-sel jantung, dan mempunyai kesan inotropik dan negatif kronotropik negatif. Kelas benzotiazepina CCB menggabungkan kesan dua kelas yang lain.
Kerana kesan inotropik negatif, penyekat saluran kalsium nondihidropiridina harus dielakkan (atau digunakan dengan berhati-hati) pada individu dengan kardiomiopati.[31]
Tidak seperti penghalang beta, penyekat saluran kalsium tidak mengurangkan tindak balas jantung terhadap input daripada sistem saraf simpatetik. Memandangkan peraturan tekanan darah dari detik ke detik dijalankan oleh sistem saraf simpatetik (melalui refleks baroreseptor), penyekat saluran kalsium membolehkan tekanan darah dikekalkan dengan lebih berkesan daripada penyekat beta. Walau bagaimanapun, oleh kerana jenis dihidropiridina mengakibatkan penurunan tekanan darah, refleks baroreseptor sering memulakan peningkatan refleks dalam aktiviti bersimpati yang membawa kepada peningkatan kadar denyutan jantung dan pengecutan.
Kalsium ion diserang oleh ion magnesium dalam sistem saraf. Oleh sebab itu, suplemen magnesium yang tersedia biologikal, mungkin termasuk magnesium klorida, magnesium laktat dan magnesium aspartat boleh meningkatkan atau meningkatkan kesan sekatan saluran kalsium.[32]
Saluran kalsium jenis N terdapat dalam neuron dan terlibat dalam pembebasan neurotransmiter pada sinaps. Zikonotida ialah penyekat terpilih saluran kalsium ini, dan bertindak sebagai analgesik.
Sejarah[sunting | sunting sumber]
Penyekat saluran kalsium mula digunakan secara meluas pada tahun 1960-an, [33] pertama kali dikenal pasti di makmal ahli farmakologi Jerman Albrecht Fleckenstein pada tahun 1964. [34]
Rujukan[sunting | sunting sumber]
- ^ Tfelt-Hansen, P; Tfelt-Hansen, J (2009). "Verapamil for cluster headache. Clinical pharmacology and possible mode of action". Headache: The Journal of Head and Face Pain. 49 (1): 117–25. doi:10.1111/j.1526-4610.2008.01298.x. PMID 19125880.
- ^ Olson, Kent (2011). "40. Calcium Channel Antagonists". Poisoning & drug overdose (ed. 6th). McGraw-Hill Medical. ISBN 978-0-07-166833-0.
- ^ calcium channel blocker di Kamus Perubatan Dorland
- ^ Nelson M (2010). "Drug treatment of elevated blood pressure". Australian Prescriber. 33 (4): 108–12. doi:10.18773/austprescr.2010.055.
- ^ a b c "Voltage-gated calcium channels in the human adrenal and primary aldosteronism". J Steroid Biochem Mol Biol. 144 (part B): 410–16. 2014. doi:10.1016/j.jsbmb.2014.08.012. PMID 25151951.
- ^ "Calcium channel blockers versus other classes of drugs for hypertension". Cochrane Database of Systematic Reviews. 8 (8): CD003654. 2010. doi:10.1002/14651858.CD003654.pub4. PMID 20687074.
- ^ "Calcium Channel Blockers". MedicineNet. m/s. 2. Diarkibkan daripada yang asal pada 2012-04-21. Dicapai pada 2013-01-19.
- ^ Norman M Kaplan, MD; Burton D Rose, MD (Apr 3, 2000). "Major side effects and safety of calcium channel blockers". Chinese Medical & Biological Information. Diarkibkan daripada yang asal pada December 30, 2011. Dicapai pada July 23, 2012.
- ^ "Clinical Practice. Nephropathy in Patients with Type 2 Diabetes". New England Journal of Medicine. 346 (15): 1145–51. 2002. doi:10.1056/NEJMcp011773. PMID 11948275.
- ^ Hockerman, G.H.; Peterson, B.Z.; Johnson, B.D.; Catterall, W.A. (1997). "Molecular Determinants of Drug Binding and Action on L-Type Calcium Channels". Annual Review of Pharmacology and Toxicology. 37: 361–96. doi:10.1146/annurev.pharmtox.37.1.361. PMID 9131258.
- ^ "Voltage-Dependent Blockade of Diverse Types of Voltage-Gated Ca2+ Channels Expressed in Xenopus Oocytes by the Ca2+ Channel Antagonist Mibefradil (Ro 40-5967)". Molecular Pharmacology. 48 (3): 540–49. 1995. PMID 7565636.
- ^ "Effect of Ca2+ Antagonists on Isolated Rabbit Detrusor Muscle". Acta Physiologica Hungarica. 77 (3–4): 269–78. 1991. PMID 1755331.
- ^ Houston, M. (2011). "The role of magnesium in hypertension and cardiovascular disease". Journal of Clinical Hypertension (Greenwich, Conn.). 13 (11): 843–847. doi:10.1111/j.1751-7176.2011.00538.x. PMC 8108907. PMID 22051430.
- ^ Sica, Domenic A. (2003). "Calcium Channel Blocker‐Related Peripheral Edema: Can It Be Resolved?". The Journal of Clinical Hypertension. Wiley. 5 (4): 291–295. doi:10.1111/j.1524-6175.2003.02402.x. ISSN 1524-6175. PMC 8099365. PMID 12939574.
- ^ "Calcium-Channel Blockers (CCBs)". CV Pharmacology. Dicapai pada 2020-02-07.
- ^ Domenic A. Sica. "Calcium Channel Blocker-Related Peripheral Edema". Medscape. Dicapai pada 2019-10-26.
- ^ Matthew R. Weir. "Incidence of Pedal Edema Formation With Dihydropyridine Calcium". Medscape. Dicapai pada 2019-10-26.
- ^ a b Mohanakumar, Sheyanth; Telinius, Niklas; Kelly, Benjamin; Hjortdal, Vibeke (2019-08-20). "Reduced Lymphatic Function Predisposes to Calcium Channel Blocker Edema: A Randomized Placebo-Controlled Clinical Trial". Lymphatic Research and Biology. Mary Ann Liebert Inc. 18 (2): 156–165. doi:10.1089/lrb.2019.0028. ISSN 1539-6851. PMID 31429625.
- ^ Babak Mehrara. John F Eidt; Joseph L Mills Sr; Harold J Burstein; Kathryn A Collins (penyunting). "Clinical features and diagnosis of peripheral lymphedema". UpToDate. Dicapai pada 2019-10-27.
- ^ Engebretsen, Kristin M.; Kaczmarek, Kathleen M.; Morgan, Jenifer; Holger, Joel S. (2011). "High-dose insulin therapy in beta-blocker and calcium channel-blocker poisoning". Clinical Toxicology. 49 (4): 277–283. doi:10.3109/15563650.2011.582471. ISSN 1556-9519. PMID 21563902.
- ^ "Calcium Channel Blockers". Medicine. 35 (11): 599–602. 2007. doi:10.1016/j.mpmed.2007.08.025.
- ^ "Ethanol directly modulates gating of a dihydropyridine-sensitive Ca2+ channel in neurohypophysial terminals". J. Neurosci. 14 (9): 5453–60. September 1994. doi:10.1523/JNEUROSCI.14-09-05453.1994. PMC 6577079. PMID 7521910.
- ^ "The involvement of actin, calcium channels and exocytosis proteins in somato-dendritic oxytocin and vasopressin release". Front Physiol. 3: 261. 2012. doi:10.3389/fphys.2012.00261. PMC 3429037. PMID 22934017.
- ^ "Inhibitory effect of ethanol on the arginine vasopressin response to insulin-induced hypoglycemia and the role of endogenous opioids". Neuroendocrinology. 51 (5): 501–04. May 1990. doi:10.1159/000125383. PMID 2112727.
- ^ "Effects of ethanol on calcium channels, potassium channels, and vasopressin release". Ann. N. Y. Acad. Sci. 625 (1): 249–63. 1991. Bibcode:1991NYASA.625..249T. doi:10.1111/j.1749-6632.1991.tb33844.x. PMID 1647726.
- ^ "Regulation of neuronal voltage-gated calcium channels by ethanol". Neurochem. Int. 35 (2): 95–101. August 1999. doi:10.1016/s0197-0186(99)00050-9. PMID 10405992.
- ^ "Increase in expression of α1 and α2/δ1 subunits of L-type high voltage-gated calcium channels after sustained ethanol exposure in cerebral cortical neurons". J. Pharmacol. Sci. 102 (2): 221–30. October 2006. doi:10.1254/jphs.fp0060781. PMID 17031067.
- ^ "Ethanol-mediated relaxation of guinea pig urinary bladder smooth muscle: involvement of BK and L-type Ca2+ channels". Am. J. Physiol., Cell Physiol. 306 (1): C45–58. January 2014. doi:10.1152/ajpcell.00047.2013. PMC 3919972. PMID 24153429.
- ^ Adams, Michael E. (April 2004). "Agatoxins: ion channel specific toxins from the american funnel web spider, Agelenopsis aperta". Toxicon. 43 (5): 509–525. doi:10.1016/j.toxicon.2004.02.004. ISSN 0041-0101. PMID 15066410.
- ^ Yousef (2005). "The mechanism of action of calcium channel blockers in the treatment of diabetic nephropathy" (PDF). Int J Diabetes & Metabolism. 13 (2): 76–82. doi:10.1159/000497574. Diarkibkan daripada yang asal (PDF) pada 2015-10-10. Dicapai pada 2013-06-29. Unknown parameter
|displayauthors=ignored (bantuan) - ^ Lehne R (2010). Pharmacology for Nursing Care (ed. 7th). St. Louis, Missouri: Saunders Elsevier. m/s. 505. ISBN 978-1-4160-6249-3.
- ^ "Magnesium: Nature's Physiologic Calcium Blocker". American Heart Journal. 108 (1): 188–93. 1984. doi:10.1016/0002-8703(84)90572-6. PMID 6375330.
- ^ Tekol, Y. (2007). "The medieval physician Avicenna used an herbal calcium channel blocker, Taxus baccata L". Phytotherapy Research. 21 (7): 701–02. doi:10.1002/ptr.2173. PMID 17533639.
- ^ Fleckenstein, A. (1983). "History of calcium antagonists". Circulation Research. 52 (2 Pt 2): 13–16. PMID 6339106.
