Kalsium klorida

| |
| |
| Nama | |
|---|---|
| Nama IUPAC
Kalsium klorida
(Calcium chloride) | |
| Nama lain
Kalsium(II) klorida,
Kalsium diklorida, E509 | |
| Sifat | |
| CaCl2 | |
| Jisim molar | 110.98 g/mol (kontang) 128.999 g/mol (monohidrat) 147.014 g/mol (dihidrat) 183.045 g/mol (tetrahidrat) 219.08 g/mol (heksahidrat) |
| Rupa bentuk | hablur putih higroskopik |
| Bau | tidak berbau |
| Ketumpatan | 2.15 g/cm3 (kontang) 1.835 g/cm3 (dihidrat) 1.83 g/cm3 (tetrahidrat) 1.71 g/cm3 (heksahidrat) |
| Takat lebur | 772 °C (kontang) 260 °C (monohidrat) 176 °C (dihidrat) 45.5 °C (tetrahidrat) 30 °C (heksahidrat)[1] |
| Takat didih | 1935 °C (kontang) |
| 74.5 g/100mL (20 °C) 59.5 g/100 mL (0 °C) | |
| Keterlarutan | larut dalam aseton, asid asetik |
| Keasidan (pKa) | 8–9 (kontang) 6.5–8.0 (heksahidrat) |
Indeks biasan (nD)
|
1.52 |
| Struktur | |
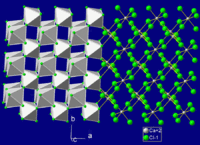
| Struktur kristal | Ortorombik (rutil ternyahbentuk), oP6 trigon (heksahidrat) |
| Kumpulan ruang | Pnnm, No. 58 |
| Geometri koordinasi |
oktahedral, 6-koordinat |
| Bahaya | |
| Piktogram GHS | 
|
| H319, H316, H302 | |
| P264, P280, P270, P305+351+338, P337+313, P301+312, P330, P501 | |
| NFPA 704 (berlian api) | |
| Dos maut (LD) atau kepekatan dos maut (LC) | |
LD50 (median dos)
|
1000 mg/kg (ditelan, tikus) |
| Sebatian berkaitan | |
Anion lain
|
kalsium florida kalsium bromida kalsium iodida |
Kation lain
|
berilium klorida magnesium klorida strontium klorida barium klorida radium klorida |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| | |
| Rujukan kotak info | |
Kalsium klorida,(Tulisan Jawi:كالسيوم كلوريدا) garam kalsium dan klorin. Ia bersifat seperti halida ion yang biasa dan berada dalam keadaan pepejal dalam suhu bilik. Antara kegunaan biasa bagi kalsium klorida ialah sebagai air garam bagi loji penyejukan, kawaan ais dan habuk di jalan-jalan, dan bagi tujuan pengeringan. Disebabkan sifatnya yang higroskopik (mudah menyerap lembapan di udara), kalsium klorida kontang perlu disimpan di dalam bekas-bekas kedap udara yang ditutup rapat.
Sifat[sunting | sunting sumber]
Kalsium klorida boleh berfungsi sebagai sumber ion kalsium dalam larutan akua kerana sifat kalsium klorida yang boleh larut dalam air. Sifat ini berguna untuk mengeluarkan ion daripada larutan. Contohnya, fosfat dikeluarkan daripada larutan oleh kalsium:
- 3 CaCl2 (ak) + 2 K3PO4 (ak) → Ca3(PO4)2 (p) + 6 KCl (ak)
Kalsium klorida lebur boleh dielektrolisis untuk mendapatkan logam kalsium dan gas klorin:
- CaCl2 (c) → Ca (p) + Cl2 (g)
Kalsium karbonat memiliki perubahan entalpi larutan yang sangat tinggi. Penguraiannya dalam air biasanya disertai kenaikan haba yang agak tinggi.
Garam kontang sebatian ini bersifat lembap cair; ia boleh mengumpul jumlah air yang cukup banyak di dalam kekisi kristalnya untuk menghasilkan larutan.
Penyediaan[sunting | sunting sumber]
Kalsium klorida boleh dihasilkan secara terus daripada batu kapur, tetapi sejumlah besar turut dihasilkan sebagai bahan sampingan proses Solvay. Penggunaan bahan ini di Amerika Utara pada tahun 2002 adalah sebanyak 1,687,000 tan (3.7 bilion paun). Kilang penghasilan milik Dow Chemical Factory di Michigan mengeluarkan kira-kira 35% pengeluaran keseluruhan kalsium klorida Amerika Syarikat.
Kejadian secara semula jadi[sunting | sunting sumber]
Kalsium klorida terbentuk secara semula jadi dalam bentuk mineral-mineral evaporit, sinjarit (dihidrat) dan antartisit (heksahidrat). Mineral lain yang berkaitan, klorokalsit (kalium kalsium klorida, KCaCl3) juga sangat jarang.
Kegunaan[sunting | sunting sumber]
Pengering[sunting | sunting sumber]
Tiub pengering selalunya dipenuhi dengan kalsium klorida. Kelp dikeringkan dengan kalsium klorida untuk menghasilkan natrium karbonat. Penambahan kalsium klorida pepejal ke dalam cecair boleh mengeluarkan air yang terlarut. Kalsium klorida kontang telah disahkan oleh FDA sebagai alat bantu pembungkusan untuk memastikan kekeringan bahan yang dibungkus (CPG 7117.02).
Sifat higroskopik ini juga digunakan untuk mengekalkan satu lapisan cecair di atas permukaan jalan raya untuk memerangkap habuk.
Nyahais dan penurunan tahap beku[sunting | sunting sumber]
Dengan menurunkan tahap beku air, kalsium klorida digunakan untuk menghalang pembentukan ais dan untuk menyahais. Ini sangat berguna bagi permukaan jalan. Penguraian kalsium klorida bersifat eksotermik (melepaskan haba), dan sebatian ini agak tidak merbahaya kepada tumbuhan dan tanih; namun, pemerhatian terkini di negeri Washington menunjukkan bahawa ia mungkin berbahaya bagi tumbuh-tumbuhan malar hijau di tepi jalan. Kalsium klorida juga lebih berkesan pada suhu yang lebih rendah berbanding natrium klorida. Apabila diedarkan untuk kegunaan, kalsium klorida biasanya berbentuk bebola kecil berwarna putih berdiameter beberapa milimeter. Larutan kalsium klorida boleh menghalang pembekuan pada suhu serendah −52 °C (−62 °F).
Sumber ion kalsium[sunting | sunting sumber]
Kalsium klorida digunakan untuk meningkatkan keliatan air dalam kolam renang. Ini mengurangkan hakisan konkrit kolam tersebut. Berdasarkan prinsip Le Chatelier dan kesan ion serupa, dengan meningkatkan penumpuan kalsium dalam air, penguraian sebatian kalsium dalam struktur konkrit dapat dikurangkan.
Dalam akuarium marin, kalsium klorida ditambah untuk menyediakan kalsium bagi haiwan-haiwan bercangkerang kalsium karbonat seperti moluska dan knidaria. Kalsium hidroksida atau reaktor kalsium juga boleh digunakan untuk menyediakan kalsium, namun penambahan kalsium klorida ialah cara yang paling pantas dan tidak memberi kesan yang besar terhadap paras pH.
Makanan[sunting | sunting sumber]
Sebagai bahan masakan, kalsium klorida dikelaskan di dalam Kesatuan Eropah sebagai bahan tambahan makanan yang dibenarkan untuk digunakan sebagai sekuestran dan agen pengental dengan nombor E E509. Ia dianggap sebagai "diiktiraf selamat secara umum (GRAS)" oleh Pentadbiran Makanan dan Ubat-ubatan A.S. dan juga terdapat di dalam Senarai Bahan-bahan yang Dibenarkan dan Diharamkan Kebangsaan Program Organik Kebangsaan A.S.. Pengambilan purata kalsium klorida sebagai bahan tambahan makanan dianggarkan sekitar 160 hingga 345 mg/hari bagi setiap individu.
Sebagai agen pengental, kalsium klorida digunakan dalam sayur tin, dalam penghasilan tauhu daripada kacang soya dan dalam pembuatan pengganti kaviar daripada jus buah-buahan atau sayur-sayuran. Ia biasanya digunakan sebagai elektrolit dalam minuman tenaga dan minuman-minuman lain termasuklah air botol. Rasa kalsium klorida yang sangat masam digunakan untuk membuat jeruk sementara tidak meningkatkan kandungan natriumnya. Sifat menurunkan tahap beku yang dimiliki kalsium klorida digunakan untuk memperlahankan pembekuan karamel di dalam bar coklat berisi karamel.
Dalam proses pembruan bir, kalsium klorida kadang kala digunakan untuk membetulkan kekurangan mineral dalam air bruan. Ia memberi kesan dan tindak balas kimia sewaktu proses pembruan, dan boleh juga memberi kesan kepada fungsi yis sewaktu penapaian. Kalsium klorida kadang kala ditambah dalam susu yang diproses untuk mengembalikan keseimbangan semulajadi antara kalsium dan protin dalam kasein bagi tujuan penghasilan keju seperti Brie, Pélardon dan Stilton. Ia juga kerap ditambah pada epal yang dipotong untuk mengekalkan tekstur.
Ubat-ubatan[sunting | sunting sumber]
CaCl2 boleh digunakan untuk merawat keracunan magnesium. Suntikan kalsium klorida boleh melawan keracunan kardiak seperti yang diukur oleh elektrokardiogram. Ia boleh membantu melindungi miokardium daripada paras kalium serum yang terlalu tinggi dalam hiperkalemia. Kalsium klorida boleh digunakan untuk merawat keracunan penghalang saluran kalsium dengan pantas, daripada kesan sampingan ubat-ubatan seperti diltiazem (Cardizem), lantas mengelakkan kemungkinan serangan jantung.[2]
Kalsium klorida akueus digunakan dalam transformasi genetik sel-sel dengan meningkatkan ketelapan membran sel, lalu mencetuskan kecekapan bagi pengambilan DNA (membenarkan cebisan DNA memasuki sel dengan lebih mudah).
Ada beberapa kesan sampingan akibat pengambilan kalsium klorida dengan cara menelan atau secara intravena dan seseorang tidak disarankan mengambil kalsium klorida sekiranya dia mengalami sebarang masalah berikut:
- alergik (hipersensitif) terhadap garam kalsium
- mengambil sebarang ubat-ubatan bagi masalah jantung (misalnya digitalis)
- mempunyai paras kalsium rendah akibat masalah ginjal
- mempunyai terlalu banyak kalsium sama ada dalam darah atau urin
- mempunyai masalah pernafasan
Seseorang perlu lebih berjaga-jaga jika menggunakan Infusi Intravena Kalsium Klorida sekiranya dia:
- mengalami masalah ginjal
- mengalami masalah jantung
- mengalami gangguan radang yang dikenali sebagai sarkoidosis[3]
Lihat juga[sunting | sunting sumber]
Rujukan[sunting | sunting sumber]
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ^
"Calcium chloride Prescribing Information". Hospira, Inc. 2009. Dicapai pada 10 Jun 2011. Unknown parameter
|month=ignored (bantuan) - ^ http://www.drugs.com/pro/calcium-chloride.html | title = Calcium Chloride Intravenous Infusion
Pautan luar[sunting | sunting sumber]
 Media berkenaan Kalsium klorida di Wikimedia Commons
Media berkenaan Kalsium klorida di Wikimedia Commons

