L-DOPA
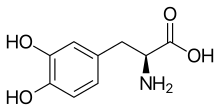 Formula rangka L-DOPA | |
 | |
| Data klinikal | |
|---|---|
| Sebutan | /ˌɛlˈdoʊpə/, /ˌlɛvoʊˈdoʊpə/ |
| Nama dagang | Larodopa, Dopar, Inbrija, lain-lain |
| AHFS/Drugs.com | Professional Drug Facts |
| MedlinePlus | a619018 |
| Data lesen | |
| Kategori kehamilan |
|
| Kaedah pemberian | Mulut, intravena |
| Kod ATC | |
| Status perundangan | |
| Status perundangan | |
| Data farmakokinetik | |
| Bioketersediaan | 30% |
| Metabolisme | Dekarboksilase asid l-amino aromatik |
| Penyingkiran separuh hayat | 0.75–1.5 jam |
| Perkumuhan | Buah pinggang: 70–80% |
| Pengecam | |
| |
| Nombor CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.000.405 |
| Data kimia dan fizikal | |
| Formula | C9H11NO4 |
| Jisim molar | 197.19 g·mol−1 |
| Model 3D (JSmol) | |
| |
| |
| (verify) | |
l-DOPA, juga dikenali sebagai levodopa dan l-3,4-dihidroksifenilalanina, ialah asid amino yang dibuat dan digunakan sebagai sebahagian daripada tindakan biologi normal sesetengah tumbuhan[3] dan haiwan, termasuk manusia. Manusia, serta sebahagian daripada haiwan lain yang memanfaatkan l-DOPA, menjadikannya melalui biosintesis daripada asid amino l-tirosina. l-DOPA ialah pelopor kepada neurotransmiter dopamina, norepinefrina (noradrenalina) dan epinefrina (adrenalina), yang secara kolektif dikenali sebagai katekolamina. Tambahan pula, l-DOPA sendiri mengantara pembebasan faktor neurotropik oleh otak dan sistem saraf pusat.[4][5] l-DOPA boleh dihasilkan dan dalam bentuk tulennya dijual sebagai ubat psikoaktif dengan nama levodopa; nama dagangan yang dipakai termasuk Sinemet, Pharmacopa, Atamet, dan Stalevo. Sebagai ubat, ia digunakan dalam rawatan klinikal penyakit Parkinson dan distonia responsif dopamina.
Penggunaan perubatan[sunting | sunting sumber]
l-DOPA melintasi sempadan darah-otak yang tidak dapat dilintasi dopamina.[6] Dengan itu, l-DOPA digunakan untuk meningkatkan dopamina dalam rawatan penyakit Parkinson, Parkinsonisme, distonia responsif dopamina dan sindrom Parkinson-plus. Keberkesanan terapeutik adalah berbeza bagi aneka jenis gejala. Bradikinesia dan ketegaran merupakan gejala paling responsif manakala getaran kurang bertindak balas terhadap levodopa. Pertuturan, gangguan telan, ketidakstabilan postur dan kekakuan ialah simptom yang paling sedikit terkesan.[7]
Ketika l-DOPA telah memasuki sistem saraf pusat, ia ditukar kepada dopamina oleh enzim dekarboksilase asid l-amino aromatik, juga dikenali sebagai DOPA dekarboksilase. Piridoksal fosfat (vitamin B6) ialah kofaktor yang diperlukan dalam tindak balas ini, dan kadangkala boleh diberikan bersama dengan l-DOPA, biasanya dalam bentuk piridoksina. Oleh kerana levodopa memintas enzim tirosina hidroksilase, langkah pengehad kadar sintesis dopamina, ia lebih mudah ditukar kepada dopamina berbanding tirosina yang biasanya merupakan pendahulu semula jadi dalam pengeluaran dopamina.
Pada manusia, penukaran daripada l-DOPA kepada dopamin bukan sahaja berlaku dalam sistem saraf pusat. Sel-sel dalam sistem saraf tepian juga melakukan tugas yang sama. Justeru, pemberian l-DOPA sahaja akan membawa kepada peningkatan isyarat dopamina di sistem tepian juga. Isyarat dopamina tepian yang berlebihan adalah tidak diingini kerana ia menyebabkan banyak kesan sampingan yang buruk yang dilihat dengan pentadbiran L-DOPA tunggal. Untuk memintas kesan ini, l-DOPA ditadbir bersama dengan perencat dekarboksilase DOPA tepian (DDCI) seperti karbidopa (sama ada secara tunggal atau digabungkan dengan l-DOPA, dijenamakan sebagai Lodosyn[8] (Aton Pharma)[9] Sinemet (Merck Sharp & Dohme Limited), Pharmacopa (Jazz Pharmaceuticals), Atamet (UCB), Syndopa dan Stalevo (Orion Corporation) atau dengan benserazida (ubat campuran berjenama Madopar atau Prolopa) untuk menghalang sintesis tepian dopamina daripada l-DOPA). Walau bagaimanapun, apabila dimakan sebagai ekstrak botani, contohnya daripada suplemen M. pruriens, perencat dekarboksilase DOPA periferi tidak hadir.[3]
Inbrija (sebelum ini dikenali sebagai CVT-301) ialah formulasi serbuk penyedutan levodopa yang ditunjukkan untuk rawatan seketika "luar episod" pada pesakit penyakit Parkinson yang sedang mengambil karbidopa/levodopa.[10] Ia telah diluluskan oleh Pentadbiran Makanan dan Dadah Amerika Syarikat pada 21 Disember 2018, dan dipasarkan oleh Acorda Therapeutics.[11]
Pemberian bersama piridoksina tanpa DDCI mempercepatkan dekarboksilasi periferi l-DOPA sehinggakan ia menafikan kesan pemberian l-DOPA, fenomena yang secara sejarah menyebabkan kekeliruan besar.
Di samping itu, l-DOPA yang diberi bersama dengan DDCI tepian dalah berkesan bagi rawatan jangka pendek resah kaki.[12]
Dua jenis tindak balas yang dilihat dalam pemberian l-DOPA ialah:
- Tindak balas jangka pendek berkaitan dengan separuh hayat ubat.
- Tindak balas jangka masa yang lebih panjang bergantung pada pengumpulan kesan selama sekurang-kurangnya dua minggu, di mana ΔFosB terkumpul dalam neuron nigrostriatum. Dalam rawatan penyakit Parkinson, tindak balas ini terbukti hanya dalam terapi awal, kerana ketidakupayaan otak untuk menyimpan dopamina masih belum menjadi kebimbangan.
Peranan biologi[sunting | sunting sumber]
l-DOPA dihasilkan daripada asid amino l-tirosina oleh enzim tirosina hidroksilase. l-DOPA boleh bertindak sebagai mimetik l-tirosina dan boleh dipakai dalam protein oleh sel mamalia sebagai gantian L-tirosina, menghasilkan protein kalis protease dan terdedah kepada pengagregatan protein secara in vitro, dan mungkin membawa kepada keracunan saraf berkaitan pemberian l-DOPA kronik.[16] Ia juga merupakan molekul pendahulu bagi neurotransmiter monoamina atau katekolamina: dopamina, norepinefrina (noradrenalina) dan epinefrina (adrenalina). Dopamina terbentuk melalui penyahkarboksilan l-DOPA oleh dekarboksilase asid l-amino aromatik (AADC).
l-DOPA boleh dimetabolismekan secara terus oleh katekol-O-metil transferase menjadi 3-O-metildopa, dan kemudiannya menjadi asid vanilaktik. Laluan metabolisme ini tidak ada dalam badan lazim yang sihat, tetapi menjadi pentik selepas pemberian l-DOPA tepian dalam kalangan pesakit Parkinson atau bagi pesakit masalah langka kekurangan enzim AADC.[17]
l-Fenilalanina, l-tirosina dan l-DOPA ialah pendahulu kepada pigmen biologi, melanin. Enzim tirosinase memangkinkan pengoksidaan l-DOPA menjadi molekul perantara aktif dopakuinon yang bertindak balas secara lanjut menjadi oligomer melanin. Di samping itu, tirosinase boleh menukarkan tirosina terus menjadi l-DOPA dengan kehadiran agen penurunan seperti asid askorbik.[18]
Lekatan marin[sunting | sunting sumber]
l-DOPA ialah sebatian penting dalam pembentukan protein lekatan marin seperti dalam kupang.[19][20] Ia dipercayai bertanggungjawab bagi sifat kalis air dan pemulihan pantas protein-protein ini. l-DOPA juga boleh digunakan untuk menghalang permukaan daripada rosak dengan mengikat polimer antikotoran terhadap substrat disyaki.[21] Sifat kimia L-DOPA yang pelbagai boleh diguna pakai dalam nanoteknologi.[22] Sebagai contoh, peptida pasang sendiri dengan DOPA diketahui membentuk struktur nano berfungsi, termasuk gel dan bahan lekat.[23][24][25][26]
Kesan sampingan dan buruk[sunting | sunting sumber]
Kesan sampingan l-DOPA mungkin termasuk:
- Hipertensi, terutamanya jika dosnya terlalu tinggi
- Aritmia, walaupun ini jarang berlaku
- Mual, yang sering dikurangkan dengan mengambil ubat dengan makanan, walaupun protein mengurangkan penyerapan ubat. l-DOPA ialah asid amino, jadi protein menghalang serapan l-DOPA secara persaaingan.
- Pendarahan gastrousus
- Pernafasan terganggu, tidak selalunya berbahaya, dan sebenarnya boleh memberi manfaat kepada pesakit yang mengalami halangan saluran pernafasan atas
- Keguguran rambut
- Kekeliruan
- Keadaan emosi yang melampau, terutamanya resah, tetapi juga libido yang berlebihan
- Mimpi ketara atau insomnia
- Halusinasi pendengaran atau visual
- Kesan ke atas pembelajaran; beberapa bukti menunjukkan ia meningkatkan memori kerja, sambil menjejaskan fungsi kompleks lain
- Mengantuk dan narkolepsi
- Keadaan yang serupa dengan psikosis perangsang
Walaupun banyak kesan buruk dikaitkan dengan l-DOPA, khususnya secara psikiatri, ia mempunyai kurang daripada agen anti-Parkinson yang lain, seperti antikolinergik dan agonis reseptor dopamina.
Kesan lebih serius wujud dalam pemberian kronik l-DOPA dalam rawatan penyakit Parkinson, termasuk:
- Kemerosotan fungsi akhir dos
- Ayunan "hidup-mati".
- Pembekuan semasa pergerakan
- Kegagalan dos (rintangan dadah)
- Doskinesia pada dos puncak (diskinesia akibat levodopa)
- Kemungkinan disregulasi dopamina: Penggunaan jangka panjang l-DOPA dalam penyakit Parkinson telah dikaitkan dengan apa yang dipanggil sindrom disregulasi dopamina.[27]
Pakar klinik cuba mengelakkan kesan sampingan dan reaksi buruk ini dengan mengehadkan l-DOPA dos sebanyak mungkin sehingga benar-benar diperlukan.
Penggunaan jangka panjang L-DOPA meningkatkan tekanan oksidatif melalui monoamina oksidase yang menyebabkan degradasi enzimatik dopamin tersintesis, menyebabkan kerosakan neuron dan sitotoksisiti. Tekanan oksidatif disebabkan oleh pembentukan spesies oksigen reaktif (H2O2) semasa metabolisme dopamin yang diterajui oleh monoamina oksidase. Ia diteruskan lagi oleh kekayaan ion Fe2+ dalam striatum melalui tindak balas Fenton dan autooksidasi intrasel. Peningkatan pengoksidaan berpotensi menyebabkan mutasi dalam DNA disebabkan oleh pembentukan 8-oksoguanina yang berupaya berpasangan secara salah dengan adenina semasa mitosis.[28]
Sejarah[sunting | sunting sumber]
Dalam kerja yang memberikannya Hadiah Nobel pada 2000, saintis Sweden Arvid Carlsson pertama kali menunjukkan pada tahun 1950-an bahawa pemberian l-DOPA kepada haiwan dengan gejala Parkinson akibat dadah (reserpina) menyebabkan pengurangan keamatan gejala haiwan itu. Pada 1960-61, selepas menemui tahap dopamina yang sangat berkurangan dalam otak yang dibedah siasat pesakit dengan penyakit Parkinson, [29] Oleh Hornykiewicz bersama-sama pakar neurologi Walther Birkmayer menerbitkan tulisan kesan anti-Parkinson terapeutik dramatik bagi l-DOPA pemberian intravena yang pada pesakit. [30] Rawatan ini kemudiannya diperluaskan kepada keracunan mangan dan kemudiannya Parkinsonisme oleh George Cotzias dan rakan sekerjanya[31] yang menggunakan dos oral yang besar, dan memenangi Hadiah Lasker 1969.[32][33] Pakar neurologi Oliver Sacks menerangkan rawatan ini pada pesakit manusia dengan ensefalitis letargika dalam bukunya Awakenings pada 1973, dan didukung oleh filem 1990 dengan nama yang sama. Kajian pertama yang melaporkan peningkatan pada pesakit dengan penyakit Parkinson akibat rawatan dengan L-DOPA telah diterbitkan pada 1968.[34]
Hadiah Nobel Kimia 2001 juga berkaitan dengan l-DOPA: Jawatankuasa Nobel menganugerahkan satu perempat hadiah kepada William S. Knowles bagi kerjanya mengenai tindak balas penghidrogenan dimangkin kiral, dengan contoh paling ketara ialah sintesis l-DOPA.[35][36][37]
Rujukan[sunting | sunting sumber]
- ^ Howard ST, Hursthouse MB, Lehmann CW, Poyner EA (1995). "Experimental and theoretical determination of electronic properties in Ldopa". Acta Crystallogr. B. 51: 328–337. doi:10.1107/S0108768194011407.
- ^ a b "Levodopa Use During Pregnancy". Drugs.com. 12 July 2019. Dicapai pada 27 September 2020.
- ^ a b "Levodopa Content of Mucuna pruriens Supplements in the NIH Dietary Supplement Label Database". JAMA Neurology. 79 (10): 1085–1086. October 2022. doi:10.1001/jamaneurol.2022.2184. PMID 35939305 Check
|pmid=value (bantuan). - ^ "L-DOPA is an endogenous ligand for OA1". PLOS Biology. 6 (9): e236. September 2008. doi:10.1371/journal.pbio.0060236. PMC 2553842. PMID 18828673.
- ^ "The protein Ocular albinism 1 is the orphan GPCR GPR143 and mediates depressor and bradycardic responses to DOPA in the nucleus tractus solitarii". British Journal of Pharmacology. 171 (2): 403–14. January 2014. doi:10.1111/bph.12459. PMC 3904260. PMID 24117106.
- ^ "Barrier mechanisms for neurotransmitter monoamines and their precursors at the blood-brain interface". Annals of Neurology. 8 (1): 1–31. July 1980. doi:10.1002/ana.410080102. PMID 6105837.
- ^ "Levodopa: History and Therapeutic Applications". Annals of Indian Academy of Neurology. 20 (3): 185–189. 2017. doi:10.4103/aian.AIAN_241_17 (Tidak aktif 31 December 2022). PMC 5586109. PMID 28904446.CS1 maint: DOI inactive as of Disember 2022 (link)
- ^ "Medicare D". Medicare. 2014. Dicapai pada 12 November 2015.
- ^ "Lodosyn", Drugs, nd, dicapai pada 12 November 2012
- ^ "Inbrija Prescribing Information" (PDF). Dicapai pada February 14, 2019.
- ^ "Acorda Therapeutics Announces FDA Approval of INBRIJA™ (levodopa inhalation powder)". ir.acorda.com (dalam bahasa Inggeris). Dicapai pada 2019-02-14.
- ^ "Levodopa for restless legs syndrome". The Cochrane Database of Systematic Reviews. 2011 (2): CD005504. February 2011. doi:10.1002/14651858.CD005504.pub2. PMC 8889887 Check
|pmc=value (bantuan). PMID 21328278. - ^ Broadley KJ (March 2010). "The vascular effects of trace amines and amphetamines". Pharmacology & Therapeutics. 125 (3): 363–375. doi:10.1016/j.pharmthera.2009.11.005. PMID 19948186.
- ^ Lindemann L, Hoener MC (May 2005). "A renaissance in trace amines inspired by a novel GPCR family". Trends in Pharmacological Sciences. 26 (5): 274–281. doi:10.1016/j.tips.2005.03.007. PMID 15860375.
- ^ Wang X, Li J, Dong G, Yue J (February 2014). "The endogenous substrates of brain CYP2D". European Journal of Pharmacology. 724: 211–218. doi:10.1016/j.ejphar.2013.12.025. PMID 24374199.
- ^ Rodgers KJ (March 2014). "Non-protein amino acids and neurodegeneration: the enemy within". Experimental Neurology. 253: 192–196. doi:10.1016/j.expneurol.2013.12.010. PMID 24374297. S2CID 2288729.
- ^ Hyland K, Clayton PT (December 1992). "Aromatic L-amino acid decarboxylase deficiency: diagnostic methodology" (PDF). Clinical Chemistry. 38 (12): 2405–10. doi:10.1093/clinchem/38.12.2405. PMID 1281049. Diarkibkan daripada yang asal (PDF) pada 2011-06-07. Dicapai pada 2008-10-16.
- ^ Ito S, Kato T, Shinpo K, Fujita K (September 1984). "Oxidation of tyrosine residues in proteins by tyrosinase. Formation of protein-bonded 3,4-dihydroxyphenylalanine and 5-S-cysteinyl-3,4-dihydroxyphenylalanine". The Biochemical Journal. 222 (2): 407–11. doi:10.1042/bj2220407. PMC 1144193. PMID 6433900.
- ^ Waite JH, Andersen NH, Jewhurst S, Sun C (2005). "Mussel Adhesion: Finding the Tricks Worth Mimicking". J Adhesion. 81 (3–4): 1–21. doi:10.1080/00218460590944602. S2CID 136967853.
- ^ "Study Reveals Details Of Mussels' Tenacious Bonds". Science Daily. Aug 16, 2006. Dicapai pada Sep 30, 2013.
- ^ "Mussel Adhesive Protein Mimetics". Diarkibkan daripada yang asal pada 2006-05-29.
- ^ Giuri D, Ravarino P, Tomasini C (June 2021). "L-Dopa in small peptides: an amazing functionality to form supramolecular materials". Organic & Biomolecular Chemistry. 19 (21): 4622–4636. doi:10.1039/D1OB00378J. hdl:11585/840774. PMID 33978030. S2CID 234474122.
- ^ Fichman G, Adler-Abramovich L, Manohar S, Mironi-Harpaz I, Guterman T, Seliktar D, dll. (July 2014). "Seamless metallic coating and surface adhesion of self-assembled bioinspired nanostructures based on di-(3,4-dihydroxy-L-phenylalanine) peptide motif". ACS Nano. 8 (7): 7220–7228. doi:10.1021/nn502240r. PMC 4108209. PMID 24936704.
- ^ Fichman G, Guterman T, Adler-Abramovich L, Gazit E (August 2014). "The Use of the Calcitonin Minimal Recognition Module for the Design of DOPA-Containing Fibrillar Assemblies". Nanomaterials. 4 (3): 726–740. doi:10.3390/nano4030726. PMC 5304689. PMID 28344244.
- ^ Fichman G, Andrews C, Patel NL, Schneider JP (October 2021). "Antibacterial Gel Coatings Inspired by the Cryptic Function of a Mussel Byssal Peptide". Advanced Materials. 33 (40): e2103677. doi:10.1002/adma.202103677. PMC 8492546 Check
|pmc=value (bantuan). PMID 34423482 Check|pmid=value (bantuan). - ^ Maity S, Nir S, Zada T, Reches M (October 2014). "Self-assembly of a tripeptide into a functional coating that resists fouling". Chemical Communications. 50 (76): 11154–11157. doi:10.1039/C4CC03578J. PMID 25110984.
- ^ "Dopamine dysregulation syndrome, addiction and behavioral changes in Parkinson's disease". Parkinsonism & Related Disorders. 14 (4): 273–80. 2008. doi:10.1016/j.parkreldis.2007.09.007. PMID 17988927.
- ^ "Molecular Effects of L-dopa Therapy in Parkinson's Disease". Current Genomics. 15 (1): 11–7. February 2014. doi:10.2174/1389202914666131210213042. PMC 3958954. PMID 24653659.
- ^ "[Distribution of noradrenaline and dopamine (3-hydroxytyramine) in the human brain and their behavior in diseases of the extrapyramidal system]". Klinische Wochenschrift. 38 (24): 1236–9. December 1960. doi:10.1007/BF01485901. PMID 13726012.
- ^ "[The L-3,4-dioxyphenylalanine (DOPA)-effect in Parkinson-akinesia]". Wiener Klinische Wochenschrift. 73: 787–8. November 1961. PMID 13869404.
- ^ "L-dopa in parkinson's syndrome". The New England Journal of Medicine. 281 (5): 272. July 1969. doi:10.1056/NEJM196907312810518. PMID 5791298.
- ^ "Lasker Award". 1969. Diarkibkan daripada yang asal pada 2016-01-05.
- ^ Simuni T, Hurtig H (2008). "Levadopa: A Pharmacologic Miracle Four Decades Later". Dalam Factor SA, Weiner WJ (penyunting). Parkinson's Disease: Diagnosis and Clinical Management. Demos Medical Publishing. ISBN 9781934559871 – melalui Google eBook.
- ^ "L-Dopa for Parkinsonism". The New England Journal of Medicine. 278 (11): 630. March 1968. doi:10.1056/nejm196803142781127. PMID 5637779.
- ^ "Asymmetric hydrogenation". Accounts of Chemical Research. 16 (3): 106–112. 1983. doi:10.1021/ar00087a006.
- ^ "Synthetic scheme for total synthesis of DOPA, L- (Monsanto)". UW Madison, Department of Chemistry. Dicapai pada Sep 30, 2013.
- ^ "Application of organometallic catalysis to the commercial production of L-DOPA". Journal of Chemical Education. 63 (3): 222. March 1986. Bibcode:1986JChEd..63..222K. doi:10.1021/ed063p222.
Pautan luar[sunting | sunting sumber]
- "Levodopa". Drug Information Portal. U.S. National Library of Medicine.
- CS1 errors: PMID
- CS1 maint: DOI inactive as of Disember 2022
- CS1 errors: PMC
- Template:drugs.com link with non-standard subpage
- Drugs with non-standard legal status
- ECHA InfoCard ID from Wikidata
- Infobox rencana dadah dengan tajuk infobox tidak lalai
- Drug has EMA link
- Drugboxes which contain changes to watched fields
- Pelopor monoamina
- Agonis dopamina
- Katekolamina
- Asid amino aromatik
- Agen anti-Parkinson



