Isomer
Dalam bidang kimia, isomer ialah molekul yang mempunyai formula kimia yang sama. Ia sering juga mempunyai jenis ikatan yang sama antara atom, namun penyusunan atom-atomnya berlainan, iaitu isomer-isomer mempunyai formula struktur yang berbeza. Banyak isomer mempunyai sifat yang hampir serupa jika bukan sama dalam kebanyakan konteks kimia. Ini harus tidak dikelirukan dengan isomer nuklear yang melibatkan sebiji nukleus dalam keadaan-keadaan keterangsangan yang berbeza.
Contoh yang mudah untuk keisomeran diberikan oleh propanol: propanol mempunyai formula C3H8O (atau C3H7OH) dan dua isomer Propan-1-ol (alkohol n-profil; I) dan Propan-2-ol (alkohol isoprofil; II)
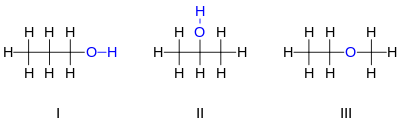
Perhatikanlah bahawa kedudukan atom oksigen berbeza antara kedua-dua isomer itu: atom oksigen diikatkan pada hujung atom karbon dalam isomer pertama, dan pada karbon tengah dalam isomer kedua. Bilangan isomer yang mungkin akan bertambah dengan pesat ketika bilangan atom bertambah; umpamanya, alkohol yang kedua terbesar, iaitu butanol (C4H10O), mempunyai lima isomer yang berbeza.
Dalam contoh di atas, harus diperhatikan bahawa untuk kedua-dua isomer itu, kesemua ikatan adalah ikatan tunggal; tidak adanya jenis ikatan yang terdapat dalam satu isomer tetapi tidak terdapat dalam isomer yang lain. Bilangan ikatan juga adalah sama. Daripada struktur kedua-dua molekul itu, bolehlah disimpulkan bahawa kestabilan kimia adalah sama atau hampir sama.
Bagaimanapun, terdapat lagi satu isomer C3H8O yang mempunyai sifat yang amat berbeza: eter etil metil (III). Perhatikanlah bahawa berbeza dengan kedua-dua contoh di atas, atom oksigen diikatkan kepada dua atom karbon, berbanding satu atom karbon dan satu atom hidrogen. Oleh sebab isomer ini tidak mempunyai satu kumpulan hidroksil, molekul tersebut tidak lagi dianggap sebagai alkohol, tetapi dikelaskan sebagai eter, dan mempunyai sifat kimia yang lebih serupa dengan eter yang lain berbanding isomer alkohol di atas.
Lagi satu contoh isomer yang mempunyai sifat yang amat berbeza boleh didapati di sebilangan xantin. Teobromin didapati dalam coklat, tetapi jika salah satu daripada dua kumpulan metilnya dialihkan ke kedudukan yang lain dalam teras cecincin kembarnya, isomer itu akan menjadi teofilin yang digunakan sebagai bronkodilator.
Bentuk keisomeran[sunting | sunting sumber]
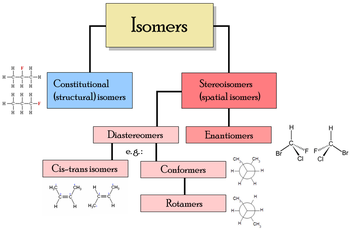
Terdapat dua jenis keisomeran yang berbeza:
Dalam isomer struktur, atom dan kumpulan fungsi diikatkan dengan cara-cara yang berbeza, umpamanya alkohol profil di atas. Kumpulan ini termasuk keisomeran rantai yang mana rantai-rantai hidrokarbon mempunyai pencabangan yang berbeza-beza; keisomeran kedudukan yang berkenaan dengan penempatan kumpulan fungsian dalam satu rantai; dan keisomeran kumpulan fungsian yang mana satu kumpulan fungsian dipisahkan menjadi kumpulan-kumpulan yang berbeza.
Dalam stereoisomer, struktur ikatan adalah sama, tetapi kedudukan geometri untuk setiap atom dan kumpulan fungsian dalam ruang adalah berbeza. Kelas ini termasuk enantiomer yang mana isomer-isomer yang berbeza adalah imej cermin bagi satu sama lain, dan diastereomer ketika sebaliknya. Kediastereomeran pula dibahagikan kepada keisomeran konformasi (konformer) jika isomer-isomer itu dapat saling bertukar melalui putaran-putaran ikatan kimia, dan keisomeran cis-trans apabila ini tidak mungkin.[1] Stereoisomer mempunyai 2 kelompok berfungsi disambung pada ikatan ganda dua atau struktur cincin yang kekal;[2] stereoisomer cis mempunyai kelompok yang sejajar sedangkan stereoisomer trans mempunyai kelompok yang bersambung saling bertentangan.

|

|
| cis-but-2-ena
dengan kelompok metil sejajar |
trans-but-2-ena
dengan kelompok metil setentangan |
Perhatikanlah bahawa walaupun konformer boleh dirujuk sebagai mempunyai satu hubungan diastereomer, isomer-isomer bukannya diastereomer pada dirinya kerana ikatan-ikatan dalam konformer boleh diputarkan untuk menghasilkan imej-imej cermin.
Dalam kimia makanan, kimia perubatan dan biokimia, keisomeran cis-trans sering dipertimbangkan. Dalam kimia perubatan dan biokimia, enantiomer kini amat menarik kerana kebanyakan perubahan dalam jenis-jenis isomer ini kini diketahui amat bermakna kepada organisma-organisma hidup. Penyelidik-penyelidik dalam industri perubatan dan universiti telah mendapat kaedah-kaedah kromatografi untuk mengasingkannya dengan pasti. Bagaimanapun, kaedah-kaedah ini amat mahal pada skala perindustrian dan hanya digunakan jika isomer yang lain berpotensi mendatangkan keburukan.
Sedangkan isomer-isomer struktur biasanya mempunyai sifat-sifat kimia yang berbeza, stereoisomer-stereoisomer mempunyai tindakan yang sama dalam kebanyakan reaksi kimia. Bagaimanapun, enzim boleh membezakan antara stereoisomer-stereoisomer sebatian yang berbeza, dan organisma-organisma seringnya lebih menyukai satu stereoisomer berbanding yang lain. Sebilangan stereoisomer juga berbeza dari segi cara untuk memutarkan cahaya terkutub.
Jenis-jenis keisomeran yang lain adalah di luar lingkungan rencana ini. Terdapat juga isomer-isomer topologi yang digelarkan topoisomer. Molekul-molekul yang mempunyai topoisomer termasuk katenana dan DNA. Enzim topoisomerase boleh menyimpulkan DNA dan oleh itu, mengubahkan topologinya. Terdapat juga isomer isotopomer (juga digelarkan "isomer isotop") yang mempunyai bilangan yang sama untuk setiap penggantian isotop tetapi dengan kedudukan kimianya berlainan. Dalam fizik nuklear, isomer-isomer nuklear merupakan keadaan-keadaan keterangsangan nukleus atom.
Sejarah[sunting | sunting sumber]
Fenomena keisomeran dilihat buat pertama kali pada 1827 ketika Friedrich Woehler menyediakan asid sianida dan memperhatikan bahawa walaupun kandungan unsurnya adalah sama sahaja dengan asid fulminik (yang disediakan oleh Justus von Liebig pada tahun yang lalu), sifat-sifatnya amat berbeza. Dapatan ini mencabarkan pemahaman kimia pada masa itu yang menganggap bahawa sebatian kimia hanya boleh berbeza jika sebatian-sebatian itu mempunyai kandungan unsur yang berbeza. Selepas temuan-temuan lain yang serupa telah dijumpai, contohnya penemuan Woehler pada tahun 1828 bahawa urea mempunyai kandungan atom yang sama dengan sainida ammonium, Berzelius memperkenalkan istilah keisomeran untuk memerihalkan fenomena itu.
Pada tahun 1849, Louis Pasteur mengasingkan kristal-kristal asid tartarik yang amat kecil itu menjadi dua bentuk imej cermin. Molekul bagi setiap bentuk itu merupakan stereoisomer optik kiri dan kanan, dengan larutan-larutannya memutarkan satah cahaya terkutub pada arah yang bertentangan.
Lihat juga[sunting | sunting sumber]
Rujukan[sunting | sunting sumber]
- ^ Kesatuan Kimia Tulen dan Gunaan Antarabangsa. "geometric isomerism". Ringkasan Terminologi Kimia Edisi Internet.
- ^ Reusch, William (2010). "Stereoisomers Part I". Virtual Textbook of Organic Chemistry. Michigan State University. Dicapai pada 7 April 2015.
