Pendarahan otak
| Pendarahan otak | |
|---|---|
Nama lain | Pembedahan intraserebrum, Pembedahan serebrum, pembedahan intrapaksi |
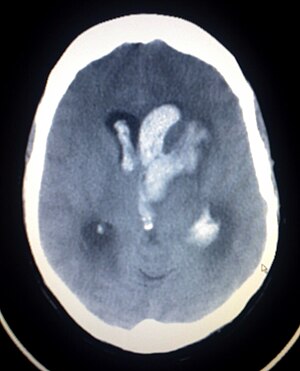 | |
| Imbasan CT pendarahan otak spontan yang membocor ke ventrikel lateral | |
| Pengkhususan | Neuropembedahan |
| Gejala | Sakit kepala, lemah sebelah badan, muntah, sawan, penurunan kesedaran, ketegangan leher, demam[1][2] |
| Punca | Trauma otak, aneurisme, malformasi arteriovena, tumor otak[1] |
| Tekanan darah tinggi, amiloidosis, alkoholisme, kolesterol rendah, penyahgumpal darah, kokain use[2] | |
| Imbasan CT[1] | |
| Angin ahmar iskemia[1] | |
| Rawatan | Kawalan tekanan darah, pembedahan, saliran ventrikel[1] |
| Prognosis | 20%, hasil baik[2] |
| Kekerapan | 2.5 per 10,000 orang setahun[2] |
| Kematian | 44% maut dalam bulan pertama[2] |
| sunting | |
Pendarahan otak/intraserebrum (ICH), juga dikenali sebagai pendarahan serebrum, pendarahan intraparenkima, dan strok hemoragik, ialah pendarahan secara tiba-tiba ke dalam tisu otak, ke dalam ventrikelnya atau kedua-duanya.[3][4][1] ICH ialah satu jenis pendarahan dalam tengkorak (kranium),[3] dan satu jenis angin ahmar.[4] Gejala boleh termasuk sakit kepala, lemah sebelah badan, muntah, sawan, tahap kesedaran menurun dan leher kaku.[2] Selalunya, gejala menjadi lebih teruk dari masa ke masa.[1] Demam pun biasa.[1]
Puncanya termasuklah trauma otak, aneurisme, kecacatan arteriovenus dan tumor otak.[1] Faktor risiko terbesar pendarahan spontan ialah tekanan darah tinggi dan amiloidosis.[2] Faktor risiko lain termasuk alkoholisme, kolesterol rendah, penyahgumpal darah dan penggunaan kokain.[2] Diagnosis biasanya melalui imbasan CT.[1] Keadaan lain yang mungkin berlaku serupa termasuk angin ahmar iskemia.[1]
Rawatan biasanya perlu dijalankan di unit rawatan rapi.[1] Garis panduan mengesyorkan menurunkan tekanan darah kepada sistolik 140 mmHg.[1][5] Penyahgumpalan darah harus diterbalikkan jika boleh dan gula darah dikekalkan dalam julat normal.[1] Pembedahan untuk meletakkan saluran ventrikel boleh digunakan untuk merawat hidrosefalus, tetapi kortikosteroid tidak boleh digunakan.[1] Pembedahan untuk mengeluarkan darah berguna dalam kes tertentu.[1]
Pendarahan serebrum menjejaskan kira-kira 2.5 setiap 10,000 orang setiap tahun.[2] Ia berlaku lebih kerap dalam kalangan lelaki dan orang tua.[2] Kira-kira 44% daripada mereka yang terjejas mati dalam masa sebulan.[2] Hasil yang baik berlaku pada kira-kira 20% daripada mereka yang terjejas.[2] Pendarahan intraserebrum, sejenis angin ahmar pendarahan, pertama kali dibezakan daripada strok iskemia kerana aliran darah yang tidak mencukupi, yang dipanggil sebagai "kebocoran dan palam", pada tahun 1823.[6]
Tanda dan gejala[sunting | sunting sumber]
Orang yang mengalami pendarahan intraserebrum mempunyai gejala yang sepadan dengan fungsi yang dikawal oleh kawasan otak yang rosak akibat pendarahan.[7] Tanda-tanda dan simptom penyetempatan ini boleh termasuk hemiplegia (lemah satu sisi badan) dan parestesia (kehilangan sensasi) termasuk kehilangan deria separuh (jika disetempat pada satu sisi badan).[8] Gejala-gejala ini biasanya berlaku dengan cepat, kadangkala berlaku dalam beberapa minit, tetapi tidak secepat permulaan gejala dalam strok iskemia.[8] Gejala lain termasuk yang menunjukkan peningkatan tekanan intrakranium yang disebabkan oleh jisim yang besar (akibat pengembangan hematoma) yang memberi tekanan pada otak.[7] Gejala ini termasuk sakit kepala, loya, muntah, tahap kesedaran yang tertekan, pengsan dan kematian.[8] Peningkatan berterusan dalam tekanan intrakranial dan kesan jisim yang disertakan akhirnya boleh menyebabkan herniasi otak (apabila bahagian otak yang berlainan dialihkan atau dialihkan ke kawasan baru berhubung dengan tengkorak dan struktur sokongan dura mater di sekeliling). Hernia otak dikaitkan dengan hiperventilasi, ketegaran ekstensor, anak mata tak simetri, tanda piramid, koma dan maut.[9]
Pendarahan ke dalam ganglion basal atau talamus menyebabkan hemiplegia kontralateral akibat kerosakan pada kapsul dalaman.[8] Gejala lain yang mungkin termasuk palsi pandangan atau kehilangan deria separa.[8] Pendarahan intraserebrum ke dalam serebelum boleh menyebabkan ataksia, vertigo, hilang koordinasi anggota badan dan muntah.[8] Sesetengah kes pendarahan serebelar membawa kepada penyumbatan ventrikel keempat dengan gangguan pengaliran cecair serebrospinal dari otak secara lanjutan.[8] Seterusnya, hidrosefalus atau pengumpulan cecair dalam ventrikel otak membawa kepada penurunan kesedaran dan koma.[8] Pendarahan batang otak paling kerap berlaku di pons dan dikaitkan dengan lumpuh saraf kranium, anak mata (tetapi reaktif), lumpuh pandangan, kelemahan muka dan koma (jika terdapat kerosakan pada sistem pengaktifan retikulum).[8]
Punca[sunting | sunting sumber]

Pendarahan intraserebrum ialah penyebab strok kedua paling biasa, menyumbang 10% daripada kemasukan ke hospital bagi angin ahmar.[11] Tekanan darah tinggi meningkatkan risiko pendarahan otak spontan sebanyak dua hingga enam kali ganda.[10] Lebih biasa pada orang dewasa berbanding kanak-kanak, pendarahan intraparenkima biasanya disebabkan oleh trauma kepala tembusan, tetapi juga boleh disebabkan oleh patah tulang tengkorak yang tertekan. Trauma pecutan-nyahpecutan,[12][13][14] pecah aneurisme atau kecacatan arteriovena (AVM), dan pendarahan dalam tumor ialah punca tambahan. Angiopati amiloid bukanlah penyebab biasa pendarahan intracerebral pada pesakit yang berumur lebih dari 55 tahun.
Faktor risiko untuk ICH termasuk:[15]
- Hipertensi (tekanan darah tinggi)
- Diabetes melitus
- Menopaus
- Pengambilan alkohol yang berlebihan
- Migrain teruk
Hipertensi ialah faktor risiko paling kuat yang dikaitkan dengan pendarahan otak, dan kawalan jangka panjang tekanan darah tinggi telah ditunjukkan untuk mengurangkan kejadian pendarahan.[8] Angiopati amiloid serebrum, penyakit yang dicirikan oleh pemendapan peptida amiloid beta di dinding saluran darah kecil otak, yang membawa kepada lemah dinding saluran darah dan peningkatan risiko pendarahan; juga merupakan faktor risiko penting untuk perkembangan pendarahan intraserebrum. Faktor risiko lain termasuk usia lanjut (biasanya dengan peningkatan serentak risiko angiopati amiloid serebrum pada orang tua), penggunaan antikoagulan atau ubat antiplatelet, kehadiran pendarahan mikro serebrum, penyakit buah pinggang kronik dan paras lipoprotein ketumpatan rendah (LDL) rendah (biasanya di bawah 70).[16][17] Antikoagulan oral langsung (DOAC) seperti perencat faktor Xa atau perencat trombin langsung dianggap mempunyai risiko pendarahan otak yang lebih rendah berbanding antagonis vitamin K seperti warfarin.[8]
Merokok mungkin menjadi faktor risiko tetapi perkaitannya lemah.[18]
Diagnosis[sunting | sunting sumber]

Kedua-dua angiografi tomografi berkomputer (CTA) dan angiografi resonans magnet (MRA) telah terbukti berkesan dalam mendiagnosis kecacatan vaskular intrakranium selepas ICH.[19] Selalunya, angiogram CT akan dilakukan untuk mengecualikan penyebab sekunder pendarahan[20] atau untuk mengesan "tanda titik".
Pendarahan intraparenkima boleh dikenal pasti dalam imbasan CT kerana darah kelihatan lebih cerah daripada tisu lain dan dipisahkan dari meja dalaman tengkorak oleh tisu otak. Tisu yang mengelilingi pendarahan selalunya kurang padat daripada bahagian otak yang lain kerana edema, dan oleh itu, kelihatan lebih gelap dalam imbasan CT.[20] Edema yang mengelilingi pendarahan akan meningkat dengan cepat dalam saiz dalam 48 jam pertama, dan mencapai tahap maksimum pada hari ke-14. Semakin besar saiz hematoma, semakin besar edema sekelilingnya.[21] Pembentukan edema otak adalah disebabkan oleh pecahan sel darah merah, di mana hemoglobin dan kandungan lain sel darah merah dibebaskan. Pembebasan kandungan sel darah merah ini menyebabkan kesan toksik pada otak dan menyebabkan edema otak. Selain itu, pemecahan sempadan darah-otak juga menyumbang kepada pembentukan edema.[22]
Selain imbasan CT, perkembangan hematoma pendarahan intraserebrum boleh dipantau menggunakan ultrabunyi transkranium. Prob ultrabunyi boleh diletakkan di lobus temporal untuk menganggar isi padu hematoma di dalam otak, dan dengan itu, mengenal pasti mereka yang mengalami pendarahan aktif bagi campur tangan selanjutnya untuk menghentikan pendarahan. Teknik ultrabunyi juga boleh mengurangkan risiko radiasi imbasan CT kepada subjek.[23]
Lokasi[sunting | sunting sumber]
Apabila disebabkan oleh tekanan darah tinggi, pendarahan intracerebral biasanya berlaku di putamen (50%) atau talamus (15%), serebrum (10-20%), otak kecil (10-13%), pons (7-15%), atau di tempat lain di batang otak (1-6%).[24][25]
Rawatan[sunting | sunting sumber]
Rawatan bergantung pada jenis ICH. Imbasan CT pantas dan langkah diagnostik lain digunakan untuk menentukan rawatan yang betul, yang mungkin termasuk kedua-dua ubat dan pembedahan.
- Intubasi trakea ditunjukkan pada orang yang mengalami penurunan tahap kesedaran atau risiko lain halangan saluran pernafasan.[26]
- Cecair intravena diberikan untuk mengekalkan keseimbangan cecair, menggunakan cecair isotonik dan bukannya hipotonik.[26]
Ubat[sunting | sunting sumber]
Penurunan tekanan darah dengan pantas dengan terapi antihipertensi bagi mereka yang mengalami kecemasan hipertensi boleh mempunyai pemulihan fungsi yang lebih tinggi pada 90 hari selepas pendarahan otak jika dibandingkan dengan mereka yang menjalani rawatan lain seperti pemberian manitol, pembalikan antikoagulasi (mereka yang sebelum ini menggunakan rawatan antikoagulan untuk keadaan lain), pembedahan mengosongkan hematoma yang sama, dan rehabilitasi lazim di hospital, dengan kadar kematian yang sama: 12%.[27] Penurunan awal tekanan darah boleh mengurangkan jumlah hematoma, tetapi mungkin tidak mempunyai sebarang kesan terhadap edema yang mengelilingi hematoma.[28] Penurunan tekanan darah dengan cepat tidak menyebabkan iskemia otak pada mereka yang mengalami pendarahan otak.[29] Garis panduan Persatuan Jantung Amerika dan Persatuan Strok Amerika pada tahun 2015 mengesyorkan menurunkan tekanan darah kepada SBP sebanyak 140 mmHg.[1] Walau bagaimanapun, tinjauan kemudian mendapati perbezaan yang tidak jelas antara kawalan tekanan darah intensif dan kurang intensif.[30][31]
Pemberian Faktor VIIa dalam masa 4 jam mengehadkan pendarahan dan pembentukan hematoma. Walau bagaimanapun, ia juga meningkatkan risiko tromboembolisme.[26] Oleh itu, ia secara keseluruhannya tidak menghasilkan hasil yang lebih baik bagi mereka yang tidak mempunyai hemofilia.[32]
Transfusi plasma beku, vitamin K, protamina atau platelet boleh diberikan sekiranya berlaku koagulopati.[26] Platelet bagaimanapun kelihatan memburukkan hasil pada mereka yang mengalami pendarahan otak spontan yang menggunakan ubat antiplatelet.[33]
Ejen pembalikan khusus idarusizumab dan andeksanet alfa boleh digunakan untuk menghentikan pendarahan intraserebrum yang berterusan pada orang yang mengambil antikoagulan bertindak secara oral (seperti perencat faktor Xa atau perencat trombin langsung).[8] Walau bagaimanapun, jika ubat khusus ini tidak tersedia, larutan kompleks protrombin juga boleh digunakan.[8]
Hanya 7% daripada mereka yang mempunyai ICH ditunjukkan dengan ciri-ciri klinikal sawan manakala sehingga 25% daripada mereka mempunyai sawan subklinikal. Sawan tidak dikaitkan dengan peningkatan risiko kematian atau hilang upaya. Sementara itu, pemberian antikonvulsan boleh meningkatkan risiko kematian. Oleh itu, antikonvulsan hanya dikhaskan untuk mereka yang telah menunjukkan ciri-ciri klinikal yang jelas bagi sawan atau aktiviti sawan pada elektroensefalografi (EEG).[34]
Antagonis H2 atau perencat pam proton biasanya diberikan untuk cuba mencegah ulser tekanan, keadaan yang dikaitkan dengan ICH.[26]
Kortikosteroid pernah dianggap mengurangkan bengkak. Walau bagaimanapun, dalam kajian terkawal yang besar, kortikosteroid didapati meningkatkan kadar kematian dan tidak lagi disyorkan.[35][36]
Pembedahan[sunting | sunting sumber]
Pembedahan diperlukan jika hematoma lebih besar daripada 3 cm (1 in), jika terdapat lesi vaskular struktur atau pendarahan lobus pada pesakit muda.[26]
Suatu kateter mungkin disalurkan ke vaskulatur otak untuk menutup atau mencairkan saluran darah, sekaligus mengelakkan pembedahan invasif.[37]
Aspirasi melalui pembedahan stereotaktik atau saliran endoskopi boleh digunakan dalam pendarahan ganglion basal, walaupun laporan kejayaan adalah terhad.[26]
Kraniektomi menjanjikan pengurangan kematian, tetapi kesan hasil neurologi jangka panjang masih menjadi kontroversi.[38]
Prognosis[sunting | sunting sumber]
Kira-kira 8 hingga 33% daripada mereka yang mengalami pendarahan intrakranial mengalami kemerosotan neurologi dalam 24 jam pertama kemasukan ke hospital, di mana sebahagian besar daripadanya berlaku dalam masa 6 hingga 12 jam. Kadar pengembangan hematoma, isi padu edema perihematoma dan kehadiran demam boleh memberi kesan terhadap peluang mendapat komplikasi neurologi.[39]
Risiko kematian akibat pendarahan intraparenkima dalam kecederaan otak traumatik amat tinggi apabila kecederaan berlaku di batang otak.[40] Pendarahan intraparenkima dalam medula oblongata hampir selalu membawa maut kerana ia menyebabkan kerosakan pada saraf kranium X, yakni saraf vagus yang memainkan peranan penting dalam peredaran darah dan pernafasan.[12] Pendarahan jenis ini juga boleh berlaku di kawasan korteks atau subkorteks, biasanya di lobus hadapan atau temporal apabila disebabkan oleh kecederaan kepala, dan kadang-kadang di serebelum .[12][41] Isi padu hematoma yang lebih besar semasa kemasukan ke hospital serta pengembangan hematoma yang lebih besar pada penilaian berikutnya (biasanya berlaku dalam masa 6 jam dari permulaan simptom) dikaitkan dengan prognosis yang lebih teruk.[8][42] Edema perihematoma atau edema sekunder yang mengelilingi hematoma, dikaitkan dengan kecederaan otak sekunder, memburukkan fungsi neurologi dan dikaitkan dengan prognosis buruk.[8] Pendarahan intraventrikel atau pendarahan ke dalam ventrikel otak yang mungkin berlaku pada 30-50% pesakit juga dikaitkan dengan ketidakupayaan jangka panjang dan prognosis yang buruk.[8] Hernia otak dikaitkan dengan prognosis yang buruk.[8]
Untuk pendarahan otak spontan yang dilihat pada imbasan CT, kadar kematian ialah 34-50% dalam masa 30 hari selepas kecederaan,[10] dan separuh daripada kematian berlaku dalam 2 hari pertama.[43] Walaupun majoriti kematian berlaku dalam beberapa hari pertama selepas pendarahan otak, mangsa yang terselamat mempunyai kadar kematian berlebihan jangka panjang sebanyak 27% berbanding populasi umum.[44] Daripada mereka yang pulih daripada pendarahan otak, 12–39% adalah bebas berkaitan penjagaan diri, dengan pesakit lain menjadi kurang upaya pada tahap yang berbeza-beza dan memerlukan penjagaan sokongan.[45]
Epidemiologi[sunting | sunting sumber]
Insiden pendarahan intraserebrum dianggarkan pada 24.6 kes bagi setiap 100,000 orang tahun dengan kadar kejadian serupa antara lelaki dengan wanita.[8][45] Insiden adalah lebih tinggi pada orang tua, terutamanya mereka yang berumur 85 tahun ke atas, yang 9.6 kali lebih berkemungkinan mengalami pendarahan otak berbanding mereka yang berumur pertengahan.[45] Ia menyumbang 20% daripada semua kes penyakit serebrovaskular di Amerika Syarikat, di belakang trombosis serebrum (40%) dan embolisme serebrum (30%).[46]
Penyelidikan[sunting | sunting sumber]
Tindak balas keradangan yang dicetuskan oleh angin ahmar telah dilihat sebagai berbahaya pada peringkat awal, memfokuskan pada leukosit bawaan darah, neutrofil dan makrofaj, serta mikroglia dan astrosit tempatan.[47][48] Kajian bedah siasat manusia menunjukkan bahawa keradangan berlaku awal dan berterusan selama beberapa hari selepas ICH.[49] Pemodulan pengaktifan dan polarisasi mikroglial mungkin mengurangkan kecederaan otak yang disebabkan oleh pendarahan otak dan menambah baik pembaikan otak.[50] Satu bidang baru yang menarik ialah peranan sel masta dalam pendarahan otak.[48][51]
Rujukan[sunting | sunting sumber]
- ^ a b c d e f g h i j k l m n o p q "Guidelines for the Management of Spontaneous Intracerebral Hemorrhage: A Guideline for Healthcare Professionals From the American Heart Association/American Stroke Association". Stroke. 46 (7): 2032–2060. July 2015. doi:10.1161/str.0000000000000069. PMID 26022637. Unknown parameter
|displayauthors=ignored (bantuan) - ^ a b c d e f g h i j k l "Intracranial hemorrhage". Emergency Medicine Clinics of North America. 30 (3): 771–794. August 2012. doi:10.1016/j.emc.2012.06.003. PMC 3443867. PMID 22974648.
- ^ a b "Brain Bleed/Hemorrhage (Intracranial Hemorrhage): Causes, Symptoms, Treatment".
- ^ a b Naidich TP, Castillo M, Cha S, Smirniotopoulos JG (2012). Imaging of the Brain, Expert Radiology Series,1: Imaging of the Brain (dalam bahasa Inggeris). Elsevier Health Sciences. m/s. 387. ISBN 978-1416050094. Diarkibkan daripada yang asal pada 2016-10-02.
- ^ "Blood Pressure Management for Acute Ischemic and Hemorrhagic Stroke: The Evidence". Seminars in Respiratory and Critical Care Medicine. 38 (6): 718–725. December 2017. doi:10.1055/s-0037-1608777. PMID 29262429.
- ^ Hennerici M (2003). Imaging in Stroke (dalam bahasa Inggeris). Remedica. m/s. 1. ISBN 9781901346251. Diarkibkan daripada yang asal pada 2016-10-02.
- ^ a b Vinas FC and Pilitsis J. 2006. "Penetrating Head Trauma." Diarkibkan 2005-09-13 di Wayback Machine Emedicine.com.
- ^ a b c d e f g h i j k l m n o p q r "Spontaneous Intracerebral Hemorrhage". The New England Journal of Medicine. 387 (17): 1589–1596. October 2022. doi:10.1056/NEJMra2201449. PMID 36300975 Check
|pmid=value (bantuan). - ^ "Brain herniations in patients with intracerebral hemorrhage". Acta Neurologica Scandinavica. 119 (4): 254–260. April 2009. doi:10.1111/j.1600-0404.2008.01095.x. PMID 19053952.
- ^ a b c d "Endoscopic management of hypertensive intraventricular haemorrhage with obstructive hydrocephalus". BMC Neurology. 7: 1. January 2007. doi:10.1186/1471-2377-7-1. PMC 1780056. PMID 17204141.
- ^ "Heart disease and stroke statistics--2013 update: a report from the American Heart Association". Circulation. 127 (1): e6–e245. January 2013. doi:10.1161/CIR.0b013e31828124ad. PMC 5408511. PMID 23239837. Unknown parameter
|displayauthors=ignored (bantuan) - ^ a b c McCaffrey P. 2001. "The Neuroscience on the Web Series: CMSD 336 Neuropathologies of Language and Cognition." Diarkibkan 2005-11-25 di Wayback Machine California State University, Chico. Retrieved on June 19, 2007.
- ^ Orlando Regional Healthcare, Education and Development. 2004. "Overview of Adult Traumatic Brain Injuries." Diarkibkan 2008-02-27 di Wayback Machine Retrieved on 2008-01-16.
- ^ Shepherd S. 2004. "Head Trauma." Diarkibkan 2005-10-26 di Wayback Machine Emedicine.com. Retrieved on June 19, 2007.
- ^ "Major risk factors for intracerebral hemorrhage in the young are modifiable". Stroke. 36 (9): 1881–1885. September 2005. doi:10.1161/01.str.0000177480.62341.6b. PMID 16081867. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Low-density lipoprotein cholesterol and risk of intracerebral hemorrhage: A prospective study". Neurology. 93 (5): e445–e457. July 2019. doi:10.1212/WNL.0000000000007853. PMC 6693427. PMID 31266905. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Epidemiology, Risk Factors, and Clinical Features of Intracerebral Hemorrhage: An Update". Journal of Stroke. 19 (1): 3–10. January 2017. doi:10.5853/jos.2016.00864. PMC 5307940. PMID 28178408.
- ^ Carhuapoma JR, Mayer SA, Hanley DF (2009). Intracerebral Hemorrhage (dalam bahasa Inggeris). Cambridge University Press. m/s. 6. ISBN 978-0-521-87331-4.
- ^ "Computed tomography angiography or magnetic resonance angiography for detection of intracranial vascular malformations in patients with intracerebral haemorrhage". The Cochrane Database of Systematic Reviews. 2014 (9): CD009372. September 2014. doi:10.1002/14651858.CD009372.pub2. PMC 6544803. PMID 25177839.
- ^ a b "Comparison of CTA to DSA in determining the etiology of spontaneous ICH". The Canadian Journal of Neurological Sciences. Le Journal Canadien des Sciences Neurologiques. 36 (2): 176–180. March 2009. doi:10.1017/s0317167100006533. PMID 19378710.
- ^ "Natural history of perihematomal edema after intracerebral hemorrhage measured by serial magnetic resonance imaging". Stroke. 42 (1): 73–80. January 2011. doi:10.1161/STROKEAHA.110.590646. PMC 3074599. PMID 21164136.
- ^ Xi, Guohua; Hua, Ya; Bhasin, R. Rick; Ennis, Steven R.; Keep, Richard F.; Hoff, Julian T. (December 2001). "Mechanisms of Edema Formation After Intracerebral Hemorrhage: Effects of Extravasated Red Blood Cells on Blood Flow and Blood-Brain Barrier Integrity". Stroke (dalam bahasa Inggeris). 32 (12): 2932–2938. doi:10.1161/hs1201.099820. ISSN 0039-2499. PMID 11739998.
- ^ Ovesen, Christian; Christensen, Anders Fogh; Krieger, Derk W.; Rosenbaum, Sverre; Havsteen, Inger; Christensen, Hanne (April 2014). "Time Course of Early Postadmission Hematoma Expansion in Spontaneous Intracerebral Hemorrhage". Stroke (dalam bahasa Inggeris). 45 (4): 994–999. doi:10.1161/STROKEAHA.113.003608. ISSN 0039-2499. PMID 24627116.
- ^ Greenberg MS (2016). Handbook of Neurosurgery. ISBN 9781626232419.
- ^ Prayson RA (2012). Neuropathology (dalam bahasa Inggeris). Elsevier Health Sciences. m/s. 49. ISBN 978-1437709490. Diarkibkan daripada yang asal pada 2017-03-12.
- ^ a b c d e f g eMedicine Specialties > Neurology > Neurological Emergencies > Intracranial Haemorrhage: Treatment & Medication. Diarkibkan 2009-03-12 di Wayback Machine By David S Liebeskind, MD. Updated: Aug 7, 2006
- ^ "Implications of INTERACT2 and other clinical trials: blood pressure management in acute intracerebral hemorrhage". Stroke. 46 (1): 291–295. January 2015. doi:10.1161/STROKEAHA.114.006321. PMID 25395408.
- ^ "Effects of early intensive blood pressure-lowering treatment on the growth of hematoma and perihematomal edema in acute intracerebral hemorrhage: the Intensive Blood Pressure Reduction in Acute Cerebral Haemorrhage Trial (INTERACT)". Stroke. 41 (2): 307–312. February 2010. doi:10.1161/STROKEAHA.109.561795. PMID 20044534. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "The Intracerebral Hemorrhage Acutely Decreasing Arterial Pressure Trial". Stroke. 44 (3): 620–626. March 2013. doi:10.1161/STROKEAHA.111.000188. PMID 23391776. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Effects of Intensive Blood Pressure Lowering on Intracerebral Hemorrhage Outcomes: A Meta-Analysis of Randomized Controlled Trials". Turkish Neurosurgery. 25 (4): 544–551. 2015. doi:10.5137/1019-5149.JTN.9270-13.0 (Tidak aktif 31 December 2022). PMID 26242330.CS1 maint: DOI inactive as of Disember 2022 (link)
- ^ "Intensive blood pressure lowering in patients with acute intracerebral haemorrhage: clinical outcomes and haemorrhage expansion. Systematic review and meta-analysis of randomised trials". Journal of Neurology, Neurosurgery, and Psychiatry. 88 (4): 339–345. April 2017. doi:10.1136/jnnp-2016-315346. PMID 28214798.
- ^ "A meta-analysis of the efficacy and safety of recombinant activated factor VII for patients with acute intracerebral hemorrhage without hemophilia". Journal of Clinical Neuroscience. 17 (6): 685–693. June 2010. doi:10.1016/j.jocn.2009.11.020. PMID 20399668.
- ^ "Haemostatic therapies for acute spontaneous intracerebral haemorrhage". The Cochrane Database of Systematic Reviews. 2018 (4): CD005951. April 2018. doi:10.1002/14651858.CD005951.pub4. PMC 6494564. PMID 29664991.
- ^ Fogarty Mack, P. (December 2014). "Intracranial haemorrhage: therapeutic interventions and anaesthetic management". British Journal of Anaesthesia (dalam bahasa Inggeris). 113: ii17–ii25. doi:10.1093/bja/aeu397. PMID 25498578.
- ^ "Effect of intravenous corticosteroids on death within 14 days in 10008 adults with clinically significant head injury (MRC CRASH trial): randomised placebo-controlled trial". Lancet. 364 (9442): 1321–1328. 9 October 2016. doi:10.1016/S0140-6736(04)17188-2. PMID 15474134. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Final results of MRC CRASH, a randomised placebo-controlled trial of intravenous corticosteroid in adults with head injury-outcomes at 6 months". Lancet. 365 (9475): 1957–1959. 2005. doi:10.1016/s0140-6736(05)66552-x. PMID 15936423. Unknown parameter
|displayauthors=ignored (bantuan) - ^ Cedars-Sinai Health System – Cerebral Hemorrhages Diarkibkan 2009-03-12 di Wayback Machine Retrieved on 02/25/2009
- ^ "Decompressive craniectomy for the treatment of high intracranial pressure in closed traumatic brain injury". The Cochrane Database of Systematic Reviews. 12 (12): CD003983. December 2019. doi:10.1002/14651858.CD003983.pub3. PMC 6953357. PMID 31887790.
- ^ "Time course and predictors of neurological deterioration after intracerebral hemorrhage". Stroke. 46 (3): 647–652. March 2015. doi:10.1161/STROKEAHA.114.007704. PMC 4739782. PMID 25657190.
- ^ Sanders MJ and McKenna K. 2001. Mosby's Paramedic Textbook, 2nd revised Ed. Chapter 22, "Head and Facial Trauma." Mosby.
- ^ Graham DI and Gennareli TA. Chapter 5, "Pathology of Brain Damage After Head Injury" Cooper P and Golfinos G. 2000. Head Injury, 4th Ed. Morgan Hill, New York.
- ^ "Volume of intracerebral hemorrhage. A powerful and easy-to-use predictor of 30-day mortality". Stroke. 24 (7): 987–993. July 1993. doi:10.1161/01.STR.24.7.987. PMID 8322400.
- ^ "Guidelines for the management of spontaneous intracerebral hemorrhage in adults: 2007 update: a guideline from the American Heart Association/American Stroke Association Stroke Council, High Blood Pressure Research Council, and the Quality of Care and Outcomes in Research Interdisciplinary Working Group". Stroke. 38 (6): 2001–2023. June 2007. doi:10.1161/strokeaha.107.183689. PMID 17478736. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Long term (13 years) prognosis after primary intracerebral haemorrhage: a prospective population based study of long term mortality, prognostic factors and causes of death". Journal of Neurology, Neurosurgery, and Psychiatry. 84 (10): 1150–1155. October 2013. doi:10.1136/jnnp-2013-305200. PMID 23715913. Diarkibkan daripada yang asal pada 2014-02-22.
- ^ a b c "Incidence, case fatality, and functional outcome of intracerebral haemorrhage over time, according to age, sex, and ethnic origin: a systematic review and meta-analysis". The Lancet. Neurology. 9 (2): 167–176. February 2010. doi:10.1016/S1474-4422(09)70340-0. PMID 20056489.
- ^ Page 117 in: Schutta HS, Lechtenberg R (1998). Neurology practice guidelines. New York: M. Dekker. ISBN 978-0-8247-0104-8.
- ^ "Preclinical and clinical research on inflammation after intracerebral hemorrhage". Progress in Neurobiology. 92 (4): 463–477. December 2010. doi:10.1016/j.pneurobio.2010.08.001. PMC 2991407. PMID 20713126.
- ^ a b "Potential therapeutic targets for intracerebral hemorrhage-associated inflammation: An update". Journal of Cerebral Blood Flow and Metabolism. 40 (9): 1752–1768. September 2020. doi:10.1177/0271678X20923551. PMC 7446569. PMID 32423330. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Dynamic changes of inflammatory markers in brain after hemorrhagic stroke in humans: a postmortem study". Brain Research. 1342 (1342): 111–117. June 2010. doi:10.1016/j.brainres.2010.04.033. PMC 2885522. PMID 20420814. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Modulators of microglial activation and polarization after intracerebral haemorrhage". Nature Reviews. Neurology. 13 (7): 420–433. July 2017. doi:10.1038/nrneurol.2017.69. PMC 5575938. PMID 28524175.
- ^ "Mast cells as early responders in the regulation of acute blood-brain barrier changes after cerebral ischemia and hemorrhage". Journal of Cerebral Blood Flow and Metabolism. 30 (4): 689–702. April 2010. doi:10.1038/jcbfm.2009.282. PMC 2949160. PMID 20087366.
Pautan luar[sunting | sunting sumber]
 Media berkenaan Pendarahan otak di Wikimedia Commons
Media berkenaan Pendarahan otak di Wikimedia Commons

