Pituitari anterior
| Kelenjar pituitari anterior | |
|---|---|
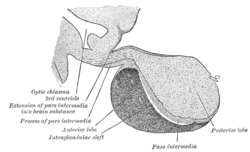 Keratan rentas sagital tengah hipofisis monyet dewasa; rajah separa. | |
| Butiran | |
| Pendahulu | Mukus mulut (kantung Rathke) |
| Arteri | Hipofisis superior |
| Urat | Hipofisis |
| Pengenalpastian | |
| nama bahasa Latin | lobus anterior hypophysis |
| MeSH | D010903 |
| NeuroNames | 407 |
| NeuroLex ID | birnlex_1581 |
| TA | A11.1.00.002 |
| FMA | FMA:74627 |
| Terminologi anatomi | |
Organ utama sistem endokrin, pituitari anterior (juga dipanggil adenohipofisis atau pars anterior) ialah kelenjar, lobus anterior yang bersama-sama dengan lobus posterior (posterior pituitari atau neurohipofisis) membentuk kelenjar pituitari (hipofisis). Pituitari anterior mengawal beberapa proses fisiologi, termasuk stres, pertumbuhan, pembiakan dan penyusuan. Fungsi yang betul dari pituitari anterior dan organ yang dikawalnya selalunya boleh dipastikan melalui ujian darah yang mengukur tahap hormon.
Struktur[sunting | sunting sumber]

Kelenjar pituitari terletak di dalam kandang tulang pelindung yang dipanggil sela tursika ("kerusi Turki"). Ia terdiri daripada tiga lobus: lobus anterior, pertengahan dan posterior. Dalam kebanyakan haiwan, lobus ini dibezakan. Walau bagaimanapun, pada manusia, lobus tengah hanyalah beberapa lapisan sel tebal dan tidak jelas; akibatnya, ia sering dianggap sebagai sebahagian daripada pituitari anterior. Dalam semua haiwan, pituitari anterior yang berkelenjar adalah berbeza daripada pituitari posterior yang lebih kepada saraf.
Pituitari anterior terdiri daripada tiga kawasan:
- Pars distalis
Pars distalis (bahagian distal) terdiri daripada sebahagian besar pituitari anterior dan merupakan tempat sebahagian besar pengeluaran hormon pituitari berlaku. Pars distalis mengandungi dua jenis sel, termasuk sel kromofob dan sel kromofil.[1] Kromofil boleh dibahagikan lagi kepada asidofil (sel alfa) dan basofil (sel beta).[1] Sel-sel ini bersama-sama menghasilkan hormon pituitari anterior dan melepaskannya ke dalam aliran darah.
- Pars tuberalis
- Pars tuberalis (bahagian bertubul) membentuk sebahagian daripada sarung yang memanjang dari pars distalis, yang bercantum dengan tangkai pituitari (juga dikenali sebagai tangkai infundibular atau infundibulum) yang timbul dari lobus posterior (tangkai pituitari menghubungkan hipotalamus ke pituitari posterior). Fungsi pars tuberalis kurang difahami. Walau bagaimanapun, ia telah diperhatikan penting dalam menerima isyarat endokrin dalam bentuk TSHB (subunit β TSH), memaklumkan pars tuberalis mengenai fotokala (panjang hari). Ekspresi subunit ini dikawal oleh rembesan melatonin sebagai tindak balas kepada maklumat cahaya yang dihantar ke kelenjar pineal.[2][3] Kajian terdahulu telah menunjukkan penyetempatan reseptor melatonin di rantau ini.[4]
- Pars intermedia
- Pars intermedia (bahagian perantaraan) terletak di antara pars distalis dan pituitari posterior, membentuk sempadan antara pituitari anterior dan posterior. Ia sangat kecil dan tidak jelas pada manusia.
Perkembangan[sunting | sunting sumber]
Pituitari anterior berasal daripada ektoderm, khususnya daripada kantung Rathke, sebahagian daripada lelangit keras yang sedang berkembang dalam embrio. Kantung Rathke juga berasal dari ektoderma.
Kantung itu akhirnya kehilangan sambungannya dengan farinks, menerbitkan pituitari anterior. Dinding anterior kantung Rathke membiak, memenuhi kebanyakan kantung untuk membentuk pars distalis dan pars tuberalis. Dinding posterior pituitari anterior membentuk pars intermedia. Pembentukannya daripada tisu lembut lelangit atas berbeza dengan pituitari posterior yang berasal dari neuroektoderma.[5]
Fungsi[sunting | sunting sumber]
Pituitari anterior mengandungi lima jenis sel endokrin, dan ia ditakrifkan oleh hormon yang dirembeskannya: somatotrop (GH); laktotrop (PRL); gonadotrop (LH dan FSH); kortikotrop (ACTH) dan tirotrop (TSH). [6] Ia juga mengandungi sel folikulostelat bukan endokrin yang dianggap merangsang dan menyokong populasi sel endokrin.
Hormon yang dirembeskan oleh pituitari anterior ialah hormon trofik (Yunani: trophe, "perkembangan"). Hormon trofik secara langsung menjejaskan pertumbuhan sama ada sebagai hiperplasia atau hipertrofi pada tisu yang dirangsangnya. Hormon trofik dinamakan kerana keupayaannya untuk bertindak secara langsung pada tisu sasaran atau kelenjar endokrin lain untuk membebaskan hormon, menyebabkan banyak tindak balas fisiologi yang melata.[5]
| Hormon | Nama lain | Simbol | Struktur | Sel rembesan | mengotorkan | Sasaran | Kesan |
|---|---|---|---|---|---|---|---|
| Hormon adrenokortikotropik | Kortikotropin | ACTH | Polipeptida | Kortikotrof | Basofil | Kelenjar adrenal | Rembesan glukokortikoid, mineralokortikoid dan androgen |
| Hormon perangsang tiroid | Tirotropin | TSH | Glikoprotein | Thyrotrophs | Basofil | Kelenjar tiroid | Rembesan hormon tiroid |
| Hormon perangsang folikel | - | FSH | Glikoprotein | Gonadotrof | Basofil | Gonad | Pertumbuhan sistem pembiakan |
| Hormon peluteinan | Lutropin | LH, ICSH | Glikoprotein | Gonadotrof | Basofil | Gonad | Pengeluaran hormon seks |
| Hormon pertumbuhan | Somatotropin | GH, STH | Polipeptida | Somatotrof | Asidofil | Hati, tisu adipos | Menggalakkan pertumbuhan; metabolisme lipid dan karbohidrat |
| Prolaktin | Laktotropin | PRL | Polipeptida | Laktotrof | Asidofil | Ovari, kelenjar susu, testis, prostat | Rembesan estrogen / progesteron; penyusuan susu ibu; spermatogenesis; hiperplasia prostat |
Peranan dalam sistem endokrin[sunting | sunting sumber]
Kawalan hipotalamus[sunting | sunting sumber]
Rembesan hormon dari kelenjar pituitari anterior dikawal oleh hormon yang dirembeskan oleh hipotalamus. Sel neuroendokrin dalam hipotalamus memproyeksikan akson ke median eminence di pangkal otak. Di tapak ini, sel-sel ini boleh melepaskan bahan ke dalam saluran darah kecil yang bergerak terus ke kelenjar pituitari anterior (saluran portal hipotalamus-hipofisis).
Mekanisme lain[sunting | sunting sumber]
Selain daripada kawalan hipotalamus pada pituitari anterior, sistem lain dalam badan telah ditunjukkan untuk mengawal fungsi pituitari anterior. GABA sama ada boleh merangsang atau menghalang rembesan hormon peluteinan (LH) dan hormon pertumbuhan (GH) dan boleh merangsang rembesan hormon perangsang tiroid (TSH). Prostaglandin kini dikenali untuk menghalang hormon adrenokortikotropik (ACTH) dan juga merangsang pelepasan TSH, GH dan LH.[7] Bukti klinikal menyokong penemuan eksperimen kesan rangsangan dan perencatan GABA terhadap rembesan GH, bergantung pada tapak tindakan GABA dalam paksi hipotalamus-pituitari.[8]
Kesan pituitari anterior[sunting | sunting sumber]
- Homeostasis haba
Penyelenggaraan homeostatik pituitari anterior adalah penting dalam kebolehan fisiologi. Peningkatan tahap plasma TSH mendorong hipertermia melalui mekanisme yang melibatkan peningkatan metabolisme dan vasodilatasi kulit. Peningkatan tahap LH juga mengakibatkan hipotermia, tetapi melalui penurunan tindakan metabolisme. ACTH meningkatkan metabolisme dan menyebabkan vasokonstriksi kulit, peningkatan paras plasma, juga mengakibatkan hipertermia dan pengurangan prolaktin dengan penurunan nilai suhu. Hormon perangsang folikel (FSH) juga boleh menyebabkan hipotermia jika meningkat melebihi tahap homeostatik melalui peningkatan mekanisme metabolik semata-mata.[9]
- Fungsi gonad
Gonadotrop, terutamanya hormon peluteinan (LH) yang dirembeskan daripada pituitari anterior merangsang kitaran ovulasi dalam mamalia betina, manakala pada lelaki, LH merangsang sintesis androgen yang mendorong kehendak berterusan untuk mengawan bersama-sama pengeluaran sperma yang berterusan.[5]
- Paksi adrenal
Pituitari anterior memainkan peranan dalam tindak balas tekanan. Hormon pelepasan kortikotropin (CRH) daripada hipotalamus merangsang pembebasan ACTH dalam kesan melata yang berakhir dengan penghasilan glukokortikoid di korteks adrenal.[5]
Kesan tingkah laku[sunting | sunting sumber]
- Tumbesaran
- Pembebasan GH, LH, dan FSH diperlukan dalam tumbesaran manusia yang betul, termasuk perkembangan gonad.[10]
- Tekanan
- Beroperasi melalui paksi hipotalamus-pituitari-adrenal (HPA), kelenjar pituitari anterior mempunyai peranan yang besar dalam tindak balas tekanan sistem neuroendokrin. Tekanan mendorong pembebasan hormon pelepasan kortikotropin (CRH) dan vasopresin daripada hipotalamus, yang mengaktifkan pembebasan hormon adrenokortikotropik (ACTH) daripada kelenjar pituitari anterior. Kemudian, ini bertindak pada korteks adrenal untuk menghasilkan glukokortikoid seperti kortisol. Glukokortikoid ini bertindak semula pada kelenjar pituitari anterior dan hipotalamus dengan maklum balas negatif untuk memperlahankan pengeluaran CRH dan ACTH.[11][12] Peningkatan kortisol dalam keadaan tekanan boleh menyebabkan yang berikut: kesan metabolik (penggunaan glukosa, asid lemak dan asid amino), penyerapan semula tulang (penggunaan kalsium), pengaktifan tindak balas sistem saraf simpatetik (lawan atau lari) kesan antiradang dan perencatan pembiakan/pertumbuhan.[10] Apabila kelenjar pituitari anterior dikeluarkan (hipofisektomi) pada tikus, mekanisme pembelajaran pengelakan mereka menjadi perlahan, tetapi suntikan ACTH memulihkan prestasi mereka.[10] Di samping itu, stres boleh melambatkan pembebasan hormon pembiakan seperti hormon peluteinan (LH) dan hormon perangsang folikel (FSH).[13] Ini menunjukkan bahawa kelenjar pituitari anterior terlibat dalam fungsi tingkah laku serta menjadi sebahagian daripada laluan yang lebih besar untuk tindak balas tekanan. Juga diketahui bahawa hormon (HPA) berkaitan dengan penyakit kulit tertentu dan homeostasis kulit. Terdapat bukti yang mengaitkan hormon HPA hiperaktif dengan penyakit dan tumor kulit berkaitan stres.[14]
- Penuaan
- Beroperasi melalui paksi hipotalamus-pituitari-gonad, kelenjar pituitari anterior juga mempengaruhi sistem pembiakan . Hipotalamus mengeluarkan hormon pelepasan gonadotropin (GnRH), yang merangsang pembebasan hormon peluteinan (LH) dan hormon perangsang folikel. Kemudian, gonad menghasilkan estrogen dan testosteron . Penurunan pembebasan gonadotropin (LH dan FSH) yang disebabkan oleh penuaan normal mungkin menyebabkan mati pucuk[10][13] dan kelemahan[15] pada lelaki tua kerana penurunan dalam pengeluaran testosteron. Tahap testosteron yang lebih rendah ini boleh memberi kesan lain, seperti penurunan libido, kesejahteraan, kekuatan otot dan tulang, dan metabolisme.[13]
- Tindak balas sentuhan
- Kajian menunjukkan bahawa bayi tikus yang dibelai dengan berus cat (meniru penjagaan ibu) mempunyai lebih banyak pelepasan dan pengikatan hormon pertumbuhan (GH) daripada kelenjar pituitari anterior.[10]
- Irama sirkadian
- Maklumat cahaya yang diterima oleh mata dihantar ke kelenjar pineal melalui perentak sirkadian (nukleus suprakiasma). Cahaya yang semakin berkurangan merangsang pembebasan melatonin daripada kelenjar pineal yang juga boleh menjejaskan tahap rembesan dalam paksi hipotalamus-pituitari-gonad.[10] Melatonin boleh menurunkan tahap LH dan FSH, yang akan mengurangkan tahap estrogen dan testosteron. Di samping itu, melatonin boleh menjejaskan pengeluaran prolaktin.[16]
Kepentingan klinikal[sunting | sunting sumber]
Peningkatan aktiviti[sunting | sunting sumber]
Hiperpituitarisme ialah keadaan di mana pituitari merembeskan jumlah hormon yang berlebihan. Hipersecretion ini selalunya mengakibatkan pembentukan adenoma (tumor) pituitari, yang bersifat setempat kecuali pecahan kecil. Secara utama, terdapat tiga jenis tumor pituitari anterior dan gangguan yang berkaitan dengannya. Sebagai contoh, akromegali terhasil daripada rembesan GH yang berlebihan yang sering dikeluarkan oleh adenoma pituitari. Gangguan ini boleh menyebabkan kecacatan dan kematian mungkin,[17] dan boleh membawa kepada gigantisme, gangguan hormon yang ditunjukkan dalam "gergasi" seperti André Si Gergasi, di mana ia berlaku sebelum plat epifisis dalam tulang tutup dalam akil baligh.[10] Jenis tumor pituitari yang paling biasa ialah prolaktinoma yang merembeskan prolaktin.[18] Adenoma pituitari jenis ketiga merembeskan ACTH secara berlebihan, yang seterusnya, menyebabkan kortisol dirembes terlalu banyak, dan menjadi punca penyakit Cushing.[10]
Pengurangan aktiviti[sunting | sunting sumber]
Hipopituitarisme dicirikan oleh penurunan rembesan hormon yang dikeluarkan oleh pituitari anterior. Contohnya, hiporembesan GH sebelum baligh boleh menjadi punca badan kerdil. Di samping itu, kekurangan adrenal sekunder boleh disebabkan oleh hiporembesan ACTH yang, seterusnya, tidak memberi isyarat kepada korteks adrenal untuk menghasilkan jumlah kortisol yang mencukupi. Ini adalah keadaan yang mengancam nyawa. Hipopituitarisme juga boleh disebabkan oleh pemusnahan atau penyingkiran tisu pituitari anterior melalui trauma otak, tumor, batuk kering atau sifilis, antara punca lain. Gangguan ini dahulunya dirujuk sebagai "penyakit Simmonds" tetapi kini dipanggil sindrom Sheehan menurut Pangkalan Data Penyakit.[19] Jika hipopituitarisme berlaku disebabkan oleh kehilangan darah yang berkaitan dengan bersalin, gangguan itu dirujuk sebagai sindrom Sheehan.
Sejarah[sunting | sunting sumber]
Etimologi[sunting | sunting sumber]
Pituitari anterior juga dikenali sebagai adenohipofisis, yang bermaksud "kelenjar semak", daripada bahasa Yunani adeno- ("kelenjar"), hypo ("di bawah"), dan physis ("pertumbuhan").
Rujukan[sunting | sunting sumber]
- ^ a b Eroschenko, Victor P.; Fiore, Mariano S. H. di (2013-01-01). DiFiore's Atlas of Histology with Functional Correlations (dalam bahasa Inggeris). Lippincott Williams & Wilkins. ISBN 9781451113419.
- ^ Ikegami, K; Iigo, M; Yoshimura, T (2013). "Circadian clock gene Per2 is not necessary for the photoperiodic response in mice". PLOS ONE. 8 (3): e58482. Bibcode:2013PLoSO...858482I. doi:10.1371/journal.pone.0058482. PMC 3591342. PMID 23505514.
- ^ Dardente, H (2012). "Melatonin-dependent timing of seasonal reproduction by the pars tuberalis: pivotal roles for long daylengths and thyroid hormones". Journal of Neuroendocrinology. 24 (2): 249–66. doi:10.1111/j.1365-2826.2011.02250.x. PMID 22070540.
- ^ Morgan, PJ; Williams, LM (1996). "The pars tuberalis of the pituitary: a gateway for neuroendocrine output". Reviews of Reproduction. 1 (3): 153–61. doi:10.1530/ror.0.0010153. PMID 9414453.
- ^ a b c d Nelson, R. J. (2011) An Introduction to Behavioral Endocrinology, 4th Edition. Sunderland, MA: Sinauer Associates, Inc.ISBN 978-0878936205
- ^ Le Tissier, P.R; Hodson, D.J; Lafont C; Fontanaud P; Schaeffer, M; Mollard, P. (2012) Anterior pituitary cell networks. Front Neuroendocrinol. Aug; 33(3):252-66
- ^ Hedge, G.A. (1977) Roles for the prostaglandins in the regulation of anterior pituitary secretion. Life Sci. Jan 1;20(1):17-33.
- ^ Racagni, G; Apud, J.A; Cocchi, D; Locatelli, V; Muller, E.E. (1982) GABAergic control of anterior pituitary hormone secretion. Life Sci. Aug 30;31(9):823-38.
- ^ Lin, M.T; Ho, L.T; and Uang, W.N. (1983) Effects of anterior pituitary hormones and their releasing hormones physiological and behavioral functions in rats. J. steroid Biochem. Vol. 19(1) 433-38.
- ^ a b c d e f g h i Nelson, Randy J. (2011). An introduction to behavioral endocrinology (ed. 4th). Sunderland, Massachusetts: Sinauer Associates. ISBN 978-0878936205.
- ^ Aguilera, Greti (1998-10-01). "Corticotropin Releasing Hormone, Receptor Regulation and the Stress Response". Trends in Endocrinology & Metabolism. 9 (8): 329–336. doi:10.1016/S1043-2760(98)00079-4. ISSN 1043-2760. PMID 18406298.
- ^ Aguilera, Greti (December 1994). "Regulation of Pituitary ACTH Secretion during Chronic Stress". Frontiers in Neuroendocrinology. 15 (4): 321–350. doi:10.1006/frne.1994.1013. ISSN 0091-3022. PMID 7895891.
- ^ a b c Dobson, H; R F Smith (2000-07-02). "What is stress, and how does it affect reproduction?". Animal Reproduction Science. 60–61: 743–752. doi:10.1016/s0378-4320(00)00080-4. ISSN 0378-4320. PMID 10844239.
- ^ Jung Eun Kim; Baik Kee Cho; Dae Ho Cho; Hyun Jeong Park (2013). "Expression of Hypothalamic-Pituitary-Adrenal Axis in Common Skin Diseases: Evidence of its Association with Stress-related Disease Activity". National Research Foundation of Korea. Dicapai pada 4 March 2014.
- ^ Tajar, Abdelouahid; O'Connell, Matthew D L; Mitnitski, Arnold B; O'Neill, Terence W; Searle, Samuel D; Huhtaniemi, Ilpo T; Finn, Joseph D; Bartfai, György; Boonen, Steven (May 2011). "Frailty in relation to variations in hormone levels of the hypothalamic-pituitary-testicular axis in older men: results from the European male aging study". Journal of the American Geriatrics Society. 59 (5): 814–821. doi:10.1111/j.1532-5415.2011.03398.x. ISSN 1532-5415. PMID 21568952.
- ^ Juszczak, Marlena; Monika Michalska (2006). "[The effect of melatonin on prolactin, luteinizing hormone (LH), and follicle-stimulating hormone (FSH) synthesis and secretion]". Postępy Higieny I Medycyny Doświadczalnej. 60: 431–438. ISSN 1732-2693.
- ^ Scacchi, Massimo; Francesco Cavagnini (2006). "Acromegaly". Pituitary. 9 (4): 297–303. doi:10.1007/s11102-006-0409-4. ISSN 1573-7403. PMID 17077948.
- ^ Ciccarelli, E; F Camanni (June 1996). "Diagnosis and drug therapy of prolactinoma". Drugs. 51 (6): 954–965. doi:10.2165/00003495-199651060-00004. ISSN 0012-6667. PMID 8736617.
- ^ Summers, V. K. (September 1947). "Diagnosis and Treatment of Simmonds' Disease". Postgraduate Medical Journal. 23 (263): 441–443. doi:10.1136/pgmj.23.263.441. ISSN 0032-5473. PMC 2529616. PMID 20258051.
