Asid fosforus
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
phosphonic acid
| |||
| Nama lain
Dihidroksifosfina oksida
Dihidroksi(okso)-λ5-fosfana | |||
| Pengecam | |||
Imej model 3D Jmol
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.033.682 | ||
| KEGG | |||
| Nombor RTECS |
| ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| H3PO3 | |||
| Jisim molar | 82.00 g/mol | ||
| Rupa bentuk | pepejal putih lembap cair | ||
| Ketumpatan | 1.651 g/cm3 (21 °C) | ||
| Takat lebur | 73.6 °C (164.5 °F; 346.8 K) | ||
| Takat didih | 200 °C (392 °F; 473 K) | ||
| 310 g/100 mL | |||
| Keterlarutan | larut dalam alkohol | ||
| Keasidan (pKa) | 1.3, 6.7 | ||
| Struktur | |||
| Bentuk molekul | tetrahedral | ||
| Bahaya | |||
| Bahaya-bahaya utama | skin irritant | ||
| Frasa R | 22-35 | ||
| Frasa S | 26-36/37/39-45 | ||
| NFPA 704 (berlian api) | |||
| Sebatian berkaitan | |||
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |||
| | |||
| Rujukan kotak info | |||
Asid fosforus merupakan sejenis sebatian diterangkan melalui formula H3PO3. Asid ini bersifat diprotik (mudah mengionkan dua proton), bukan triprotik seperti yang mungkin dicadangkan oleh formula ini. Asid fosforus adalah perantara dalam penyediaan sebatian fosforus lain.
Tatanama dan tautomerisme[sunting | sunting sumber]
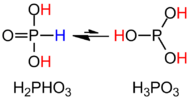
H3PO3 adalah lebih jelas untuk dihuraikan dengan formula strukturnya HPO(OH)2. Spesies ini wujud dalam keseimbangan dengan tautomer P(OH)3 yang kecil. Pengesyoran IUPAC, 2005, bahawa yang kedua dipanggil asid fosforus, manakala bentuk dihidroksi dipanggil asid fosfonik.[1] Hanya sebatian fosforus yang diturunkan dieja menggunakan "us" sebagai imbuhan akhir.
Tautomer P(OH)3 telah diperhatikan sebagai suatu ligand terikat kepada molibdenum.[2][3] Oksiasid fosforus lain yang juga penting adalah asid fosforik (H3PO4) dan asid hidrofosforus (H3PO2). Asid-asid fosforus yang diturunkan tertakluk kepada tautomerisme yang seiras termasuk peralihan daripada H antara O dan P.
Rujukan[sunting | sunting sumber]
- ^ International Union of Pure and Applied Chemistry (2005). Nomenclature of Inorganic Chemistry (IUPAC Recommendations 2005). Cambridge (UK): RSC–IUPAC. ISBN 0-85404-438-8. Electronic version..
- ^ Chanjuan Xi, Yuzhou Liu, Chunbo Lai, Lishan Zhou (2004). "Synthesis of molybdenum complex with novel P(OH)3 ligand based on the one-pot reaction of Mo(CO)6 with HP(O)(OEt)2 and water". Inorganic Chemistry Communications. 7 (11): 1202. doi:10.1016/j.inoche.2004.09.012.CS1 maint: multiple names: authors list (link)
- ^ M. N. Sokolov, E. V. Chubarova, K. A. Kovalenko, I. V. Mironov, A. V. Virovets1, E. V. Peresypkina,V. P. Fedin (2005). "Stabilization of tautomeric forms P(OH)3 and HP(OH)2 and their derivatives by coordination to palladium and nickel atoms in heterometallic clusters with the Mo3MQ44+ core (M = Ni, Pd; Q = S, Se)". Russian Chemical Bulletin. 54 (3): 615. doi:10.1007/s11172-005-0296-1.CS1 maint: multiple names: authors list (link)
Bacaan lanjutan[sunting | sunting sumber]
- Holleman, A. F.; Wiberg, E. “Inorganic Chemistry.” Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- D. E. C. Corbridge. “Phosphorus: An Outline of its Chemistry, Biochemistry, and Technology.” 5th ed. Elsevier: Amsterdam. ISBN 0-444-89307-5.
- Concise Inorganic Chemistry J.D.Lee Oxford University Press ISBN 978-81-265-1554-7



