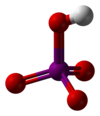
Asid periodik
| |||
| Nama | |||
|---|---|---|---|
| Nama lain
Asid paraperiodik
| |||
| Pengecam | |||
Imej model 3D Jmol
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.030.839 | ||
PubChem CID
|
|||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| H5IO6 | |||
| Jisim molar | 227.941 g/mol | ||
| Rupa bentuk | Kristal tidak berwarna | ||
| Takat lebur | 122 °C (252 °F; 395 K) | ||
| Bahaya | |||
| Pengelasan EU | {{{value}}} | ||
| Frasa R | Templat:R23 Templat:R24 Templat:R25 Templat:R34 Templat:R41 | ||
| NFPA 704 (berlian api) | |||
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |||
| | |||
| Rujukan kotak info | |||
| |||
| Nama | |||
|---|---|---|---|
| Nama lain
Asid periodik
| |||
| Pengecam | |||
Imej model 3D Jmol
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.030.839 | ||
PubChem CID
|
|||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| HIO4 | |||
| Jisim molar | 190.91 g/mol | ||
| Rupa bentuk | Kristal tidak berwarna | ||
| Takat lebur | 122 °C (252 °F; 395 K) | ||
| Bahaya | |||
| Pengelasan EU | {{{value}}} | ||
| Frasa R | Templat:R23 Templat:R24 Templat:R25 Templat:R34 Templat:R41 | ||
| NFPA 704 (berlian api) | |||
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |||
| | |||
| Rujukan kotak info | |||
Asid periodik,[1] atau asid iodik(VII)[2] ialah sejenis oksoasid iodin dengan formula kimia HIO4 atau H5IO6.
Dalam larutan akua cair, asid periodik wujud dalam bentuk ion hidronium (H3O+) dan ion metaperiodat (IO−
4) secara berasingan. Apabila dipekatkan, asid ortoperiodik dibentuk. Ia berpisah kepada ion hidronium dan ion ortoperiodat (IO5−
6). Pada praktiknya, ion metaperiodat dan ion ortoperiodat ini wujud bersama-sama dalam keseimbangan kimia yang bergantung pada pH:
- IO−
4 + 6 H2O IO5−
IO5−
6 + 4 H3O+
Asid ortoperiodik boleh diperolehi dalam bentuk pepejal kristal yang boleh dinyahhidratkan kepada asid metaperiodik, HIO4. Pemanasan selanjutnya memberikan diiodin pentoksida (I2O5) dan oksigen dan bukannya anhidrida yang diramalkan, diiodin heptoksida. Anhidrida ini tidak wujud secara semula jadi tetapi boleh dihasilkan secara sintetik.
Oleh kerana terdapat dua jenis asid periodik, dua jenis garam periodat yang berbeza boleh dihasilkan. Contohnya, natrium metaperiodat, NaIO4, boleh disintesis daripada HIO4, manakala natrium ortoperiodat, Na5IO6 boleh disintesis daripada H5IO6. Sebatian metaperiodat mempunyai keterlarutan dan ciri-ciri kimia yang serupa dengan perklorat (serupa tetapi dengan saiz ion lebih besar) tetapi sebatian-sebatian ini kurang mengoksida berbanding perklorat.
Asid periodik digunakan dalam kimia organik untuk analisa struktur. Asid periodik akan membelah diol-diol visinal kepada dua pecahan aldehid atau keton. Ini boleh digunakan dalam menentukan struktur karbohidrat. Ia juga boleh digunakan dalam sintesis organik sebagai agen pengoksida dengan kuasa sederhana.
Rujukan[sunting | sunting sumber]
- ^ Nama ini tidak diterbitkan daripada perkataan "period" (kala), tetapi daripada "iodine" (iodin): asid per-iodik (bandingkan dengan asid iodik, asid perklorik), dan oleh itu sebutannya ialah per-iodik /ˌpɜːr.aɪˈɒdᵻk/PURR-eye-OD-ik, dan bukannya /ˌpɪərɪˈɒdᵻk/PEER-ee-OD-ik.
- ^ Alan Isaacs, John Daintith, Elizabeth Martin, penyunting (1984). Concise Science Dictionary. Oxford: Oxford University Press. m/s. 356. ISBN 0-19-211593-6.CS1 maint: multiple names: editors list (link)