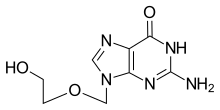
Asiklovir
 | |
 | |
| Data klinikal | |
|---|---|
| Nama dagang | Zovirax, lain-lain[1] |
| Nama lain | Asikloguanosina, acyclovir (BAN UK), acyclovir (USAN AS) |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a681045 |
| Data lesen | |
| Kategori kehamilan |
|
| Kaedah pemberian | Intravena, mulut, topikal, titisan mata |
| Kod ATC | |
| Status perundangan | |
| Status perundangan |
|
| Data farmakokinetik | |
| Bioketersediaan | 15–20% (mulut)[2] |
| Pengikatan protein | 9–33%[2] |
| Metabolisme | Hati |
| Penyingkiran separuh hayat | 2–4 jam |
| Perkumuhan | Buah pinggang (62–90% tidak berubah) |
| Pengecam | |
| |
| Nombor CAS | |
| PubChem CID | |
| PubChem SID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Ligan PDB | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.056.059 |
| Data kimia dan fizikal | |
| Formula | C8H11N5O3 |
| Jisim molar | 225.21 g·mol−1 |
| Model 3D (JSmol) | |
| Takat lebur | 256.5 °C (493.7 °F) |
| |
| |
| (verify) | |
Asiklovir (ACV) ialah ubat antivirus.[3] Ia digunakan terutamanya dalam rawatan jangkitan virus herpes simplex, cacar air, dan kayap.[4] Kegunaan lain termasuk pencegahan jangkitan sitomegalovirus berikutan pemindahan dan komplikasi teruk jangkitan virus Epstein-Barr.[4][5] Ia boleh diambil melalui mulut, digunakan sebagai krim, atau disuntik.[4]
Kesan sampingan yang biasa termasuk loya dan cirit-birit.[4] Kesan sampingan yang berpotensi serius termasuk masalah buah pinggang dan platelet rendah.[4] Penjagaan yang lebih baik disyorkan kepada mereka yang mempunyai fungsi hati atau buah pinggang yang lemah.[4] Ia secara amnya dianggap selamat untuk digunakan semasa kehamilan tanpa sebarang bahaya telah diperhatikan.[4][6] Nampaknya selamat semasa menyusu.[7][8] Asiklovir ialah analog nukleosida yang meniru guanosina.[4] Ia berfungsi dengan mengurangkan pengeluaran DNA virus.[4]
Asiklovir telah dipatenkan pada 1974 oleh Burroughs Wellcome, dan diluluskan untuk kegunaan perubatan pada 1981.[9] Ia berada dalam Senarai Ubat Penting Pertubuhan Kesihatan Sedunia.[10][11] Ia boleh didapati sebagai ubat generik dan dipasarkan di bawah banyak jenama di seluruh dunia.[1] Pada 2020, ia adalah ubat ke-162 yang paling kerap dipreskripsi di Amerika Syarikat, dengan lebih daripada 3 juta preskripsi.[12][13]
Penggunaan perubatan
[sunting | sunting sumber]
Asiklovir digunakan untuk rawatan virus herpes simplex (HSV) dan jangkitan virus varicella zoster, termasuk:[2][14][15]
- Herpes simplex kelamin (rawatan dan pencegahan)
- Herpes simpleks neonatal
- Herpes simplex labialis (luka selsema)
- Kayap
- Cacar air akut dalam pesakit imunokompromi
- Herpes simplex ensefalitis
- Jangkitan HSV mukokutaneus akut dalam pesakit lemah imun
- Herpes mata dan herpes simplex blefaritis (bentuk jangkitan mata herpes kronik (jangka panjang))
- Pencegahan virus herpes pada orang yang lemah imun (seperti orang yang menjalani kemoterapi kanser)[16]
Keberkesanannya dalam merawat jangkitan virus Epstein-Barr (EBV) adalah kurang jelas.[4] Ia tidak didapati berguna bagi mononukleosis berjangkit akibat EBV.[17] Valasiklovir dan asiklovir bertindak dengan menghalang replikasi DNA virus, tetapi sehingga 2016, terdapat sedikit bukti bahawa ia berkesan terhadap virus Epstein-Barr; ia mahal dan ia berisiko menyebabkan ketahanan terhadap agen antivirus, dan (dalam 1% hingga 10% kes) boleh menyebabkan kesan sampingan yang tidak menyenangkan.[18]
Asiklovir yang diambil melalui mulut nampaknya tidak mengurangkan risiko sakit selepas kayap.[19] Bagi mereka yang menghidap herpes mata, asiklovir mungkin lebih berkesan dan lebih selamat daripada idoksuridina.[20] Tidak jelas sama ada titisan mata asiklovir lebih berkesan daripada titisan mata brivudina.[20]
Asiklovir intravena berkesan untuk merawat keadaan perubatan yang teruk yang disebabkan oleh spesies berlainan keluarga virus herpes, termasuk jangkitan tempatan yang teruk bagi virus herpes, herpes genital yang teruk, cacar air dan ensefalitis herpesvirus. Ia juga berkesan dalam jangkitan herpes sistemik atau traumatik, ekzema herpetikum dan meningitis herpesvirus. Ulasan penyelidikan sejak 1980-an menunjukkan terdapat beberapa kesan dalam mengurangkan bilangan dan tempoh lesi jika asiklovir digunakan pada peringkat awal wabak.[21] Penyelidikan menunjukkan keberkesanan asiklovir topikal dalam kedua-dua peringkat awal dan akhir wabak serta bertambah baik dari segi metodologi dan dari segi kepastian statistik daripada kajian terdahulu.[22] Percubaan asiklovir menunjukkan bahawa ejen ini tidak mempunyai peranan dalam mencegah penularan HIV, tetapi ia boleh membantu memperlahankan perkembangan penyakit HIV pada orang yang tidak mengambil terapi antiretrovirus (ART). Penemuan ini menekankan kepentingan menguji strategi bukan ART yang mudah dan murah, seperti asiklovir dan kotrimoksazola, pada orang yang menghidap HIV.[23]
Kehamilan
[sunting | sunting sumber]Dikelaskan sebagai ubat Kategori B,[24] CDC dan lain-lain telah mengisytiharkan bahawa semasa episod herpes kelamin berulang atau pertama yang teruk, asiklovir boleh digunakan.[25] Bagi jangkitan HSV yang teruk (terutama HSV yang disebarkan), asiklovir IV juga boleh digunakan.[26]
Kajian terhadap tikus, dan arnab dan (dengan dos lebih daripada 10 kali ganda bersamaan dengan yang digunakan pada manusia) yang diberikan semasa organogenesis telah gagal menunjukkan kecacatan kelahiran.[27] Kajian ke atas tikus, di mana mereka diberi bersamaan dengan 63 kali kepekatan berian ubat piawaian terhadap manusia[Nota 1] pada hari ke-10 kehamilan menunjukkan kecacatan di kepala dan ekor.[27]
Asiklovir disyorkan oleh CDC untuk rawatan cacar air semasa kehamilan, terutamanya semasa trimester kedua dan ketiga.[28]
Asiklovir dikumuhkan dalam susu ibu, oleh itu adalah disyorkan bahawa langkah berhati-hati harus digunakan pada wanita yang menyusu. Telah ditunjukkan dalam kajian ujian terhad bahawa bayi penyusuan terdedah kepada kira-kira 0.3 mg/kg/hari selepas pemberian oral asiklovir kepada ibu. Jika ibu yang menyusu mempunyai lesi herpes berhampiran atau pada payudara, penyusuan susu ibu harus dielakkan.[24][29]
Kesan buruk
[sunting | sunting sumber]Terapi sistemik
[sunting | sunting sumber]Reaksi buruk ubat lazim (≥1% pesakit) yang dikaitkan dengan terapi asiklovir sistemik (oral atau IV) termasuk loya, muntah, cirit-birit, ensefalopati (dengan penggunaan IV sahaja), tindak balas tapak suntikan (dengan penggunaan IV sahaja) dan sakit kepala. Dalam dos yang tinggi, halusinasi telah dilaporkan. Kesan buruk yang jarang berlaku (0.1–1% pesakit) termasuk gelisah, vertigo, kekeliruan, pening, edema, arthralgia, sakit tekak, sembelit, sakit perut, keguguran rambut, ruam dan kelemahan. Kesan buruk yang jarang berlaku (<0.1% pesakit) termasuk koma, sawan, neutropenia, leukopenia, kristaluria, anoreksia, keletihan, hepatitis, sindrom Stevens–Johnson, nekrolisis epidermis toksik, Purpura trombositopenik trombotik, sindrom anafilaksis,[14] dan sindrom Cotard.
Asiklovir intravena boleh menyebabkan nefrotoksisiti boleh balik dalam 5% hingga 10% pesakit kerana pemendakan kristal asiklovir dalam buah pinggang. Nefropati kristal asiklovir adalah lebih biasa apabila asiklovir diberikan sebagai infusi cepat dan pada pesakit yang mengalami dehidrasi dan kerosakan buah pinggang yang sedia ada. Penghidratan yang mencukupi, kadar infusi yang lebih perlahan, dan dos berdasarkan fungsi buah pinggang boleh mengurangkan risiko ini.[30][31][32]
Metabolit asiklovir 9-karboksimetoksimetilguanina (9-CMMG) telah ditunjukkan memainkan peranan dalam kejadian neurologi buruk, terutamanya pada orang tua dan mereka yang mempunyai fungsi buah pinggang yang rendah.[33][34][35]
Terapi topikal
[sunting | sunting sumber]Krim topikal asiklovir biasanya dikaitkan (≥1% pesakit) dengan: kulit kering atau mengelupas atau rasa pedih/terbakar sementara. Kesan buruk yang jarang berlaku termasuk eritema atau gatal-gatal.[14] Apabila disapu pada mata, asiklovir biasanya dikaitkan (≥1% pesakit) dengan rasa pedih ringan sementara. Dalam kes langka (0.1–1% pesakit), asiklovir oftalmik dikaitkan dengan keratitis punktat cetek atau tindak balas alahan.[14]
Interaksi dadah
[sunting | sunting sumber]Ketokonazola: Kajian replikasi in vitro telah menemui aktiviti antivirus yang sinergistik, bergantung kepada dos terhadap HSV-1 dan HSV-2 apabila diberikan bersama asiklovir. Walau bagaimanapun, kesan ini belum ditubuhkan secara klinikal dan lebih banyak kajian perlu dilakukan untuk menilai potensi sebenar sinergi ini.[36]
Probenesid: Laporan peningkatan separuh hayat asiklovir serta penurunan perkumuhan air kencing dan pembersihan buah pinggang telah ditunjukkan dalam kajian di mana probenesid diberikan serentak dengan asiklovir.[24]
Interferon: Kesan sinergistik apabila diberikan dengan asiklovir, dan langkah berhati-hati perlu diambil apabila memberikan asiklovir kepada pesakit yang menerima interferon IV.[37]
Zidovudina: Walaupun sering diberikan dengan asiklovir dalam pesakit HIV, neurotoksisiti telah dilaporkan dalam sekurang-kurangnya seorang pesakit yang mengalami rasa mengantuk dan lesu yang melampau 30–60 hari selepas menerima asiklovir IV; gejala hilang apabila pengambilan asiklovir dihentikan.[38]
Pengesanan dalam cecair biologi
[sunting | sunting sumber]Asiklovir boleh dikuantisasi dalam plasma atau serum untuk memantau pengumpulan ubat pada pesakit dengan disfungsi buah pinggang atau untuk mengesahkan diagnosis keracunan pada mangsa dos berlebihan akut.[39]
Mekanisme tindakan
[sunting | sunting sumber]

Asiklovir ditukar oleh kinase timidina virus menjadi asiklovir monofosfat, yang kemudiannya ditukarkan oleh kinase sel perumah kepada asiklovir trifosfat (ACV-TP, juga dikenali sebagai asiklo-GTP).[27] ACV-TP ialah perencat replikasi DNA virus yang sangat kuat. ACV-TP secara bersaingan menghalang dan menyahaktifkan polimerase DNA virus.[40] Bentuk monofosfatnya juga digabungkan ke dalam DNA virus, mengakibatkan penamatan rantai.[27][41][42]
Kerintangan
[sunting | sunting sumber]Rintangan terhadap asiklovir jarang berlaku pada orang yang mempunyai sistem imun yang sihat, tetapi lebih biasa (sehingga 10%) pada orang yang mengalami kekurangan imun pada profilaksis antivirus kronik (penerima pemindahan, orang yang mengalami sindrom kekurangan imun diperoleh akibat jangkitan HIV). Mekanisme rintangan dalam HSV termasuk kekurangan kinase timidina virus; dan mutasi kinase timidina virus atau polimerase DNA lalu mengubah sensitiviti substrat.[43][44]
Mikrobiologi
[sunting | sunting sumber]
Asiklovir aktif terhadap kebanyakan spesies keluarga herpesvirus. Dalam susunan aktiviti menurun:[45][46]
- Virus herpes simplex jenis I (HSV-1)
- Virus herpes simplex jenis II (HSV-2)
- Virus Varicella zoster (VZV)
- Virus Epstein-Barr (EBV)
- Sitomegalovirus manusia (HCMV) – aktiviti paling sedikit
Farmakokinetik
[sunting | sunting sumber]Asiklovir kurang larut dalam air dan mempunyai bioketersediaan oral yang lemah (15-30%), dan oleh itu, pentadbiran intravena diperlukan jika kepekatan tinggi diperlukan. Apabila diberi melalui mulut, kepekatan plasma puncak berlaku selepas 1-2 jam. Menurut Sistem Pengelasan Biofarmaseutikal (BCS), asiklovir berada di bawah ubat Kelas III, iaitu larut dengan kebolehtelapan usus yang rendah.[47] Asiklovir mempunyai kadar pengedaran yang tinggi; pengikatan protein dilaporkan berkisar antara 9 hingga 33%.[48] Separuh hayat penyingkiran (t1/2) asiklovir bergantung mengikut kumpulan umur; neonatus mempunyai t1/2 daripada 4 jam, kanak-kanak 1-12 tahun mempunyai t1/2 daripada 2-3 jam manakala orang dewasa mempunyai t1/2 daripada 3 jam.[2]
Kimia
[sunting | sunting sumber]Butiran sintesis asiklovir pertama kali diterbitkan oleh saintis dari Universiti Buffalo.[49]
Dalam langkah pertama yang ditunjukkan, 2,6-dikloropurina dialkilasi dengan 1-benzoiloksi-2-klorometoksietana. Kumpulan klorin pada kedudukan 6 gelang heterosiklik adalah lebih reaktif daripada klorin kedudukan 2, oleh itu ia boleh digantikan secara selektif oleh kumpulan amino, yang kemudiannya ditukar kepada amida menggunakan asid nitrus. Akhirnya, baki klorin digantikan oleh kumpulan amino asiklovir menggunakan ammonia dalam metanol.[50] Sintesis ini dan kaedah lain untuk menyediakan sebatian telah dikaji semula.[51]
Sejarah
[sunting | sunting sumber]Asiklovir dilihat sebagai permulaan era baru dalam terapi antivirus, kerana ia sangat selektif dan memiliki kadar sitotoksin rendah.[3] Sejak ia ditemui pada pertengahan 1970-an, ia telah digunakan sebagai ubat yang berkesan dalam rawatan jangkitan yang disebabkan oleh kebanyakan spesies keluarga herpesvirus yang diketahui, termasuk virus herpes simplex dan varicella zoster. Nukleosida yang diasingkan daripada span Caribbean, Cryptotethya crypta, menjadi asas untuk sintesis asiklovir.[52][53][54] Ia ditemui bersama oleh Howard Schaeffer berikutan kerjanya dengan Robert Vince, S. Bittner dan S. Gurwara mengenai asikloadenosina analog adenosina yang menunjukkan aktiviti antivirus yang berpotensi.[49] Kemudian, Schaeffer menyertai Burroughs Wellcome dan meneruskan pembangunan asiklovir dengan ahli farmakologi Gertrude B. Elion.[55] Paten AS mengenai asiklovir yang menyenaraikan Schaeffer sebagai pencipta telah dikeluarkan pada 1979.[56] Vince kemudiannya mencipta abakavir, ubat nRTI buat pesakit HIV.[57] Elion telah dianugerahkan Hadiah Nobel dalam Perubatan pada 1988, sebahagiannya untuk pembangunan asiklovir.
Bentuk prodrug yang berkaitan, valasiklovir mula digunakan dalam perubatan pada tahun 1995. Ia ditukar kepada asiklovir dalam badan selepas penyerapan.[58]
Pada tahun 2009, asiklovir dalam kombinasi dengan krim hidrokortison, dipasarkan sebagai Xerese, telah diluluskan di Amerika Syarikat bagi rawatan awal herpes labialis berulang (kudis selesem) untuk mengurangkan kemungkinan luka selesema berulser dan memendekkan masa penyembuhan lesi pada orang dewasa dan kanak-kanak (berumur enam tahun ke atas).[59][60]
Masyarakat dan budaya
[sunting | sunting sumber]Ia pada asalnya dipasarkan sebagai Zovirax; paten telah tamat tempoh pada tahun 1990-an dan sejak itu ia adalah generik dan dipasarkan di bawah banyak jenama di seluruh dunia.[1]
Nota
[sunting | sunting sumber]- ^ Diberi keadaan sama seperti sebelumnya.
Rujukan
[sunting | sunting sumber]- ^ a b c "Aciclovir". Drugs.com. Diarkibkan daripada yang asal pada 23 September 2015. Dicapai pada 6 September 2015.
- ^ a b c d "Zovirax (acyclovir) dosing, indications, interactions, adverse effects, and more". Medscape Reference. WebMD. Diarkibkan daripada yang asal pada 19 February 2014. Dicapai pada 5 February 2014.
- ^ a b "Antiviral prodrugs – the development of successful prodrug strategies for antiviral chemotherapy". British Journal of Pharmacology. 147 (1). Wiley-Blackwell (diterbitkan January 2006). 5 October 2005. m/s. 1–11. doi:10.1038/sj.bjp.0706446. PMC 1615839. PMID 16284630.
- ^ a b c d e f g h i j "Acyclovir". The American Society of Health-System Pharmacists. Diarkibkan daripada yang asal pada 2015-01-05. Dicapai pada Jan 1, 2015.
- ^ "Antiviral treatment for severe EBV infections in apparently immunocompetent patients". Journal of Clinical Virology. 49 (3): 151–157. November 2010. doi:10.1016/j.jcv.2010.07.008. PMID 20739216.
- ^ "Prescribing medicines in pregnancy database". Australian Government. 3 March 2014. Diarkibkan daripada yang asal pada 8 April 2014. Dicapai pada 22 April 2014.
- ^ Hamilton R (2015). Tarascon Pocket Pharmacopoeia 2015 Deluxe Lab-Coat Edition. Jones & Bartlett Learning. m/s. 59. ISBN 9781284057560.
- ^ "Acyclovir use while Breastfeeding". Mar 10, 2015. Diarkibkan daripada yang asal pada 5 March 2016. Dicapai pada 8 March 2016.
Even with the highest maternal dosages, the dosage of acyclovir in milk is only about 1% of a typical infant dosage and would not be expected to cause any adverse effects in breastfed infants
- ^ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery. John Wiley & Sons. m/s. 504. ISBN 9783527607495.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ World Health Organization (2021). World Health Organization model list of essential medicines: 22nd list (2021). Geneva: World Health Organization. hdl:10665/345533. WHO/MHP/HPS/EML/2021.02.
- ^ "The Top 300 of 2020". ClinCalc. Dicapai pada 7 October 2022.
- ^ "Acyclovir - Drug Usage Statistics". ClinCalc. Dicapai pada 7 October 2022.
- ^ a b c d Rossi, S, penyunting (2013). Australian Medicines Handbook (ed. 2013). Adelaide: The Australian Medicines Handbook Unit Trust. ISBN 978-0-9805790-9-3.
- ^ Joint Formulary Committee (2013). British National Formulary (BNF) (ed. 65). London: Pharmaceutical Press. ISBN 978-0-85711-084-8.
- ^ "A systematic review of viral infections associated with oral involvement in cancer patients: a spotlight on Herpesviridea". Supportive Care in Cancer. 18 (8): 993–1006. August 2010. doi:10.1007/s00520-010-0900-3. PMID 20544224. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Epstein-Barr virus infections: prospects for treatment". The Journal of Antimicrobial Chemotherapy. 56 (2): 277–281. August 2005. CiteSeerX 10.1.1.320.6721. doi:10.1093/jac/dki240. PMID 16006448.
- ^ "Antiviral agents for infectious mononucleosis (glandular fever)". The Cochrane Database of Systematic Reviews. 2016 (12): CD011487. December 2016. doi:10.1002/14651858.CD011487.pub2. PMC 6463965. PMID 27933614.
- ^ "Antiviral treatment for preventing postherpetic neuralgia". The Cochrane Database of Systematic Reviews. 2014 (2): CD006866. February 2014. doi:10.1002/14651858.CD006866.pub3. PMC 10583132 Check
|pmc=value (bantuan). PMID 24500927. - ^ a b "Antiviral treatment and other therapeutic interventions for herpes simplex virus epithelial keratitis". The Cochrane Database of Systematic Reviews. 1 (1): CD002898. January 2015. doi:10.1002/14651858.CD002898.pub5. PMC 4443501. PMID 25879115.
- ^ "Acyclovir in recurrent herpes labialis". BMJ. 312 (7022): 6. January 1996. doi:10.1136/bmj.312.7022.6. PMC 2349724. PMID 8555890. Diarkibkan daripada yang asal pada 2007-05-15. – Editorial
- ^ "Acyclovir cream for treatment of herpes simplex labialis: results of two randomized, double-blind, vehicle-controlled, multicenter clinical trials". Antimicrobial Agents and Chemotherapy. 46 (7): 2238–2243. July 2002. doi:10.1128/aac.46.7.2238-2243.2002. PMC 127288. PMID 12069980.
- ^ "5th International AIDS Society Conference on HIV Pathogenesis, Treatment and Prevention: summary of key research and implications for policy and practice - biomedical prevention". Journal of the International AIDS Society. 13 (Suppl 1): S4. June 2010. doi:10.1186/1758-2652-13-S1-S4. PMC 2880255. PMID 20519025.
- ^ a b c "Acyclovir label" (PDF). GSK. FDA. 2005. Diarkibkan daripada yang asal (PDF) pada 2017-09-08.
- ^ "Drugs for non-HIV viral infections". Treatment Guidelines from the Medical Letter. 3 (32): 23–32. April 2005. PMID 15767977.
- ^ "Guidelines for prevention and treatment of opportunistic infections in HIV-infected adults and adolescents: recommendations from CDC, the National Institutes of Health, and the HIV Medicine Association of the Infectious Diseases Society of America". MMWR. Recommendations and Reports. 58 (RR-4): 1–207, quiz CE1–4. April 2009. PMID 19357635.
- ^ a b c d "PRODUCT INFORMATION NAME OF THE DRUG OZVIR TABLETS" (PDF). TGA eBusiness Services. Ranbaxy Australia Pty Ltd. 26 August 2011. Diarkibkan daripada yang asal pada 20 August 2016. Dicapai pada 6 February 2014.
- ^ Centers for Disease Control and Prevention. (January 2006). Epidemiology and prevention of vaccine-preventable diseases (ed. 9th). Public Health Foundation. m/s. 171–192.
- ^ "Breastfeeding and the use of human milk". Pediatrics. 115 (2): 496–506. February 2005. doi:10.1542/peds.2004-2491. PMID 15687461.
- ^ "Antiviral drugs for viruses other than human immunodeficiency virus". Mayo Clinic Proceedings. 86 (10): 1009–1026. October 2011. doi:10.4065/mcp.2011.0309. PMC 3184032. PMID 21964179.
- ^ "Renal function after acyclovir intravenous injection". The American Journal of Medicine. 73 (1A): 182–185. July 1982. doi:10.1016/0002-9343(82)90087-0. PMID 6285711.
- ^ "Acyclovir-induced renal failure. Clinical course and histology". The American Journal of Medicine. 84 (6): 1067–1071. June 1988. doi:10.1016/0002-9343(88)90313-0. PMID 3376977.
- ^ "High serum concentrations of the acyclovir main metabolite 9-carboxymethoxymethylguanine in renal failure patients with acyclovir-related neuropsychiatric side effects: an observational study". Nephrology, Dialysis, Transplantation. 18 (6): 1135–1141. June 2003. doi:10.1093/ndt/gfg119. PMID 12748346. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Aciclovir-induced neurotoxicity: Utility of CSF and serum CMMG levels in diagnosis". Journal of Clinical Virology. 61 (4): 608–610. December 2014. doi:10.1016/j.jcv.2014.09.001. PMID 25440915.
- ^ "Acyclovir-Induced Neurotoxicity: A Case Report and Review of Literature". American Journal of Therapeutics. 23 (3): e941–e943. 2016. doi:10.1097/MJT.0000000000000093. PMID 24942005.
- ^ "In vitro activity of ketoconazole against herpes simplex virus". Antimicrobial Agents and Chemotherapy. 30 (2): 215–219. August 1986. doi:10.1128/aac.30.2.215. PMC 180521. PMID 3021048.
- ^ GlaxoSmithKline. Zovirax® (acyclovir sodium) for injection prescribing information. Research Triangle Park, NC; 2003 Nov
- ^ "Possible drug interaction during therapy with azidothymidine and acyclovir for AIDS". The New England Journal of Medicine. 316 (9): 547. February 1987. doi:10.1056/NEJM198702263160912. PMID 3468354.
- ^ Baselt RC (2008). Disposition of toxic drugs and chemicals in man (ed. 8th). Foster City, CA: Biomedical Publications. m/s. 29–31. ISBN 9780962652370.
- ^ "VALTREX (valacyclovir hydrochloride) Caplets -GSKSource". gsksource.com. Dicapai pada 2019-08-02.
- ^ "Acyclovir (acyclovir) Capsule Acyclovir (acyclovir) Tablet [Genpharm Inc.]". DailyMed. Genpharm Inc. November 2006. Diarkibkan daripada yang asal pada 21 February 2014. Dicapai pada 5 February 2014.
- ^ "Aciclovir Tablets BP 400mg - Summary of Product Characteristics (SPC)". electronic Medicines Compendium. Actavis UK Ltd. 20 August 2012. Diarkibkan daripada yang asal pada 22 February 2014. Dicapai pada 5 February 2014.
- ^ Sweetman, S, penyunting (7 August 2013). "Aciclovir". Martindale: The Complete Drug Reference. London, UK: Pharmaceutical Press. Dicapai pada 6 February 2014.
- ^ "Resistance of herpes simplex viruses to nucleoside analogues: mechanisms, prevalence, and management". Antimicrobial Agents and Chemotherapy. 55 (2): 459–472. February 2011. doi:10.1128/AAC.00615-10. PMC 3028810. PMID 21078929.
- ^ "Acyclovir. An updated review of its antiviral activity, pharmacokinetic properties and therapeutic efficacy". Drugs. 37 (3): 233–309. March 1989. doi:10.2165/00003495-198937030-00002. PMID 2653790.
- ^ "Aciclovir. A reappraisal of its antiviral activity, pharmacokinetic properties and therapeutic efficacy". Drugs. 47 (1): 153–205. January 1994. doi:10.2165/00003495-199447010-00009. PMID 7510619.
- ^ "Development and Optimization of Acyclovir Loaded Mucoadhesive Microspheres by Box -Behnken Design". Dhaka University Journal of Pharmaceutical Sciences. 18 (1): 1–12. 2019. doi:10.3329/dujps.v18i1.41421.
- ^ "Aciclovir Tablets BP 400mg - Summary of Product Characteristics (SmPC) - (emc)". www.medicines.org.uk.
- ^ a b "Novel substrate of adenosine deaminase". Journal of Medicinal Chemistry. 14 (4): 367–369. April 1971. doi:10.1021/jm00286a024. PMID 5553754.
- ^ US, "Methods and compositions for treating viral infections and guanine acyclic nucleosides"
- ^ Vardanyan R, Hruby V (2016). "34: Antiviral Drugs". Synthesis of Best-Seller Drugs. Academic Press. m/s. 706–708. doi:10.1016/B978-0-12-411492-0.00034-1. ISBN 9780124114920.
- ^ Garrison T (1999). Oceanography: An Invitation to Marine Science, 3rd ed. Belmont, CA: Wadsworth Publishing Company. m/s. 471.
- ^ "Bioactive Alkylpyridinium Compounds from Marine Sponges". Toxin Reviews. 19 (2): 139–160. 2000. doi:10.1081/TXR-100100318.
- ^ "Marine sponges: potential sources of new antimicrobial drugs". Current Pharmaceutical Biotechnology. 10 (1): 86–105. January 2009. doi:10.2174/138920109787048625. PMID 19149592.
- ^ "Selectivity of action of an antiherpetic agent, 9-(2-hydroxyethoxymethyl) guanine". Proceedings of the National Academy of Sciences of the United States of America. 74 (12): 5716–5720. December 1977. Bibcode:1977PNAS...74.5716E. doi:10.1073/pnas.74.12.5716. PMC 431864. PMID 202961.
- ^ US
- ^ "A brief history of the development of Ziagen". Chemtracts. 21: 127–134. 2008.
- ^ "Valacyclovir Hydrochloride Monograph for Professionals". Drugs.com. American Society of Health-System Pharmacists. Dicapai pada 17 March 2019.
- ^ "Drug Approval Package: Acyclovir and Hydrocortisone NDA #022436". U.S. Food and Drug Administration (FDA). 13 December 2019. Diarkibkan daripada yang asal pada 13 December 2019. Dicapai pada 13 December 2019.
 Rencana ini mengandungi teks dari suatu penerbitan yang kini berada dalam domain awam:
Rencana ini mengandungi teks dari suatu penerbitan yang kini berada dalam domain awam:
- ^ "Xerese- acyclovir and hydrocortisone cream". DailyMed. 12 December 2019. Diarkibkan daripada yang asal pada 13 December 2019. Dicapai pada 12 December 2019.
- CS1 errors: PMC
- Source attribution
- Infobox drug with local INN variant
- Template:drugs.com link with non-standard subpage
- Semua rencana dengan kenyataan tidak bersumber dari May 2022
- Rencana dengan pengecam KEGG berubah
- ECHA InfoCard ID from Wikidata
- Pelbagai bahan kimia dalam infobox dadah
- Multiple chemicals in an infobox that need indexing
- Drugboxes which contain changes to watched fields
- Ubat penting Pertubuhan Kesihatan Sedunia
- Purina
- Nefrotoksin
- Perencat CYP1A2
- Ubat antivirus herpes

