Badan keton
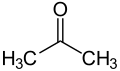
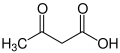
Badan keton ialah molekul atau sebatian larut air yang mengandungi kumpulan keton yang dihasilkan daripada asid lemak oleh hati (ketogenesis).[1][2] Badan keton mudah diangkut ke dalam tisu di luar hati, di mana ia ditukar kepada asetil-KoA (acetyl-Koenzim A)—yang kemudiannya memasuki kitaran asid sitrik (kitaran Krebs) dan dioksidakan menjadi tenaga.[3][4] Kumpulan keton yang berasal dari hati ini termasuk asid asetoasetik (asetoasetat), beta-hidroksibutirat, dan aseton, produk pecahan spontan asetoasetat (lihat grafik).
Badan keton dihasilkan oleh hati semasa tempoh sekatan kalori dalam pelbagai senario: pengambilan makanan yang rendah (berpuasa), diet rendah karbohidrat, kelaparan, senaman sengit yang berpanjangan,[5] ketagihan alkohol, atau semasa diabetes melitus jenis 1 yang tidak dirawat (atau tidak dirawat secukupnya). Badan keton dihasilkan dalam sel hati melalui pemecahan asid lemak.[6] Mereka dilepaskan ke dalam darah selepas simpanan glikogen dalam hati telah habis. (Simpanan glikogen biasanya akan habis dalam tempoh 24 jam pertama berpuasa.)[2]
Badan keton juga dihasilkan dalam sel glia di bawah tempoh sekatan makanan untuk mengekalkan pembentukan ingatan.[7]
Apabila dua molekul asetil-KoA kehilangan KoA-nya (atau kumpulan koenzim A), ia boleh membentuk dimer (kovalen) yang dipanggil asetoasetat. β-hidroksibutirat ialah bentuk asetoasetat diturunkan, di mana kumpulan keton ditukarkan kepada kumpulan alkohol (atau hidroksil) (lihat ilustrasi di sebelah kanan). Kedua-duanya ialah molekul 4 karbon yang mudah ditukar kembali kepada asetil-KoA oleh kebanyakan tisu badan kecuali hati. Aseton ialah bentuk asetoasetat dinyahkarboksil yang tidak boleh ditukar kembali kepada asetil-KoA kecuali melalui detoksifikasi dalam hati, di mana ia ditukar kepada asid laktik, yang boleh, seterusnya, dioksidakan kepada asid piruvik, dan hanya kemudian menjadi asetil-KoA.
Badan keton mempunyai bau yang khas yang boleh dikesan dengan mudah dalam nafas orang yang mengalami ketosis dan ketoasidosis. Ia sering digambarkan sebagai berbau buah atau seperti pengilat kuku (yang biasanya mengandungi aseton atau etil asetat).
Selain daripada tiga jasad keton endogen, jasad keton lain seperti β-ketopentanoat dan β-hidroksipentanoat mungkin terhasil hasil daripada metabolisme trigliserida sintetik seperti triheptanoin.
Pengeluaran[sunting | sunting sumber]

Lemak yang disimpan dalam tisu adipos dilepaskan daripada sel lemak ke dalam darah sebagai asid lemak bebas dan gliserol apabila tahap insulin rendah dan tahap glukagon dan epinefrina dalam darah adalah tinggi. Ini berlaku antara waktu makan, semasa berpuasa, kelaparan dan senaman berat, apabila paras glukosa darah berkemungkinan menurun. Asid lemak ialah bahan api tenaga yang sangat tinggi dan diambil oleh semua sel metabolisme yang mempunyai mitokondria. Ini kerana asid lemak hanya boleh dimetabolismekan dalam mitokondria.[2][8] Sel darah merah tidak mengandungi mitokondria, dan oleh itu, bergantung sepenuhnya kepada glikolisis anaerob demi keperluan tenaga mereka. Dalam semua tisu lain, asid lemak yang memasuki sel metabolisme digabungkan dengan koenzim A untuk membentuk rantai asil-KoA . Ini dipindahkan ke dalam mitokondria sel, di mana ia dipecahkan kepada unit asetil-KoA melalui urutan tindak balas yang dikenali sebagai β-pengoksidaan.[2][8]
Asetil-KoA yang dihasilkan oleh β-pengoksidaan memasuki kitaran asid sitrik dalam mitokondria dengan bergabung dengan oksaloasetat untuk membentuk sitrat. Ini menghasilkan pembakaran lengkap kumpulan asetil bagi asetil-KoA (lihat rajah di atas, di sebelah kanan) kepada CO2 dan air. Tenaga yang dibebaskan dalam proses ini ditangkap dalam bentuk 1 GTP dan 9 molekul ATP setiap kumpulan asetil (atau molekul asid asetik) teroksida.[2][8] Ini ialah nasib asetil-KoA ketika β-pengoksidaan asid lemak berlaku, kecuali dalam keadaan tertentu dalam hati. Dalam hati, oksaloasetat sepenuhnya atau sebahagiannya dialihkan ke dalam laluan glukoneogenesis semasa berpuasa, kelaparan, diet rendah karbohidrat, senaman berat yang berpanjangan, dan dalam diabetes melitus jenis 1 yang tidak terkawal. Di bawah keadaan ini, oksaloasetat dihidrogenkan kepada malat yang kemudiannya dikeluarkan daripada mitokondria untuk ditukar kepada glukosa dalam sitoplasma sel hati, dari mana glukosa dilepaskan ke dalam darah.[2] Di dalam hati, oleh itu, oksaloasetat tidak tersedia bagi pemeluwapan dengan asetil-KoA apabila glukoneogenesis yang ketara telah dirangsang oleh insulin yang rendah (atau ketiadaannya) dan kepekatan glukagon yang tinggi dalam darah. Di bawah keadaan ini, asetil-KoA dialihkan kepada pembentukan asetoasetat dan beta-hidroksibutirat.[2] Asetoasetat, beta-hidroksibutirat, dan produk pecahan spontannya, aseton,[9] dikenali sebagai badan keton. Badan keton dilepaskan oleh hati ke dalam darah. Semua sel dengan mitokondria boleh mengambil badan keton daripada darah dan menukarkannya semula kepada asetil-KoA yang kemudiannya boleh digunakan sebagai bahan api dalam kitaran asid sitrik mereka kerana tiada tisu lain boleh mengalihkan oksaloasetatnya ke dalam laluan glukoneogenik dengan cara yang hati melakukan ini. Tidak seperti asid lemak bebas, badan keton boleh melintasi penghalang darah-otak, dan oleh itu, boleh didapati sebagai bahan api untuk sel-sel sistem saraf pusat, bertindak sebagai pengganti glukosa, di mana sel-sel ini biasanya bertahan.[2] Kejadian badan keton yang tinggi dalam darah semasa kelaparan, diet rendah karbohidrat dan senaman berat yang berpanjangan boleh menyebabkan ketosis, dan dalam bentuk yang melampau dalam diabetes melitus jenis 1 di luar kawalan, sebagai ketoasidosis.
Asetoasetat mempunyai bau yang sangat khas, untuk orang yang dapat mengesan bau ini, yang berlaku dalam nafas dan air kencing semasa ketosis. Sebaliknya, kebanyakan orang boleh menghidu aseton, di mana bau "manis & berbuah" seseorang juga dapat mencirikan nafas orang yang mengalami ketosis atau ketoasidosis secara utamanya.[10]
Penggunaan bahan api dalam organ berbeza[sunting | sunting sumber]
Badan keton boleh digunakan sebagai bahan api dalam jantung, otak dan otot, tetapi bukan hati. Ia menjana 2 guanosina trifosfat (GTP) dan 22 adenosina trifosfat (ATP) molekul setiap molekul asetoasetat apabila teroksida dalam mitokondria. Badan keton diangkut dari hati ke tisu lain, di mana asetoasetat dan β-hidroksibutirat boleh ditukar semula kepada asetil-KoA untuk menghasilkan molekul setara penurunan (NADH dan FADH2), melalui kitaran asid sitrik. Walaupun ia merupakan sumber badan keton, hati tidak boleh menggunakannya buat menjana tenaga kerana ia tidak mempunyai enzim tioforase (β-ketoasil-KoA transferase). Aseton diambil oleh hati dalam kepekatan rendah, dan menjalani detoksifikasi melalui laluan metilglioksal yang berakhir dengan laktat. Aseton dalam kepekatan tinggi, seperti ketika puasa berpanjangan atau diet ketogenik, diserap oleh sel di luar hati dan dimetabolismekan melalui laluan berbeza melalui propilena glikol. Walaupun laluan itu mengikut siri langkah yang berbeza yang memerlukan ATP, propilena glikol akhirnya boleh bertukar menjadi piruvat.[11]
Jantung[sunting | sunting sumber]
Jantung lebih suka menggunakan asid lemak sebagai bahan api dalam keadaan fisiologi normal. Walau bagaimanapun, dalam keadaan ketosis, jantung boleh menggunakan badan keton dengan berkesan untuk tujuan ini.[12]
Otak[sunting | sunting sumber]
Selama beberapa dekad, hati telah dianggap sebagai pembekal utama badan keton untuk menjana metabolisme tenaga otak. Walau bagaimanapun, bukti terkini telah menunjukkan bahawa sel glia boleh memacu neuron dengan badan keton yang disintesis secara tempatan untuk mengekalkan pembentukan ingatan ketika sekatan makanan.[3]
Otak mendapat sebahagian daripada keperluan bahan apinya daripada badan keton apabila glukosa kurang tersedia daripada biasa. Sekiranya kepekatan glukosa rendah dalam darah, kebanyakan tisu lain mempunyai sumber bahan api alternatif selain badan keton dan glukosa (seperti asid lemak), tetapi kajian telah menunjukkan bahawa otak mempunyai keperluan wajib untuk beberapa glukosa.[13] Selepas berpuasa selama 3 hari, otak mendapat 25% tenaga daripada badan keton.[14] Selepas kira-kira 24 hari, badan keton menjadi bahan api utama otak, yakni dua pertiga daripada penggunaan bahan api otak.[15] Banyak kajian mencadangkan bahawa sel otak manusia boleh bertahan dengan sedikit atau tanpa glukosa, tetapi cubaan pembuktian boleh dipersoalkan secara etika.[15] Semasa peringkat awal ketosis, otak tidak membakar keton kerana ia merupakan substrat penting bagi sintesis lipid dalam otak. Tambahan pula, keton yang dihasilkan daripada asid lemak omega-3 boleh mengurangkan kemerosotan kognitif pada usia tua .[16]
Ketogenesis membantu memacu pembesaran otak manusia semasa evolusinya. Sebelum ini, ada cadangan bahawa ketogenesis ialah kunci kepada evolusi dan daya maju otak yang lebih besar secara umum. Walau bagaimanapun, kehilangan HMGCS2 (dan seterusnya keupayaan ini) dalam tiga keturunan mamalia berotak besar (setasea, gajah–mastodon, kelawar buah Dunia Lama) menunjukkan sebaliknya. Daripada tiga keturunan, hanya kelawar buah yang mempunyai sensitiviti yang dijangkakan terhadap kelaparan; dua yang lain telah menemui cara alternatif untuk menjana tenaga badan semasa kelaparan.[17]
Ketosis dan ketoasidosis[sunting | sunting sumber]
Dalam individu normal, terdapat pengeluaran badan keton yang berterusan oleh hati dan penggunaannya oleh tisu ekstrahepatik. Kepekatan badan keton dalam darah dikekalkan sekitar 1 mg/dL. Perkumuhan mereka dalam air kencing adalah sangat rendah, dan tidak dapat dikesan oleh ujian air kencing rutin (ujian Rothera).[18]
Apabila kadar sintesis badan keton melebihi kadar penggunaan, kepekatannya dalam darah meningkat; ini dikenali sebagai ketonemia. Ini diikuti oleh ketonuria - perkumuhan badan keton dalam air kencing. Gambaran keseluruhan ketonemia dan ketonuria biasanya dirujuk sebagai ketosis. Bau asetoasetat dan/atau aseton dalam nafas ialah ciri biasa dalam ketosis.
Apabila pesakit diabetes jenis 1 mengalami tekanan biologi akut (jangkitan, serangan jantung atau trauma fizikal) atau gagal mendapat insulin yang mencukupi, mereka mungkin memasuki keadaan patologi ketoasidosis diabetes. Di bawah keadaan ini, kekurangan atau ketiadaan insulin dalam darah, digabungkan dengan kepekatan glukagon tinggi yang tidak sesuai,[19] mendorong hati untuk menghasilkan glukosa pada kadar meningkat yang tidak sesuai, menyebabkan asetil-KoA yang terhasil daripada pengoksidaan beta asid lemak bertukar menjadi badan keton. Paras badan keton yang sangat tinggi yang terhasil merendahkan pH plasma darah, yang secara refleks mencetuskan buah pinggang untuk mengeluarkan air kencing dengan paras asid yang sangat tinggi. Paras glukosa dan keton yang tinggi dalam darah juga melimpah secara pasif ke dalam air kencing (disebabkan oleh ketidakupayaan tubul renal untuk menyerap semula glukosa dan keton daripada cecair tiub oleh kerana ditimpa oleh jumlah tinggi bahan-bahan ini yang ditapis ke dalam cecair tiub). Diuresis osmosis glukosa yang terhasil menyebabkan penyingkiran air dan elektrolit daripada darah, dan dapat mengakibatkan dehidrasi yang boleh membawa maut.
Proses ketosis kini sedang disiasat untuk keberkesanan dalam memulihkan gejala penyakit Alzheimer[20] dan sindrom Angelman.[21]
Lihat juga[sunting | sunting sumber]
Rujukan[sunting | sunting sumber]
- ^ Cahill, George F.; Veech, Richard L. (2003). "Ketoacids? Good medicine?". Transactions of the American Clinical and Climatological Association. 114: 149–161, discussion 162–163. ISSN 0065-7778. PMC 2194504. PMID 12813917.
- ^ a b c d e f g h Stryer, Lubert (1995). Biochemistry (ed. Fourth). New York: W.H. Freeman and Company. m/s. 510–515, 581–613, 775–778. ISBN 0-7167-2009-4.
- ^ a b Silva, B., Mantha, O. L., Schor, J., Pascual, A., Plaçais, P. Y., Pavlowsky, A., & Preat, T. (2022). Glia fuel neurons with locally synthesized ketone bodies to sustain memory under starvation. Nature Metabolism, 4(2), 213–224. https://doi.org/10.1038/s42255-022-00528-6 Diarkibkan 2024-03-06 di Wayback Machine
- ^ Mary K. Campbell; Shawn O. Farrell (2006). Biochemistry (ed. 5th). Cengage Learning. m/s. 579. ISBN 0-534-40521-5.
- ^ Koeslag, J.H.; Noakes, T.D.; Sloan, A.W. (1980). "Post-exercise ketosis". Journal of Physiology. 301: 79–90. doi:10.1113/jphysiol.1980.sp013190. PMC 1279383. PMID 6997456.
- ^ Berg, Jeremy (2019). Biochemistry (ed. 9). MacMillan. m/s. 724. ISBN 9781319402853.
- ^ Silva, Bryon; Mantha, Olivier L.; Schor, Johann; Pascual, Alberto; Plaçais, Pierre-Yves; Pavlowsky, Alice; Preat, Thomas (17 February 2022). "Glia fuel neurons with locally synthesized ketone bodies to sustain memory under starvation". Nature Metabolism. 4 (2): 213–224. doi:10.1038/s42255-022-00528-6. PMC 8885408 Check
|pmc=value (bantuan). PMID 35177854 Check|pmid=value (bantuan). - ^ a b c "Oxidation of fatty acids". Diarkibkan daripada yang asal pada 2018-01-08. Dicapai pada 2015-12-17.
- ^ Ketone body metabolism Diarkibkan 2016-09-22 di Wayback Machine, University of Waterloo
- ^ "American Diabetes Association-Ketoacidosis". Diarkibkan daripada yang asal pada 2010-04-29. Dicapai pada 2010-03-02.
- ^ "Archived copy" (PDF). Diarkibkan daripada yang asal (PDF) pada 2015-09-24. Dicapai pada 2013-09-18.CS1 maint: archived copy as title (link)
- ^ "Metabolic and genetic regulation of cardiac energy substrate preference". Comp. Biochem. Physiol. A. 146 (1): 26–39. January 2007. doi:10.1016/j.cbpa.2006.09.014. PMID 17081788.
- ^ Clarke, DD; Sokoloff, L (1999). "Substrates of Cerebral Metabolism". Dalam Siegel, GJ; Agranoff, BW; Albers, RW (penyunting). Basic Neurochemistry: Molecular, Cellular and Medical Aspects (ed. 6th). Philadelphia: Lippincott-Raven. Diarkibkan daripada yang asal pada 2019-03-23. Dicapai pada 2017-09-02.
- ^ Hasselbalch, SG; Knudsen, GM; Jakobsen, J; Hageman, LP; Holm, S; Paulson, OB (1994). "Brain metabolism during short-term starvation in humans". Journal of Cerebral Blood Flow and Metabolism. 14 (1): 125–31. doi:10.1038/jcbfm.1994.17. PMID 8263048.
- ^ a b Cahill GF. Fuel metabolism in starvation. Annu Rev Nutr 2006;26:1–22
- ^ Freemantle, E.; Vandal, M. N.; Tremblay-Mercier, J.; Tremblay, S. B.; Blachère, J. C.; Bégin, M. E.; Thomas Brenna, J.; Windust, A.; Cunnane, S. C. (2006). "Omega-3 fatty acids, energy substrates, and brain function during aging". Prostaglandins, Leukotrienes and Essential Fatty Acids. 75 (3): 213–20. doi:10.1016/j.plefa.2006.05.011. PMID 16829066.
- ^ Jebb, David; Hiller, Michael (16 October 2018). "Recurrent loss of HMGCS2 shows that ketogenesis is not essential for the evolution of large mammalian brains". eLife. 7: e38906. doi:10.7554/eLife.38906. PMC 6191284. PMID 30322448.
- ^ Comstock, John P.; Garber, Alan J. (1990). Walker, H. Kenneth; Hall, W. Dallas; Hurst, J. Willis (penyunting). Clinical Methods: The History, Physical, and Laboratory Examinations (ed. 3rd). Boston: Butterworths. ISBN 040990077X. PMID 21250091. Diarkibkan daripada yang asal pada 2017-09-10. Dicapai pada 2017-12-19.
- ^ Koeslag, J.H.; Saunders, P.T.; Terblanche, E. (2003). "Topical Review: A reappraisal of blood glucose homeostat which comprehensively explains the type 2 diabetes mellitus/syndrome X complex". Journal of Physiology. 549 (Pt 2): 333–346. doi:10.1113/jphysiol.2002.037895. PMC 2342944. PMID 12717005.
- ^ Henderson, Samuel T. (2008-07-01). "Ketone bodies as a therapeutic for Alzheimer's disease". Neurotherapeutics. 5 (3): 470–480. doi:10.1016/j.nurt.2008.05.004. ISSN 1933-7213. PMC 5084248. PMID 18625458.
- ^ "Evaluation of the Safety and Tolerability of a Nutritional Formulation in Angelman Syndrome". 18 August 2020. Diarkibkan daripada yang asal pada 9 February 2022. Dicapai pada 9 February 2022.