Triiodotironina
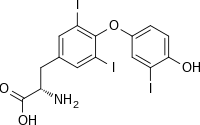 Formula rangka
| |
 Model bola dan batang
| |
 Model isian ruang
| |
| Nama | |
|---|---|
| Nama IUPAC
Asid (2S)-2-amino-3-[4-(4-hidroksi-3-iodofeniksi)-3,5-diiodofenil]propanoik
| |
| Nama lain
triiodotironina
T3 3,3′,5-triiodo-L-tironina | |
| Pengecam | |
Imej model 3D Jmol
|
|
| 2710227 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.027.272 |
| Nombor EC |
|
| KEGG | |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C15H12I3NO4 | |
| Jisim molar | 650.98 g·mol−1 |
| Bahaya | |
| Piktogram GHS | 
|
| Perkataan isyarat GHS | Warning |
| H315, H319, H335 | |
| P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405, P501 | |
| NFPA 704 (berlian api) | |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| | |
| Rujukan kotak info | |
Triiodotironina, juga dikenali sebagai T3, ialah sejenis hormon tiroid. Ia mempengaruhi hampir setiap proses fisiologi dalam badan, termasuk pertumbuhan dan perkembangan, metabolisme, suhu badan, dan kadar denyutan jantung.[1]
Pengeluaran T 3 dan prohormon tiroksina (T4) diaktifkan oleh hormon perangsang tiroid (TSH), yang dikeluarkan daripada kelenjar pituitari anterior. Laluan ini adalah sebahagian daripada proses maklum balas kitaran tertutup: Peningkatan kepekatan T3 dan T4 dalam plasma darah menghalang pengeluaran TSH dalam kelenjar pituitari anterior. Apabila kepekatan hormon ini berkurangan, kelenjar pituitari anterior meningkatkan pengeluaran TSH, dan melalui proses ini, sistem kawalan maklum balas menstabilkan tahap hormon tiroid dalam aliran darah.
T3 ialah hormon sebenar. Kesannya pada tisu sasaran adalah kira-kira empat kali lebih kuat daripada T4.[2] Daripada hormon tiroid yang dihasilkan, hanya kira-kira 20% adalah T3, manakala 80% dihasilkan sebagai T4. Kira-kira 85% daripada T3 yang beredar kemudiannya terbentuk dalam hati dan pituitari anterior dengan penyingkiran atom iodin daripada atom karbon nombor lima gelang luar T4. Walau apa pun, kepekatan T3 dalam plasma darah manusia adalah kira-kira satu per 40 daripada T4. Separuh hayat T3 adalah kira-kira 2.5 hari.[3] Separuh hayat T4 adalah kira-kira 6.5 hari.[4]
Pengeluaran[sunting | sunting sumber]
Sintesis daripada T 4[sunting | sunting sumber]

T3 ialah hormon yang lebih aktif metabolik terbitan T4. T4 dideiodinasikan oleh tiga enzim deiodinase untuk menghasilkan triiodotironina yang lebih aktif:
- Jenis I hadir dalam hati, buah pinggang, tiroid, dan (sebahagian kecilnya) pituitari; ia menyumbang 80% daripada penyahiodinan T4.
- Jenis II terdapat dalam sistem saraf pusat, pituitari, tisu adipos perang dan saluran jantung, kebanyakannya intrasel. Dalam pituitari, ia mengantara maklum balas negatif pada hormon perangsang tiroid.
- Jenis III terdapat dalam plasenta, sistem saraf pusat, dan hemangioma. Deiodinase ini menukarkan T4 kepada T3 terbalik, yang tidak aktif, tidak seperti T3.
T4 disintesis dalam sel folikel tiroid seperti berikut.
- Simporter natrium-iodida mengangkut dua ion natrium merentasi membran bawah tanah sel folikel bersama-sama dengan ion iodin. Ini ialah pengangkut aktif sekunder yang menggunakan kecerunan kepekatan Na+ untuk menggerakkan I− melawan kecerunan kepekatannya.
- I− digerakkan merentasi membran apikal ke dalam koloid folikel.
- Tiroperoksidase mengoksidakan I− untuk membentuk radikal I.
- Tiroperoksidase memberi iodin terhadap sisa tirosil tiroglobulin dalam koloid. Tiroglobulin disintesis dalam retikulum endoplasma sel folikel dan dirembeskan ke dalam koloid.
- Hormon perangsang tiroid (TSH) yang dikeluarkan daripada kelenjar pituitari anterior mengikat reseptor TSH (reseptor berganding protein Gs) pada membran basolateral sel dan merangsang endositosis koloid.
- Vesikel endositos bergabung dengan lisosom sel folikel. Enzim lisosom membelah T4 daripada tiroglobulin beryodium.
- Vesikel ini kemudiannya dieksositosis, melepaskan hormon tiroid.

Sintesis langsung[sunting | sunting sumber]
Kelenjar tiroid juga menghasilkan sejumlah kecil T3 secara langsung. Dalam lumen folikel, sisa tirosina menjadi teriodin. Tindak balas ini memerlukan hidrogen peroksida. Iodin mengikat karbon 3 atau karbon 5 sisa tirosin tiroglobulin dalam proses yang dipanggil "pengorganikian" iodin. Iodinasi tirosina tertentu menghasilkan monoiodotirosina (MIT) dan diiodotirosina (DIT). Satu MIT dan satu DIT digandingkan secara enzimatik untuk membentuk T3 . Enzimnya ialah tiroid peroksidase.
Jumlah kecil T3 mungkin penting kerana tisu yang berbeza mempunyai sensitiviti yang berbeza terhadap T4 disebabkan oleh perbezaan dalam pengubikuitinan deiodinase dalam tisu yang berbeza.[6] Ini sekali lagi menimbulkan persoalan jika T3 perlu dimasukkan dalam terapi penggantian hormon tiroid (THRT).
Mekanisme tindakan[sunting | sunting sumber]
T3 dan T4 mengikat kepada reseptor nukleus (reseptor hormon tiroid). [7] T3 dan T4, walaupun bersifat lipofilik, tidak dapat meresap secara pasif melalui dwilapisan fosfolipid sel sasaran,[8] sebaliknya bergantung pada pengangkut iodotironin transmembran. Lipofilisiti T3 dan T4 memerlukan pengikatannya kepada pembawa protein protein pengikat tiroid (TBG) (globulin pengikat tiroksina, praalbumin pengikat tiroksina dan albumin) bagi pengangkutan dalam darah. Reseptor tiroid mengikat unsur tindak balas dalam promoter gen, dengan itu membolehkan mereka mengaktifkan atau menghalang transkripsi. Kepekaan tisu kepada T3 dimodulasi melalui reseptor tiroid.
Pengangkutan[sunting | sunting sumber]

T3 dan T4 dibawa dalam darah sambil terikat kepada protein plasma. Ini mempunyai kesan meningkatkan separuh hayat hormon dan mengurangkan kadar di mana ia diambil oleh tisu periferi. Terdapat tiga protein utama yang terikat kepada kedua-dua hormon. Globulin pengikat tiroksina (TBG) ialah glikoprotein yang mempunyai afiniti yang lebih tinggi terhadap T4 berbanding T3. Transtiretin juga merupakan glikoprotein, tetapi hanya membawa T4, dengan hampir tidak ada pertalian sama sekali untuk T3. Akhirnya, kedua-dua hormon mengikat dengan pertalian rendah kepada albumin serum, tetapi, disebabkan ketersediaan albumin yang besar, ia mempunyai kapasiti yang tinggi.
Ketepuan tapak pengikat pada globulin pengikat tironina (TBG) oleh T3 endogen boleh dianggarkan dengan ujian pengambilan resin triiodotironina. Ujian dilakukan dengan mengambil sampel darah, di mana lebihan T3 eksogen radioaktif ditambah, diikuti dengan resin yang juga mengikat T3 . Sebilangan kecil T3 radioaktif mengikat tapak TBG yang belum diduduki hormon tiroid endogen, dan selebihnya mengikat resin. Jumlah hormon berlabel yang terikat pada resin kemudiannya ditolak daripada jumlah yang ditambahkan, dengan bakinya adalah jumlah yang terikat pada tapak pengikat yang tidak dihuni pada TBG.[10]
Kesan[sunting | sunting sumber]
T 3 meningkatkan kadar metabolisme basal, dan dengan itu, meningkatkan penggunaan oksigen dan tenaga badan. Kadar metabolisme basal ialah keperluan kalori minimum yang diperlukan untuk mengekalkan kehidupan dalam individu yang berehat. T3 bertindak pada kebanyakan tisu dalam badan, dengan beberapa pengecualian termasuk limpa. Ia meningkatkan sintesis dan aktiviti Na+/K+-ATPase (yang biasanya membentuk sebahagian besar daripada jumlah perbelanjaan ATP selul) tanpa mengganggu keseimbangan ion transmembran.[11] Secara umum, ia meningkatkan perolehan makromolekul endogen yang berbeza dengan meningkatkan sintesis dan degradasi mereka.
Pertumbuhan rangka[sunting | sunting sumber]
Hormon tiroid adalah penting untuk pertumbuhan normal dan kematangan rangka.[12] Mereka mempotensikan kesan hormon pertumbuhan dan somatomedin untuk menggalakkan pertumbuhan tulang, penutupan epifisis dan kematangan tulang.[11][12]
Lipid[sunting | sunting sumber]
T3 merangsang pecahan kolesterol dan meningkatkan bilangan reseptor LDL, dengan itu meningkatkan kadar lipolisis.
Hati[sunting | sunting sumber]
T3 meningkatkan kadar denyutan jantung dan daya penguncupan, dengan itu meningkatkan output jantung, dengan meningkatkan tahap reseptor β-adrenergik dalam miokardium.[13] Ini mengakibatkan peningkatan tekanan darah sistolik dan penurunan tekanan darah diastolik. Dua kesan terakhir bertindak menghasilkan denyutan terikat yang biasa dilihat dalam hipertiroidisme. Ia juga mengimbangi protein filamen tebal miosin, yang membantu meningkatkan pengecutan. Langkah klinikal yang berguna untuk menilai kontraksi ialah masa antara kompleks QRS dan bunyi jantung kedua. Ini sering berkurangan dalam hipertiroidisme.
Perkembangan[sunting | sunting sumber]
T3 mempunyai kesan yang mendalam terhadap perkembangan embrio dan bayi. Ia menjejaskan paru-paru dan mempengaruhi pertumbuhan postnatal sistem saraf pusat. Ia merangsang pengeluaran mielin, penghasilan neurotransmitter, dan pertumbuhan akson. Ia juga penting dalam pertumbuhan linear tulang.
Neurotransmitter[sunting | sunting sumber]
T3 boleh meningkatkan serotonin dalam otak, khususnya dalam korteks serebrum, dan mengawal turun reseptor 5HT-2, berdasarkan kajian di mana T3 membalikkan ketidakberdayaan terpelajar dalam tikus dan kajian fisiologi otak tikus.[14]
Fungsi fisiologi[sunting | sunting sumber]
Hormon tiroid bertindak meningkatkan perolehan protein. Ini mungkin berfungsi sebagai fungsi penyesuaian berhubung dengan sekatan kalori jangka panjang dengan protein yang mencukupi.[15][16] Apabila kalori kekurangan bekalan, pengurangan dalam perolehan protein boleh mengurangkan kesan kekurangan itu.
Pengukuran[sunting | sunting sumber]
Triiodotironina boleh diukur sebagai triiodotironina bebas yang merupakan penunjuk aktiviti triiodotironina dalam badan. Ia juga boleh diukur dalam jumlah keseluruhan yang juga termasuk triiodotironina yang terikat kepada globulin pengikat tiroksina.[17]
Kegunaan[sunting | sunting sumber]
Rawatan gangguan kemurungan[sunting | sunting sumber]
Penambahan triiodotironina kepada rawatan sedia ada seperti SSRI adalah salah satu strategi pembesaran yang paling banyak dikaji untuk kemurungan refraktori,[18] namun kejayaan mungkin bergantung pada dos T3. Kajian siri kes jangka panjang oleh Kelly dan Lieberman terhadap 17 pesakit dengan kemurungan unipolar refraktori utama mendapati bahawa 14 pesakit menunjukkan peningkatan simptom yang berterusan dalam jangka masa purata dua tahun, dalam beberapa kes dengan dos T3 yang lebih tinggi daripada dos tradisional 50 µg diperlukan untuk mencapai kesan terapeutik, dengan purata 80 µg dan tempoh dos selama 24 bulan; julat dos: 25–150 µg.[18] Penulis yang sama menerbitkan kajian retrospektif 125 pesakit dengan dua kategori gangguan bipolar II dan NOS yang paling biasa yang rawatannya sebelum ini tahan terhadap purata 14 ubat lain. Mereka mendapati bahawa 84% mengalami peningkatan dan 33% mengalami remisi penuh dalam tempoh purata 20.3[[:]] (sisihan piawai 9.7). Tiada pesakit yang mengalami hipomania semasa menjalani T3.[19]
Suplemen penurun lemak[sunting | sunting sumber]
3,5-Diiodo-L-tironina dan 3,3′-diiodo-L-tironina digunakan sebagai bahan dalam suplemen kehilangan lemak tertentu yang dijual bebas, direka untuk bina badan . Beberapa kajian telah menunjukkan bahawa sebatian ini meningkatkan metabolisme asid lemak dan pembakaran tisu lemak adipos dalam tikus.[20][21]
Perubatan alternatif[sunting | sunting sumber]
Triiodotironina telah digunakan untuk merawat sindrom Wilson, suatu diagnosis perubatan alternatif yang tidak diiktiraf sebagai keadaan perubatan oleh perubatan arus perdana. Diagnosis ini melibatkan pelbagai gejala tidak khusus yang dikaitkan dengan tiroid, meskipun dengan ujian fungsi tiroid biasa. Persatuan Tiroid Amerika telah menimbulkan kebimbangan bahawa rawatan yang ditetapkan dengan triiodotironina berpotensi berbahaya.[22]
Sejarah[sunting | sunting sumber]
Pada 1950, ahli endokrinologi Jack Gross datang ke Institut Penyelidikan Perubatan Kebangsaan British untuk bekerja dengan Rosalind Pitt-Rivers sebagai felo pascadoktoral. Gross mempunyai pengalaman sebelum ini bekerja di Universiti McGill di bawah Profesor Charles Leblond, di mana mereka menggunakan iodin radioaktif untuk mengkaji fisiologi hormon tiroid dan menggunakan kromatografi untuk menganalisis protein radioiodinasi dalam darah manusia selepas terapi radioiodin. Gross dan Leblond menemui sebatian radioaktif yang tidak diketahui dalam darah tikus yang diberi iodin radioaktif. Sebatian itu berhijrah dekat dengan tiroksin dalam kromatografi dan mereka pada mulanya menamakannya "awanama 1". Pada masa itu, kumpulan yang diketuai oleh Jean Roche di Paris menggambarkan aktiviti penyahiodinan dalam kelenjar tiroid biri-biri, menimbulkan kemungkinan bahawa "awanama 1" ialah analog T4 yang kurang iodinasi, triiodotironina.[23] Pada Mac 1952, Gross & Pitt-Rivers menerbitkan kertas kerja dalam The Lancet bertajuk "Pengenalan 3: 5: 3'-L-triiodotironina dalam plasma manusia".[24]
Walaupun Gross & Pitt-Rivers biasanya dikreditkan dengan penemuan T3, sebatian ini sebenarnya mula diasingkan oleh ahli biokimia Hird & Trikojus di Universiti Melbourne pada 1948.[25] Telah dicadangkan bahawa kertas terbitan mereka kurang diketahui dan dengan itu mudah diabaikan.[26] Ia juga telah menyatakan bahawa Pitt-Rivers telah membaca kertas ini tetapi gagal menyebutnya.[27]
Rujukan[sunting | sunting sumber]
- ^ "Physiologic Effects of Thyroid Hormones". Colorado State University. 2010-07-24. Dicapai pada 2013-09-29.
- ^ "How Your Thyroid Works – "A delicate Feedback Mechanism"". endocrineweb. 2012-01-30. Dicapai pada 2013-09-29.
- ^ "Cytomel (Liothyronine Sodium) Drug Information". RxList. 2011-01-03. Dicapai pada 2013-09-29.
- ^ "Thyroid Hormone Toxicity". Medscape. WedMD LLC. 23 April 2014. Dicapai pada 2 May 2014.
- ^ Boron WF (2005). Medical Physiology: A Cellular And Molecular Approach. Philadelphia, PA: Elsevier / Saunders. m/s. 1300. ISBN 1-4160-2328-3. LCCN 2004051158.
- ^ "Differences in hypothalamic type 2 deiodinase ubiquitination explain localized sensitivity to thyroxine". The Journal of Clinical Investigation. 125 (2): 769–781. February 2015. doi:10.1172/JCI77588. PMC 4319436. PMID 25555216. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Nuclear thyroid hormone receptors". The Journal of Clinical Investigation. 86 (6): 1777–1782. December 1990. doi:10.1172/JCI114906. PMC 329808. PMID 2254444.
- ^ "[Absorption, transport and bio-availability of iodothyronines]" [Absorption, transport and bio-availability of iodothyronines]. Deutsche Medizinische Wochenschrift (dalam bahasa Jerman). 133 (31–32): 1644–1648. August 2008. doi:10.1055/s-0028-1082780. PMID 18651367.
- ^ References used in image are found in image article in Commons:Commons:File:Thyroid_system.png#References.
- ^ triiodothyronine resin uptake test from Farlex Medical Dictionary, citing: Mosby's Medical Dictionary, 8th edition. 2009, Elsevier.
- ^ a b Costanzo LS (2018). Physiology (ed. 6th). Philadelphia, PA. m/s. 425. ISBN 978-0-323-47881-6. OCLC 966608835.
- ^ a b Barrett KE, Barman SM, Brooks HL, Yuan JX, Ganong WF (2019). Ganong's review of medical physiology (ed. 26th). [New York]. m/s. 364–365. ISBN 9781260122404. OCLC 1076268769.
- ^ "Thyroid physiology and tests of function". Anaesthetist.com.
- ^ "Triiodothyronine-induced reversal of learned helplessness in rats". Biological Psychiatry. 20 (9): 1023–1025. September 1985. doi:10.1016/0006-3223(85)90202-1. PMID 2992618.
- ^ "Effect of long-term calorie restriction with adequate protein and micronutrients on thyroid hormones". The Journal of Clinical Endocrinology and Metabolism. 91 (8): 3232–3235. August 2006. doi:10.1210/jc.2006-0328. PMID 16720655.
- ^ "Effects of dietary caloric restriction and aging on thyroid hormones of rhesus monkeys". Hormone and Metabolic Research = Hormon- und Stoffwechselforschung = Hormones et Metabolisme. 34 (7): 378–382. July 2002. doi:10.1055/s-2002-33469. PMID 12189585.
- ^ Military Obstetrics & Gynecology – Thyroid Function Tests In turn citing: Operational Medicine 2001, Health Care in Military Settings, NAVMED P-5139, May 1, 2001, Bureau of Medicine and Surgery, Department of the Navy, 2300 E Street NW, Washington, D.C., 20372-5300
- ^ a b "Long term augmentation with T3 in refractory major depression". Journal of Affective Disorders. 115 (1–2): 230–233. May 2009. doi:10.1016/j.jad.2008.09.022. PMID 19108898.
- ^ "The use of triiodothyronine as an augmentation agent in treatment-resistant bipolar II and bipolar disorder NOS". Journal of Affective Disorders. 116 (3): 222–226. August 2009. doi:10.1016/j.jad.2008.12.010. PMID 19215985.
- ^ "Effect of 3,5-di-iodo-L-thyronine on the mitochondrial energy-transduction apparatus". The Biochemical Journal. 330 (Pt 1): 521–526. February 1998. doi:10.1042/bj3300521. PMC 1219168. PMID 9461551.
- ^ "3,5-diiodo-L-thyronine powerfully reduces adiposity in rats by increasing the burning of fats". FASEB Journal. 19 (11): 1552–1554. September 2005. doi:10.1096/fj.05-3977fje. PMID 16014396. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "ATA Statement on "Wilson's Syndrome"". American Thyroid Association. 24 May 2005.
- ^ "HISTORY: Rosalind Pitt-Rivers, the co-discoverer of T3 hormone". Thyroid Patients Canada (dalam bahasa Inggeris). 2018-08-05. Dicapai pada 2022-09-13.
- ^ "The identification of 3:5:3'-L-triiodothyronine in human plasma". Lancet. 1 (6705): 439–441. March 1952. doi:10.1016/s0140-6736(52)91952-1. PMID 14898765.
- ^ Hird, F.; Trikojus, V. M. (June 1948). "Paper partition chromatography with thyroxine and analogues". The Australian Journal of Science. 10 (6): 185–187. ISSN 0365-3668. PMID 18875255.
- ^ Hulbert, Anthony J. (2001). The comparative physiology of vertebrate metabolism :studies of its evolution, control and development (Tesis) (dalam bahasa English). UNSW Sydney. doi:10.26190/unsworks/14477.CS1 maint: unrecognized language (link)
- ^ Humphreys, L. R., "Trikojus, Victor Martin (Trik) (1902–1985)", Australian Dictionary of Biography (dalam bahasa Inggeris), Canberra: National Centre of Biography, Australian National University, dicapai pada 2023-07-27
Pautan luar[sunting | sunting sumber]
- Triiodotironina terikat kepada protein dalam PDB
- T 3 di Ujian Makmal Dalam Talian
- ECHA InfoCard ID from Wikidata
- Articles containing unverified chemical infoboxes
- Chembox image size set
- Articles with short description
- Short description matches Wikidata
- Toksikologi
- Hormon manusia
- Eter difenil
- Agonis reseptor hormon tiroid
- Hormon kelenjar tiroid
- Terbitan tirosina teriodin
- Hormon paksi hipotalamus-pituitari-tiroid

